- 作者/山田昌治;譯者/吳佩俞
小麥蛋白質在麵粉的狀態下是堅硬且不易變形的,不過一旦加水搓揉就會產生變化,成為具有獨特彈性與黏性的物質。這種同時具備彈性與黏性的性質稱為「黏彈性(Viscoelasticity)」。如先前所提到的,因為室溫的水不會造成澱粉糊化,所以可以說這種黏彈性是因為小麥蛋白質才得以出現。

接下來,我們就針對小麥當中的蛋白質種類及性質加以解說。
小麥蛋白質的水合物稱為「麩質( gluten)」。蛋白質是一種由許多胺基酸聚集構成的串珠狀天然高分子(macromolecule),構造相當複雜。在這裡,我們先省略蛋白質構造的相關說明,把重點放在麩質的物理特性解析,並試著以湯馬斯.奧斯本(Thomas Osborne)的分餾(fractionation)分析法來進行說明。
奧斯本的分餾法是將麩質加入極性(溶解蛋白質的性質)較弱的溶劑當中,接著對溶出的蛋白質性質進行測試檢查,而無法溶出的物質會再繼續浸入極性較弱的溶劑裡,然後再繼續檢查溶出蛋白質的性質,換言之,分餾是一種依序不斷重複進行的手法。使用這種方法可以得知構成小麥蛋白質的蛋白質。也就是表 1-1 的內容。

至於這份表格的閱讀方法,則是若為白蛋白(albumin),可溶在水中,不溶於水的球蛋白(globulin)則是溶入鹽水裡,然後這樣就能由上而下依序看出各種蛋白質能夠溶解和不能溶解的溶劑了。
- 白蛋白
白蛋白的主要成分為澱粉酶抑制劑,不過其特性是只會抑制動物性澱粉酶,並不會對植物性澱粉酶產生抑制。許多研究學者都認為這可能是小麥種子為了避免被動物和昆蟲吃掉,才會發展出此種防禦特性。這也是大家說生吃小麥麵粉會讓胃腸不適的原因之一。
- 球蛋白
所謂的「球蛋白」,就是無法溶入水中、但卻能以「食鹽水」萃取出的「餾分」。目前已經知道這是一種可溶於鹽水的蛋白質。雖然佔比極低,僅有 3 %,不過球蛋白擁有 α-澱粉酶、β-澱粉酶、蛋白酶(protease)等許多對於植物維持生命活動極為重要的酵素。
- 麥膠蛋白
使用比食鹽水極性更強的「酒精溶液」萃取出的餾分,稱為麥膠蛋白(gliadin)。這種蛋白質具有黏性,置於斜面上會如泥流般滑動。麥膠蛋白與下面提到的麥穀蛋白(glutenin)都與小麥麵粉麵團展現的黏彈性有著密切的關聯。
- 麥穀蛋白
麥穀蛋白是一種無法溶解於酒精溶液的蛋白質,不過卻可以溶在比酒精溶液更強烈的「醋酸溶液」當中。這種蛋白質與極富彈力的性質有著密切的關聯。所謂的極富彈性,就是意味著施加力道後,只要不再使力就會恢復原狀的性質。
小麥麵團黏彈性的祕密
在小麥蛋白質中,佔有關鍵地位的就是極具彈性的麥穀蛋白和富有黏性的麥膠蛋白。那麼,麥穀蛋白又為何會富有彈性呢?
我們在前面曾提過,小麥是生長在沙漠高原地帶並持續進化的植物。在這樣的環境中,與水同為小麥所必須的氮應該會出現常態性缺乏的情況。不過,即使在如此嚴苛的環境,有時還是會因為降雨而以銨離子(ammonium ion)與硝酸鹽離子(nitrate ion)的形式來取得氮的供給。
雖然無法獲得大量的補充,但小麥還是會盡其所能地留下這些氮的養分並加以儲存。銨離子雖然會保持原狀,但硝酸鹽離子一旦轉換成銨離子,就會改以麩胺酸(glutamic acid)及麩醯胺酸(glutamine)這類胺基酸的形式儲存在種子當中。
| 含量(質量%) | |
| 麩胺酸 | 34.7 |
| 脯胺酸 | 11.8 |
| 絲胺酸 | 4.4 |
| 天門冬胺酸 | 3.7 |
| 甘胺酸 | 3.4 |
| 精胺酸 | 3.1 |
| 丙胺酸 | 2.6 |
| 蘇胺酸 | 2.4 |
| 離胺酸 | 1.9 |
| 芳香族胺基酸 | 11.0 |
| 含硫胺基酸 (branched-chain amino acid) |
4.1 |
| 支鏈胺基酸 (ammonia) |
13.1 |
| 氨 | 3.8 |
| 合計 | 100 |
小麥麩質的胺基酸組成
麩胺酸與麩醯胺酸都是蛋白質的原料,利用這些原料所合成的蛋白質即被稱為儲藏蛋白(storage protein)。因此,小麥種子當中的蛋白質就是由麩胺酸、麩醯胺酸,以及作為誘導體的脯胺酸(proline)以極高比率所構成的。
麥穀蛋白加水揉和,結構開始變化
如同圖① 所顯示的,麥穀蛋白的構造是兩條帶子於末端互相連結。因為麥殼蛋白也是一種蛋白質,所以這種「帶子」其實是由胺基酸連結成為一長串而形成的。

我們在前面提過,麥殼蛋白的構成胺基酸因含有較多麩醯胺酸,所以乾燥狀態下會因麩醯胺酸彼此結合而變成兩條軌道般的形狀。此時加水揉和的話,水分就會進入這兩條軌道之間,成為圖② 那樣的小圓圈。

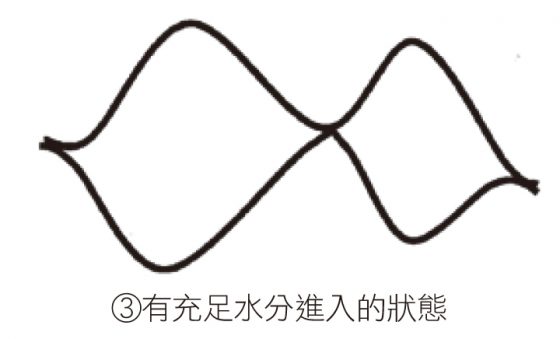
如果再繼續加入大量水分,即會出現如同圖③ 的大圓圈。看到這張圖,大家應該就能夠感受到小麥麵粉具有的彈性了。
擁有泥土般黏性的小麥麵團
另一方面,若從分子等級來觀察,可以發現麥膠蛋白呈現微小球狀,直覺上就給人似彈珠滾來滾去那種滑動的感覺,所以在目視程度時,就會有如泥土般地溢流移動。這種泥土般流動的性質稱為「黏性」。
因此,麥穀蛋白的彈性與麥膠蛋白的黏性彼此混合在一起後,就形成了小麥麵粉麵團的性質。從這層意義來看,小麥麵粉麵團的物理性質也可以稱為黏彈性質。
麥殼蛋白、麥膠蛋白的每一個單位(domain,結構域)大小約僅有數奈米(奈米:10億分之1公尺),不過,這些結構域會因各種相互作用而連結起來,並且聚合(polymerization)成為目視程度尺寸的薄膜般構造。
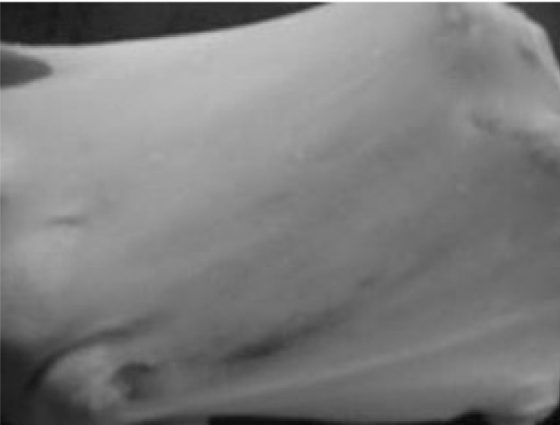
上圖就是將小麥麵粉與水混合並充分搓揉後的麵團狀態。這點從麵團延展性極佳,且呈現為可透光至對側的薄膜就能看得出來。
掌控空間、溫度與時間,做出專屬口感
麵團之所以延展良好,其實是來自於結構域彼此結合的相互作用,但其中原因為何正是長年研究小麥學者們的課題。目前知道的是這與名為交聯(cross-link)的結合作用有著密切的關係。
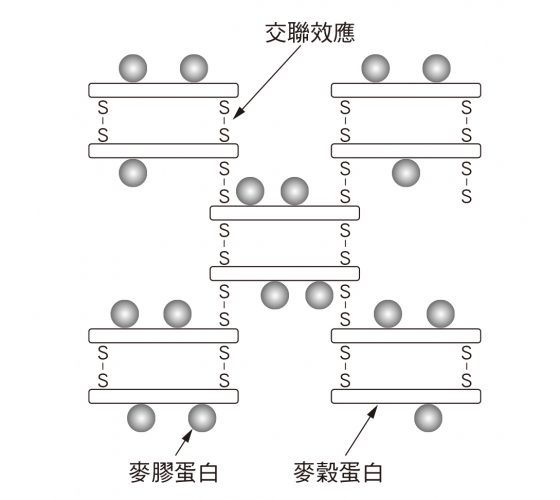
因為交聯的形成屬於一種化學反應,所以也會依循化學反應的一般規則。換言之,只要充分混合拌勻,就能提高與反應相關部分的促發機率,進而開展交聯作用。這種情況就稱之為「空間效果」。
另外,我們也可以說溫度較高時亦較容易進行化學反應。這種情況被稱為溫度效果。還有,花費較多時間也能使化學反應持續進展。這個情況則稱之為時間效果。
空間效果、溫度效果,以及時間效果這三大原則,對於思考麩質的形成與控制是很有幫助的。
舉例來說,烤點心時,如果充分揉和麵團,就會做出脆硬口感的餅乾,但若只是稍加搓揉,就會成為鬆軟口感的點心。不同揉製方法帶來不同口感,應該就是交聯作用的空間效果。此外,製作烏龍麵時,也是有個充分揉和後放上一晚靜置醒麵的作業,這個程序的重點應該就是交聯作用的時間效果了。