人類改良
二○一三年,「去滅絕」觀念在集結分子生物學者、環保主義者與記者的 TED x 去滅絕研討會上廣受接納,與會者討論了讓長毛象、袋狼(Tasmanian tiger)等物種起死回生的可能性。布蘭特在會上發表了一場引人深思的演說,論及生物多樣性的喪失,以及利用丘奇的科技再次賦予滅絕動物生命的機會。他藉著研討會與 TED 平臺推出「基因重現及復原計畫」(Revive and Restore),旨在調查生物滅絕的原因、保存生物學與遺傳上的多樣性,並且應用生物科技修復我們的生態系統。
布蘭特的 TED 演講大受好評,同時卻也令許多人又驚又怒,一些科學家、環保主義者聽到布蘭特想讓滅絕已久的生物死而復生,不禁感到十分驚恐。這可不僅是複製現存的動物那麼簡單——也不是在複製曾經生存在地球上的動物——而是模糊了現存與滅絕動物之間原本分明的壁壘。況且,丘奇也表明自己不僅對長毛象與鴿子感興趣,還想拿尼安德塔人(Neanderthal)的 DNA 來做實驗——他不僅想復活其他動物,甚至想改良人類。
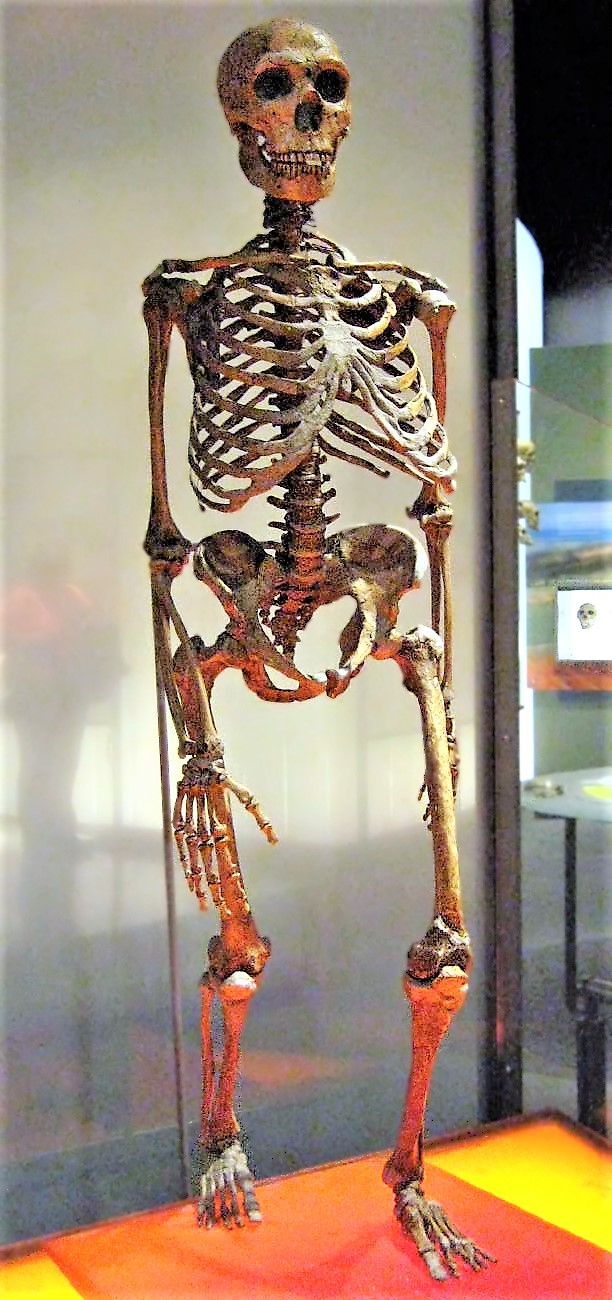
你也許和過去的科學家一樣,認為尼安德塔人是原始的次人類物種,基本上就是粗獷、野蠻版的人類。不過從近期的研究看來,尼安德塔人其實十分聰明,他們不僅建造了有組織的文明,以物種而言也十分成功,存活了二十五萬年。(作為對比,研究者認為最古老的智人〔Homo sapiens〕生存於三十萬年前的地球。)尼安德塔人的身體能有效保溫,因此能在嚴酷的環境生存,而且他們非常強壯——這部分倒是符合人們對他們的刻板印象——卻也擁有良好的精細肌動技能(fine motor skills),能夠做到精細的動作。若製作智人與尼安德塔人(Homo neanderthalensis)的雜交種,或許就能創造較健壯的人類物種,這種新尼安德塔人可能可以面對現代的氣候變遷難題與極端天氣事件,也比較有可能在遷徙至全新環境時存活下來。
目前已經有人定序歐洲與亞洲出土的幾組尼安德塔人化石基因體,接下來科學家便能小片段分析與合成此基因體,在人類幹細胞中拼組出正確的尼安德塔人 DNA 序列,如此一來,理論上就能做出尼安德塔人複製體了。我們來聽聽丘奇的說明吧:
你會先從成年人類的幹細胞基因體著手,逐步反向操作回推至尼安德塔人基因體,或者是合理程度上相近的基因體。這些幹細胞可以生產組織與細胞。假如未來社會接受複製動物的觀念,也重視真正的人類多樣性,那甚至能將完整的尼安德塔人複製出來。
出生於現代的尼安德塔人當然會面臨許多挑戰,舉例而言,典型的西方人飲食多為乳製品、精緻穀物製品與加工食品,即使是鐵胃的尼安德塔人可能也無法消化塔可鐘(Taco Bell)的起司玉米片多力多滋瘋狂塔可餅——你如果沒吃過,可以把它想像為多力多滋做成的塔可餅,裡頭包著調味過的廉價絞肉與抗結劑做成的切達起司混合物。尼安德塔人再怎麼健壯,兩份塔可餅下肚後,他們——還有他們的史前消化系統——想必也會舉旗投降。

你或許認為復活尼安德塔人這種想法糟糕至極,那如果我們單純借用幾段尼安德塔人基因,稍微修改人類自己的身體呢?你想想看,尼安德塔人可是沒有乳糜瀉(celiac disease)這種疾病,不會像現代一些人一樣對麩質過敏而導致身體疼痛。他們的免疫反應與我們不同,研究者也許能藉助尼安德塔人免疫系統,找出根治類風溼關節炎(rheumatoid arthritis)、多發性硬化症(multiple sclerosis)與克隆氏症(Crohn’s disease)等自體免疫疾病的方法。此外,尼安德塔人的骨骼非常堅硬,我們也許能借用骨骼密度相關的基因,用以治療數億女性在逐漸老化時不得不面對的骨質疏鬆問題。
***
你也許會覺得混合尼安德塔人與智人基因並讓代理孕母生下這樣的融合生物,聽起來完全就是恐怖片或反烏托邦科幻小說的劇情——沒錯,許多虛構作品的確探討了類似的議題,而在大部分故事中,人類試圖改變上帝偉大的計畫時,往往會招致災難。這類作品包括:H.G.威爾斯(H. G. Wells)的《攔截人魔島》(The Island of Dr. Moreau,一八九六)、阿道斯.赫胥黎(Aldous Huxley)的《美麗新世界》(Brave New World,一九三一)、法蘭克.赫伯特(Frank Herbert)的《沙丘》(Dune,一九六五)、娥蘇拉.勒瑰恩(Ursula Le Guin)的《黑暗的左手》(The Left Hand of Darkness,一九六九)、南希.克雷斯(Nancy Kress)的《西班牙乞丐》(Beggars in Spain,一九九一),以及理查.摩根(Richard Morgan)的《碳變》(Altered Carbon,二○○二)。這同時也是《星艦迷航記》(Star Trek)與漫威(Marvel)X戰警(X-Men)系列頻頻討論的議題,後者的反派角色萬磁王(Magneto)甚至打算「讓智人臣服於變種人!」。
綜觀歷史,無論是科學或社會都不樂見任何人扮演上帝,甚至是談論扮演上帝相關的議題。瑪麗.雪萊僅僅是撰寫了關於怪物的故事——並不是創造出真正的怪物——就因為故事太具顛覆性而不敢以本名出版作品,以免政府剝奪她扶養孩子的權利。

桃莉羊成功複製出來時,全球各地無數人召開了緊急會議與記者會,幾乎無人注意到桃莉羊計畫明文道出的宗旨:增進我們對生物發育過程中細胞變化的瞭解。人們迅速做出了極端負面的反應,密蘇里大學聖路易斯分校(University of Missouri in St. Louis)醫學倫理學者隆納.孟松(Ronald Munson)博士對《紐約時報》表示:「精靈已經從神燈裡放出來了。」他接著質問道:下一步會是什麼,難道要用十字架上的一滴血把耶穌基督也複製出來?波士頓大學(Boston University)公共衛生學院公衛法律系主任喬治.安納斯(George Annas)教授也對生物學與遺傳學界表示譴責。「正確的反應該是驚恐才對。」他說道,並聲稱按邏輯推演,下一步想必就是複製人類了。「父母並沒有權利收集孩子的細胞,做出那個孩子的複製品。大眾對於複製人的反對聲浪是對的。」蘇格蘭教會甚至正式頒布教令,要求聯合國通過具約束力的禁令,禁止複製生物行為。該教會引用《舊約》的《耶利米書》(Jeremiah)1:4-5,表明人類不可取代上帝:「耶和華……〔說〕:『我未將你造在腹中,我已曉得你;你未出母胎,我已分別你為聖。』」美國總統比爾.柯林頓特地舉辦一場活動並安排電視轉播,在活動上宣布禁止聯邦政府提供經費給任何複製人類相關的研究計畫。
CNN與《時代》(Time)雜誌在一九九七年三月一日發表的調查結果顯示,多數美國人突然對核轉置技術——生物複製技術之一——產生了明確的意見。現在說來你也許會覺得難以置信,不過在桃莉羊誕生前,那些人大多從未花心思想過複製生物議題,也從沒思考過核轉置技術相關的問題。那份調查中,三分之一填答者表示他們為桃莉羊的存在深感不安,甚至願意參加反對生物複製的公眾示威與抗議。在桃莉羊問世將近二十五年後的今日,我們獲得了重要的知識、新生物科技,以及對生命運作模式更廣泛的理解。地球可還沒被惡魔複製羊攻占呢。多虧了桃莉羊,科學家開始複製成人的幹細胞,進而創造出人工「誘導性多功能幹細胞」(induced pluripotent stem cell,iPSC),並將之用於醫學研究。有了 iPSC 之後,利用胚胎做研究的需求減少了,多少消弭了胚胎研究多年來引起的倫理疑慮。研究者能用 iPSC 研究老化過程——並且首次將成年細胞再程序化,表現出年輕細胞的特性。這類研究開啟了新一道大門:人類也許能使用各種幹細胞療法治療疾病,畢竟解藥若出自病人自身的遺傳密碼,那就不可能受免疫系統排斥了。今天已經有許多再生醫學療法可用以治療血液相關疾病,其中包括白血病、淋巴癌(lymphoma)與多發性骨髓瘤(multiple myeloma),以及心衰竭等其他退行性疾病。
要改變人們的信念與觀感往往要花費大量時間,而這也無可厚非——我們畢竟受數百年的著作與根深柢固的社會價值觀影響。科學家經常在無預警的情況下發表驚天動地的新發現,當我們面對這些挑戰現存思想的新聞時,自然會感到震驚、疑惑,甚至是焦慮,而有時連科學界內部人士也會感到不安。當丘奇的生物去滅絕想法廣泛傳開後,《科學人》(Scientific American)的編審委員會在二○一三年寫了一篇帶諷刺意味的譴責文章,主要論點是丘奇花在這份實驗性技術上的金錢,應該用在傳統保育行動上才對。丘奇自己也在《科學人》發表一篇文章反駁他們,在文中鎮定地說明讓滅絕生物復活的目的,並表示自己的計畫不是為了製作「絕種生物的完美活體複製品,也不是為了成為實驗室或動物園裡一次性的展演」。他解釋道,他的研究重點是探討我們能對現存生態系統做出的調整,以確保在人為環境變遷過後,人類仍能存活下去。
截至二○二○年十二月,丘奇與他的哈佛研究團隊已逐步逼近他們複製長毛象的「巨大」目標了。亞洲象的基因體和長毛象約有百分之九十九.九六相似,然而剩下那百分之○.○四加總起來卻等同DNA序列當中的一百四十萬處差異。這些差異大多無關緊要,不過在我們寫這本書的目前為止,丘奇團隊已辨識出一千六百四十二段重要的不相似基因,仍須持續做研究才有可能複製出長毛象。團隊還在努力逐一設計、測試與微調他們在實驗室裡培養的細胞,希望能製作出正確的基因序列,讓類似長毛象的亞洲象得以存活下來。他們希望能用長毛象與亞洲象相似的基因作為基底,只不過這頭大象會擁有長毛象濃密的毛髮、適應嚴寒氣候的血紅素、積存多層脂肪的能力,以及其他優點,例如可讓鈉離子通透的細胞膜,這對長毛象適應冬季嚴苛環境大有幫助。在調整出正確的特性組合之後,研究團隊便能將這些改良版皮膚細胞注入幹細胞,做出活生生的(有點長毛的)長毛象。丘奇與德州企業家班恩.拉姆(Ben Lamm)在二○二一年九月成立了巨大公司(Colossal),專門支援他們的長毛象研究計畫。
假使成功製造出長毛象,這些二十一世紀版的長毛象將會居住在新的家園裡——一個靈感起源於小說家麥克.克萊頓(Michael Crichton)作品的新家,只不過這地方不會取名為侏儸紀公園,而會以更新世為名。更新世公園(Pleistocene Park,沒錯,真的是這個名字)是位於西伯利亞的實驗區,許多原生物種在多年工業化衝擊過後,終於得以重返這個自然保護區,在此再野化(rewild)的物種包括雅庫特馬、加拿大馬鹿、美洲野牛、犛牛等動物。若將修改版長毛象野放於此,就能看出大動物踩踏雪地與永凍土是否能改善氣候問題了。

——本文摘自《未來的造物者》,2023 年 11 月,臉譜出版,未經同意請勿轉載。