本文轉載自顯微觀點
細胞膜是區隔細胞與其外在環境的屏障,表面佈有許多特殊蛋白,透過不同的位置、結構和物理化學性質,讓細胞膜具有「辨別敵我」選擇讓特定物質進入細胞的功能,因此成為現今藥物設計最重要的靶點之一。
然而,這類蛋白一旦脫離細胞膜就容易變性,像被拉上岸的水母,瞬間失去原有形狀甚至硬化,導致後續的檢驗和研究遭遇瓶頸。
任教於台大化工系的教授趙玲,便以膜蛋白為研究主題,發展新方法來分離膜蛋白,建造各式細胞膜晶片以完成後續的功能研究。她更以傑出的研究於2018年獲得台灣傑出女科學家獎的新秀獎。

善用化工所學 創造細胞膜安心「躺平」環境
許多人對化工系的印象常與石化工業、傳統工廠或是有毒化學物質畫上等號,但在趙玲的研究室裡,卻充斥著培養皿、生物晶片和各種光學儀器。
「化工其實滿廣泛的,就是化學加上工程」,趙玲老師解釋,只是早期產業以石油工業為主讓大眾誤以為化工系的出路就是如此,但化工是以工程的方式將化學產品實用化,因此舉凡生活用品、製藥甚至現在提倡的永續、減碳,也都是化工觸及的研究領域。
趙玲實驗室的研究核心包括建造細胞膜平台來分離膜蛋白、利用生物晶片了解與細胞膜相關的疾病機制,以及利用細胞膜和特殊生物現象來做來做生物檢測應用或工程、材料上的應用。
對於自己以膜蛋白作為研究重心,趙玲表示起心動念希望協助科學家解決過去始終難以突破的問題。以細胞膜上主要受體之一的GPCR(G protein-coupled receptor)為例,這類受器非常重要,是許多藥物的主要靶點。
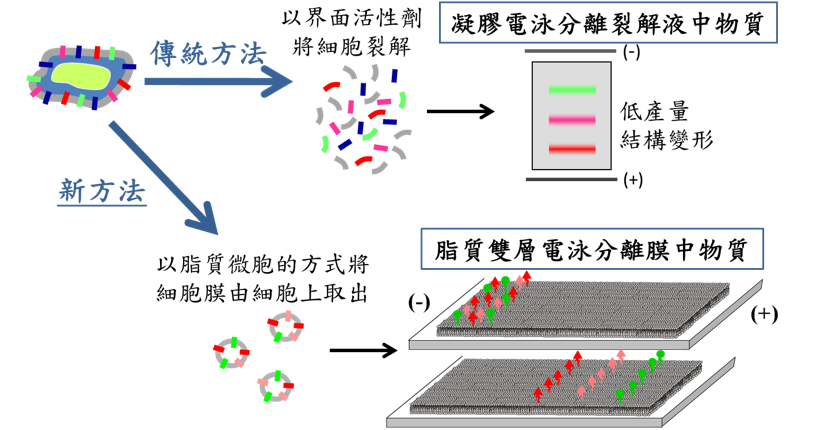
但過去研究GPCR的方式通常是在「非自然狀態」下取得。由於膜蛋白必須先用界面活性劑溶解、脫離細胞膜,直接或帶著界面活性劑一起結晶,最後研究者會嘗試把蛋白重新插入脂質體(liposome)或 奈米圓盤(nanodisc,一種保留膜蛋白結構與功能的技術),再以X光或冷凍電子顯微鏡分析。但以此傳統方法取得的膜蛋白不僅構型改變,產量也較低。
然而,GPCR 的運作非常依賴其「真實構型」與上下游分子的互動。因此,即使研究者成功取得某一個「靜態狀態」的結構,也仍無法確定那是否符合它在真正細胞環境中的運作形式,更難以推測與藥物結合後,蛋白質到底發生了什麼改變。
趙玲所開發的平台正是為了解決這個瓶頸。趙玲團隊採取的方法是在抽取膜蛋白時,以脂質微胞的方式將蛋白和細胞膜一起取出。將類似膜泡的脂質微胞鋪在平台上,再透過平台下的感測器,觀察膜蛋白再給予刺激物後,鍵結是否發生。由於研究目標的膜蛋白始終待在原本的脂質雙層中,完整保持原本的天然構型,因此與刺激物的交互作用也就更接近在原本環境中的樣貌。
而平台本身支援多種偵測方式。除了最常用的螢光分析之外,為了驗證無標記(label-free)感測的可靠度,趙玲團隊也經常把兩種方法同時使用,以便確認訊號的正確性。目前平台也正在擴展到可整合電子顯微鏡等其他技術,只要能讓膜泡穩定地鋪在感測層上,就能進一步觀察更細緻的構造與動態。
但脂質微胞如何「完整」的貼附在平台上並保持天然構型?趙玲笑稱,「這便是化工人的優勢」。
她解釋,細胞膜一旦離開細胞,就容易因為鹽濃度、pH 值或環境不穩定而破裂,因此必須精準調整這些條件,使膜能保持完整。而到了平台上,也要創造「膜喜歡」的環境,才能讓膜穩定地依附上去。
因此不論是鹽濃度、pH值、靜電力、凡得瓦力(van der Waals force)等物理化學相關的參數,都必須被考量控制。「我們理解這些力如何作用,也了解熱力學和動力學,因此可以微調整個系統」,因為這樣的學習背景,趙玲認為者也是化工人才切入生醫領域的優勢。
研究沒有冤枉路 十年磨一劍確定方法學
跨足生醫領域對趙玲來說,是偶然也是必然。雖然不是從大學就決定專注膜蛋白或細胞膜領域,但趙玲一直對生物充滿興趣,認為生物體經過漫長演化所呈現的複雜與精巧令人驚嘆,尤其當中其實藏著大量物理與化學原理。不過大學時期的學習以化工基礎學科為主,真正開始接觸相關研究主題,是進入研究所之後的事了。
當時她和許多老師討論各自的研究主題,只要覺得有興趣、能用化工的工具與思維去理解與延伸,加上原本對生命系統著迷,因此更傾向跟隨研究生物、醫藥相關題目的老師進行研究。
而博士班在美國麻省理工學院(MIT)的學習也深刻影響著趙玲。她回憶,當時麻省理工學院化工系要求學生必修生物。因為系方認為不論要要什麼解決問題,研究主題最後都回歸到「與人(生命系統)有關」,因此希望所有學生都必須修習過基礎生物,若過去沒有基礎便必須在入學後補修。
這樣的制度更讓她確信,化工並不是被侷限在化學製程或石化工業,而是能支援所有「與化學相關、且需要工程化」的領域,包括生物與醫學。
至於後來跨到細胞膜的研究,則是因為當時博士班指導教授的研究方向從表面化學逐漸延伸到生物界面。
她提到,指導教授研究領域在於表面化學不限於細胞膜,主要研究高分子塗佈、自組裝(self-assembly)等主題,後來開始對蛋白質與脂質等「生物高分子」感到興趣,開始購買不同脂質成分、在平坦的基板上自組裝,嘗試打造「人工細胞膜」。
趙玲便也開始了一系列相關研究,直到回台灣也成立了仿生膜現象及及工程實驗室,繼續從事仿細胞膜生物晶片和細胞膜上特殊現象的研究及應用。
而平台方法學的開發,一路走來也將近十年。一開始,她們必須先拿相對成熟、背景資訊充分的系統來做概念驗證,例如使用大家常使用的海拉細胞(HeLa)作為測試標的。因為這些蛋白的特性早已有完整文獻記載,研究團隊才能將自己的平台結果與既有資料比對,證明方法的可靠性。「要跟其他團隊合作,尤其是涉及昂貴或珍貴的蛋白質,合作方一定要先相信你的工具是穩定可靠的」,因此只有在前期驗證充分後,別人才會願意把高成本的蛋白或細胞系交付測試。
從一開始的概念,到平台能夠被不同領域採用、開始和外部團隊合作,趙玲認為,這段歷程不只漫長,也必須面對許多方向上的選擇。例如團隊曾經嘗試以電訊號作為主要偵測方式,結果發現為了拉高訊號強度,必須把鹽濃度降得非常低,卻不利於生物樣本的維持。「我們還是會把不同方向都試過,最後再把力氣集中在真正可行的地方」,趙玲表示這條路最後雖被放棄,但並未白走,不僅讓學生得以完成研究所學位,也讓團隊更清楚研究的方向。
建立方法學後,在應用面也需與許多不同領域的研究者合作。以新藥開發來說,細胞膜平台可作為「眾多候選藥物」的第一層過濾器。透過平台,可以讓新藥開發者觀察作用機制,甚至透過理解分子如何「從細胞膜通關」,反向思考設計符合機制的新藥。
但要建構一個能解析機制的平台,「要模仿到什麼程度才算接近真實?」趙玲認為,這也體現工程師的價值-在複雜的真實世界中抓出最重要的幾個步驟。
也因此跨領域合作對她而言不可或缺,更必須視需要應用的面向,在選擇合適合作的對象。例如生物學家提供細胞與組織層級的資訊;臨床醫師則帶來病患端的觀察。兩者的資料深度不同,可解答的問題也不同。工程師則必須在不同資料之間縫補拼圖,找到系統的「痛點」,才能設計出有效的平台。
隨著方法學的建立,一個更貼近真實細胞世界的細胞膜平台也逐步拓展應用範圍,盼成為未來探索生物機制、開發新藥物的重要推進力量。