- 林翰佐/銘傳大學生物科技學系副教授,科學月刊總編輯。
最近生命科學界爆發一宗廣受關注的事件:
中國科學家賀建奎博士將 CRISPR/Cas9 活體基因編輯技術用於人類胚胎的編輯,並經植入孕母著床懷孕後,於日前成功產下 2 名基因體受到修改的女嬰。
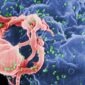
賀建奎博士宣稱,該計畫主要針對具有人類免疫缺陷病毒(HIV,即一般人俗稱的愛滋病毒)感染的夫妻,研究其對胎兒垂直感染的可能性,並藉由將受精卵中名為 CCR5 基因剔除來達到防治之目的。
賀博士似乎對此研究信心滿滿,但透過網路視頻的發表與媒體專訪披露之後,反而引發科學界與社會的震驚。在中國,數百名科學家幾乎在第一時間便聯署聲明譴責,稱此瘋狂的實驗存在著嚴重的生命倫理問題,並要求政府補上監管漏洞。聲明更直言該實驗在技術上沒有任何創新,唯一的突破是科學家的倫理道德底線。

圖/wikipedia
顯然,這樣的研究跨越了科學界普世道德標準。即便是一般社會人士,相信對於這樣的研究也會感到有所不妥。不過生命科學的相關研究道德尺度在哪裡?其實這仍有嚴謹的脈絡可循。
人體試驗的普世道德標準
探索生命一直是人類積極發展的科學議題,在人類進化的歷程當中,科學研究方向大抵朝向增進人類福祉為目標,但其中也不乏一些黑歷史,像是二次世界大戰時期納粹德國對集中營中的猶太人及日本 731 部隊對戰俘所做一系列不人道的人體試驗,這些研究顯然有其道德上的不公義性。不過,即便在承平時期,科學研究也有出岔錯的時候,例如美國發生塔斯基吉梅毒試驗 (Tuskegee syphilis experiment),原本立意良善的梅毒治療研究,在時空環境的改變下演變成為殘忍的見死不救。這些血淋淋的案例一再地揭示,以人類為主體的研究,似乎應該有明確的道德規範,藉以防止這類事情的不斷的重演。

圖/wikipedia
有鑑於此,國際相關研究社群開始著手訂定人體試驗所應遵守的倫理規範。這些規範雖並非全然具有法律上的約束力,但這些凝聚國際團體共識的議定界定了普世對人體試驗中倫理的基本要求,因此幾經更迭修改,許多規範仍沿用至今,例如紐倫堡宣言 (Nuremberg Code)、赫爾辛基宣言 (Declaration of Helsinki) 及貝爾蒙特報告書 (Belmont Report) 等。
基本上,這些宣言與報告楬櫫人體試驗中應該遵行的 3 項重要的倫理基礎,分別為:
- 對人的尊重 ── 包括對人權的維護以及對受試個人的尊重。
- 善意的對待 ── 窮盡實驗的設計與執行降低對實驗者的傷害。
- 公平正義。
這些意涵也被各國的立法單位所重視,並將精神落實於立法之中,例如目前臺灣的「醫療法」中,即規定「人體試驗委員會」的設立,針對凡涉及人體及其組織檢體的研究進行實質上的審查,透過審核機制的管控確保研究計畫的品質,並保障對受試者的尊重以及各種權力的維護。
人類胚胎的研究與對社會的衝擊
人類胚胎的研究一直是生命科學研究上道德的邊緣地帶,爭議的觀點有很多,除了部分宗教裡對於「人」形成的見解之外,更廣泛的關注在於胚胎是否應視為人而賦予其等同於人的權利。
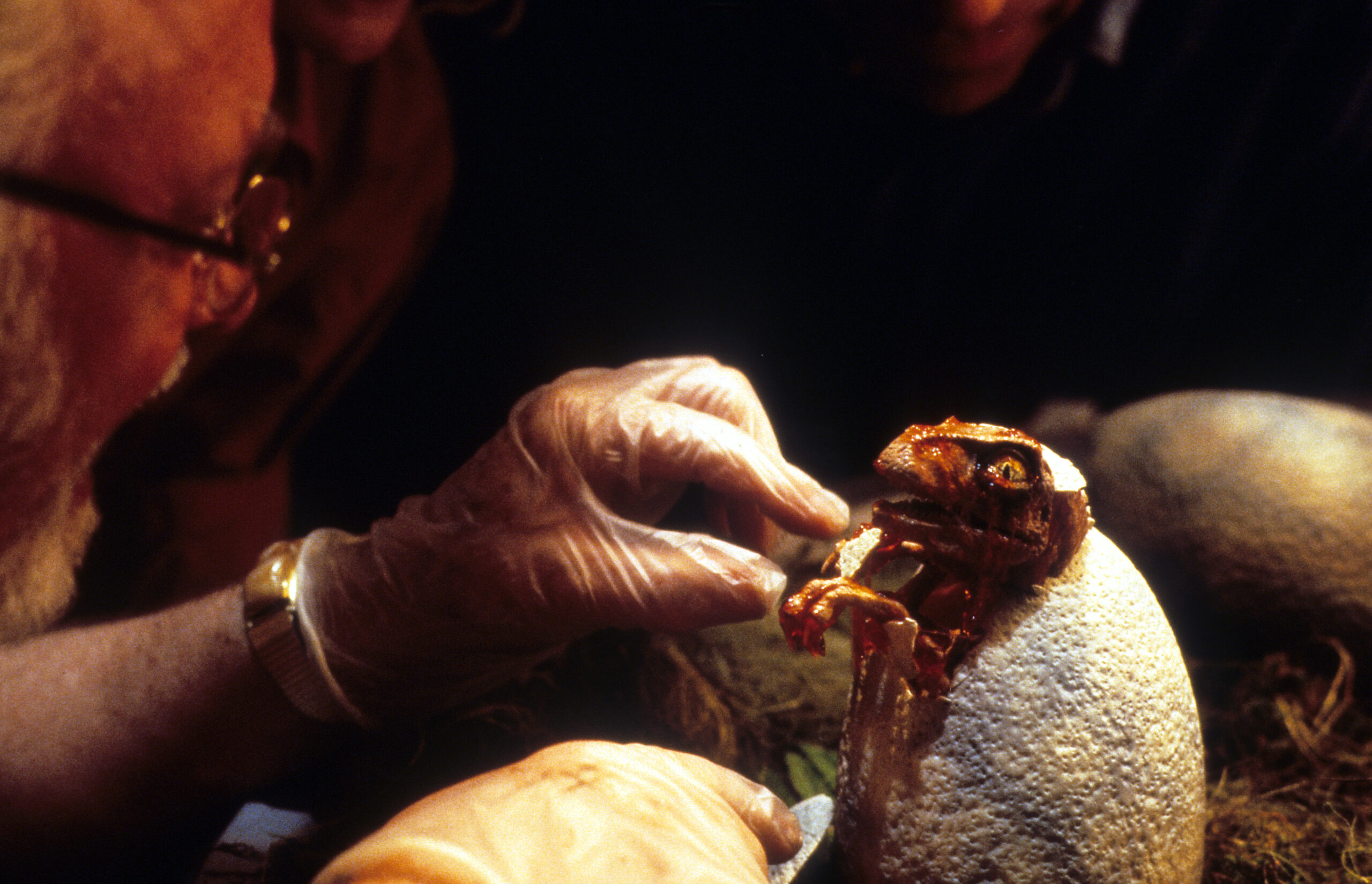
雖說我國《民法》中規定「人之權利能力,始於出生,終於死亡。」,但並不意味著可對未出生的人類胚胎得以高唱科學為名為所欲為。在 1997 年透過核轉殖技術成功培育出第一隻高等哺乳動物「桃莉羊」,隨即引發人類社會的重視,其中的原因就是意識到人類科技的進展以迅雷不及掩耳的速度發展至今,已有操弄胚胎,改變生命的可能。發明人威爾穆特博士 (Sir Ian Wilmut) 在成名之後旋即受到梵蒂岡天主教教宗的召見垂詢,足見其影響性。即便這類高等動物的複製技術未來商機無限,科學家宣稱可以透過預定的方式訂做一個 mini me,作為未來器官移植的備料庫,但更多反對的聲浪也接踵而至,例如這樣直接取用他人器官的方式是否合法的問題。

圖/wikipedia
生命科技進展對社會的另一次震撼教育發生於人類胚胎幹細胞 (embryonic stem cells) 的相關研究,所謂胚胎幹細胞係指位於囊胚期 (blastocyst) 胚胎中位於特定區域;內細胞團 (inner cell mass) 中游離出來的細胞。先前的研究顯示,胚胎幹細胞具有多元分化 (pluripotency),可以透過誘導技術分化成人體內任何一種型態的細胞,故具有相當的醫療未來性。
然而,人類胚幹細胞株的建立必須透過破壞一顆胚胎來獲得,這種殺生式的救人科學在道德層面上有著尷尬的地位。美國國會曾於 1996 年通過所謂的迪基維克法案 (Dickey-Wicker Amendment),禁止聯邦的經費資助足以製造或摧毀人類胚胎幹細胞用之研究,企圖從金源上來限縮該領域的發展,然而囿於龐大的醫療商機,確保戰略上的科技競爭優勢,該法案已於 2009 年由美國聯邦法案明令廢止。
讓我們再回到賀博士的問題
談到這裡,相信讀者會明顯的感受到問題的渾沌性,所有論述似乎只有原則與道德上的說明,而無明確的、法律上的明文規定。
看起來的確如此,科技進展如此迅速與日益複雜,立法部門很難跟上腳步;另從實務的角度來看,法律保障的對象仍以現身在世者,在民主國家的政權當中更可能進一步的限縮於那些具有投票資格的選民,畢竟其為所謂的「民意基礎」,花心思在一個並不存在的個體為其設立法律謀求應有的福祉,並不是立法機構的首要任務。所以一切的把關機制,完全存乎研究主事者一心。
CRISPR/Cas 9 技術無疑是 21 世紀生物科學界最偉大的發現之一,透過這項技術可以實踐在世界上絕大多數生物體內誘導基因體的修改。然而此技術的不確定性也是眾所周知──整個技術如同拿霰彈槍獵鳥,除了目標,也會有「脫靶」造成其他基因被誤擊的可能──對人類胚胎而言,這意味著致癌機率的增加及未來衍生之代謝疾病發生的可能性。
更離譜的是,該實驗的設計與問題解決之間並沒有存在著必然性,反而有極大的機會衍生更多的問題。流行病學中研究中所論及的是擁有特殊亞型之 CCR5 基因的白血球可以降低 HIV 病毒感染的特性,但賀博士的作法是極端地利用 CRISPR 技術將 CCR5 基因的運作硬生生停止, CCR5 基因在器官發育等生理機轉中均扮演著重要的角色,僅為防止 HIV 病毒入侵的可能就大費周章的摘除宛如削足適履。
筆者認為,除了急功近利,實在看不出這樣的研究真正的學術價值。人體胚胎研究不比實驗動物,我們必須為出生的生命負責,不知道賀博士是否有想過這樣更深層的意義?

圖/pixabay
延伸閱讀
- 臺灣學術倫理教育資源中心
- 林翰佐,〈物種基因剔除技術爆炸性的新突破 ─ CRISPR/Cas9 技術淺談〉,《科學月刊》,第 552 期,2015 年 12 月。
〈本文轉載自《科學月刊》2019年1月號〉
一個在資訊不值錢的時代中,試圖緊握那知識餘溫的科普雜誌。