兩年前,哥倫比亞大學醫學中心(Columbia University Medical Center)的研究指出,老鼠腸道內的細胞可以轉換成可以分泌胰島素的細胞,最新的發現指出,相似的原理也能應用在人類身上。
第一型糖尿病的病因在於胰腺裡負責分泌胰島素的β(Beta)細胞失能,科學家一直試圖利用幹細胞製造出能代替胰腺裡B細胞的「代理胰臟細胞」,希望能在需要的時候代替胰臟細胞釋放胰島素至血液中。
然而,即使科學家的確能在實驗室中利用胚胎幹細胞(embryonic stem cell)製造出能產生胰島素的細胞,那些成品卻不適合移植到糖尿病病人體內,因為那些人造細胞並不懂得對血糖作出反應,也無法判斷釋放胰島素的正確時機,也就是說如果真的把它移植到病人體內,這些人造細胞會不分青紅皂白地在不需要的時候釋放胰島素,導致病人血糖過低而死。
不同於一心想著要把胚胎幹細胞或內層祖細胞(induced pluripotent stem)轉化成代理胰島細胞的思維,一項新的技術可能比較簡單一點,只要想辦法抑制腸道細胞內的FOXO1轉化因子,或許就能讓腸道自行分泌胰島素。
哥倫比亞大學醫學博士Domenico Accili和他的博士後研究生Ryotaro Bouchi今年六月在自然通訊期刊(Nature Communication) 提出一篇論文名為〈FOXO1 inhibition yields functional insulin-producing cells in human gut organoid cultures.〉當中提到了這個新穎的想法。
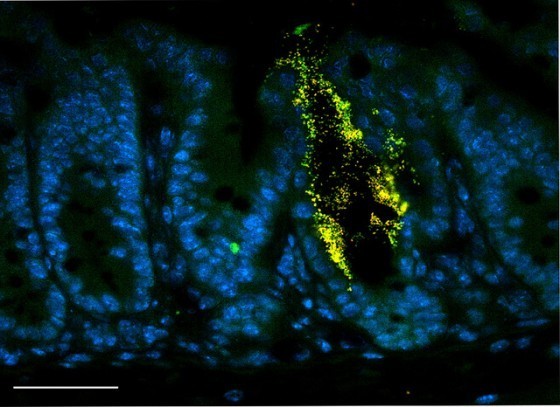
他們首先利用多功能幹細胞(pluripotent stem cells)做出人類腸道的組織模型,並透過基因工程(genetic engineering)抑制了當中FOXO1因子的所有活動,七天之後,當中的細胞便開始製造胰島素,甚至會對葡萄糖產生相應的反應。
「利用人類幹細胞製成的腸道組織模型,我們成功證明只要利用顯性負突變體(dominant-negative mutant)或慢性病毒小髮夾RNA(hairpin RNA,一種可以使基因表現沈默化的RNA序列)抑制FOXO1,就能促進腸道內可以分泌胰島素的細胞生長,那些細胞的特性幾乎和成熟的胰腺B細胞無異,而且能成功在老鼠體內存活。」Domenico Accili在論文中提到:「這個新發現提升了以腸道作為標地製造胰島代理細胞,藉以治療糖尿病的可能。」
事實上,科學家先前已經施行類似的技術在老鼠身上,那些被製造出來的胰島素確實能順利釋放到老鼠的血液之中,甚至能讓患有糖尿病的老鼠恢復正常血糖指數,那項實驗在2012年刊載在《自然遺傳學期刊》(Nature Genetic)上。
「我們已經証實人類細胞對於這項技術的反應與老鼠細胞相同,接下來我們希望這項技術能在真的實際應用在糖尿病的治療。」Accili博士正著手研究能順利抑制腸道細胞FOXO1因子的藥物。
參考資料:
Gutting Out a Cure for Diabetes? Human GI Cells Retrained to Make Insulin. GEN News.[June 30 2014]