- 作者/照護線上編輯部
- 本文轉載自 Care Online 照護線上《對付去勢抗性攝護腺癌,PARP 抑制劑標靶治療解析,泌尿專科醫師圖文懶人包》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接

60 多歲的李先生有頻尿、夜尿、解尿不順的狀況,原本以為是良性攝護腺肥大,但在就醫之後,才發現竟然是攝護腺癌,而且切片檢查的結果顯示患者屬於高惡性度攝護腺癌。台中慈濟醫院泌尿科顧問裘坤元醫師指出,接受荷爾蒙治療一段時間後,攝護腺癌細胞便出現去勢抗性,而改用化學治療。
大約一年半後,患者的攝護腺癌已轉移至骨骼、肝臟、肺臟。裘坤元醫師說,因為基因檢測的結果顯示患者具有 BRCA 基因突變,於是開始使用口服 PARP 抑制劑標靶藥物。在 PARP 抑制劑標靶藥物的治療下,攝護腺特定抗原 PSA 指數有下降的趨勢,而且骨頭疼痛也大幅改善。
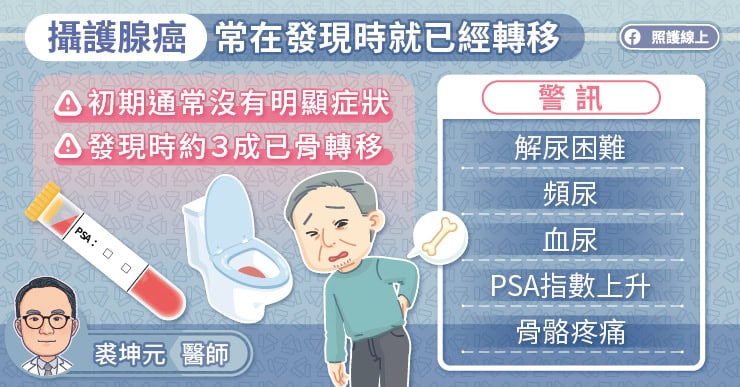
「早期的攝護腺癌沒有症狀!」裘坤元醫師指出,「在台灣,有一半的患者在診斷攝護腺癌的時候就已經是比較晚期的狀況,甚至有三成以上已經轉移到骨頭。」
攝護腺癌可能造成頻尿、夜尿、解尿困難等症狀,患者會誤以為是良性攝護腺肥大,而延誤就醫。裘坤元醫師說,攝護腺癌容易轉移至骨骼、淋巴結,可能造成骨骼疼痛。
針對轉移性攝護腺癌必須使用全身性治療,裘坤元醫師說,首先是使用荷爾蒙治療,因為男性荷爾蒙會刺激攝護腺癌生長,所以會利用藥物將男性荷爾蒙降到最低濃度,稱為去勢性治療。
荷爾蒙治療能夠有效抑制攝護腺癌生長,讓患者的病情得到控制,但是在經過 2 至 3 年的荷爾蒙治療後,攝護腺癌可能出現去勢抗性。裘坤元醫師說,「我常常跟患者解釋,把攝護腺癌比喻成壞人,壞人本來需要吃飯才能夠做壞事。荷爾蒙治療就像是讓壞人沒飯吃,壞人就沒辦法做壞事。但是壞人也會漸漸進化,可能改吃別的東西,甚至不用吃東西也可以做壞事。」
攝護腺癌出現去勢抗性後,病情便會持續惡化,可能轉移至肺臟、肝臟等重要器官,而危及性命。裘坤元醫師說,因此若發現病情有變化,就須調整治療策略。
隨著精準醫療的發展,標靶治療已被運用於治療去勢抗性攝護腺癌。裘坤元醫師說,經過基因檢測,如果患者具有 BRCA 基因突變,可使用口服 PARP 抑制劑標靶藥物,而且能夠申請健保給付。
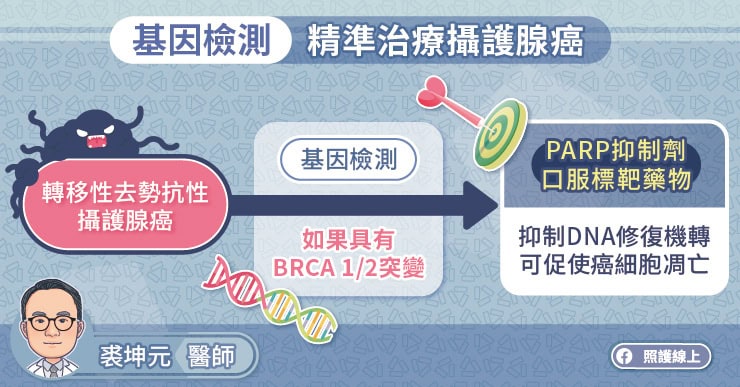
研究顯示,相較於沒有 BRCA 基因突變的患者,具有 BRCA 基因突變的患者,病程進展較快,且對傳統治療的反應較差,預後較差。利用 PARP 抑制劑標靶藥物,有助提升治療成效。
PARP 抑制劑標靶藥物能夠有效延緩疾病惡化,延長存活期。相較於化學治療,副作用較少,有助維持生活品質,且採用口服,便利性高,能夠提升患者的治療順從度。
「在過去,當患者進展為轉移性去勢抗性攝護腺癌的時候,平均存活期大概是 1 年左右。」裘坤元醫師說,「使用 PARP 抑制劑標靶藥物能夠顯著延長存活期,我們曾經有患者使用到 26 個月。」

接受 PARP 抑制劑標靶藥物治療後,患者可能有貧血的狀況,請務必按時回診追蹤檢查。
「對患者而言,PARP 抑制劑標靶藥物能通過健保給付,是令人振奮的好消息。」裘坤元醫師說,「轉移性去勢抗性攝護腺癌患者可考慮接受基因檢測,若具有 BRCA 基因突變,便可申請用藥。」
筆記重點整理
- 早期攝護腺癌沒有症狀,確定診斷時大多已經比較晚期。具有家族病史的男性,可以從 45 歲開始每年抽血檢測攝護腺特定抗原 PSA 指數,幫助早期發現攝護腺癌。
- 針對轉移性攝護腺癌必須使用全身性治療,首先是使用荷爾蒙治療,利用藥物讓男性荷爾蒙降到最低濃度,稱為去勢性治療。
- 荷爾蒙治療能夠有效抑制攝護腺癌生長,讓患者的病情得到控制,但是在經過 2 至 3 年的荷爾蒙治療後,攝護腺癌可能出現去勢抗性。
- 經過基因檢測,如果去勢抗性攝護腺癌患者具有 BRCA 基因突變,可使用 PARP 抑制劑標靶藥物,目前已能向健保申請給付。
- PARP 抑制劑標靶藥物能夠有效延緩疾病惡化,延長存活期。相較於化學治療,副作用較少,有助維持生活品質,且採用口服,便利性高,能夠提升患者的治療順從度。
- 本文轉載自 Care Online 照護線上《對付去勢抗性攝護腺癌,PARP 抑制劑標靶治療解析,泌尿專科醫師圖文懶人包》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接