- 作者/照護線上編輯部
- 本文轉載自 Care Online 照護線上《停經前轉移性荷爾蒙受體陽性、HER2陰性乳癌,CDK4/6抑制劑、抗荷爾蒙治療、停經針顯著延長存活期,專科醫師圖文解析》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接

「那是一位大學教授,發現乳癌後便接受手術,不過大約一年半後發現肝臟轉移。」新光醫院乳癌中心主任鄭翠芬醫師表示,「因為患者屬於停經前荷爾蒙受體陽性、HER2 陰性乳癌,所以便開始接受口服 CDK4/6 抑制劑標靶藥物、抗荷爾蒙治療與停經針。」
經過一年的治療後,患者肝臟的腫瘤幾乎完全消失。鄭翠芬醫師說,經過討論後,患者決定接受手術,切除部分肝臟。術後患者持續使用口服 CDK4/6 抑制劑,至今又過了 4 年,病情依然維持穩定,都沒有使用到化學治療。因為是口服藥,沒有明顯肝心毒性副作用,只有些許的白血球低下,可透過調整劑量而控制改善,所以患者的生活沒有受到影響,依然在大學裡教書、作研究。
「這在過去是難以想像的狀況,因為以前的乳癌患者若出現肝臟轉移,都必須接受化學治療,而存活期大概僅有一年。」鄭翠芬醫師說,「CDK4/6 抑制劑不僅大幅提升治療成效,也讓患者能夠維持生活品質。經常有患者出國旅遊,回診時還特地帶小禮物來跟我們分享。」
鄭翠芬醫師說,從今年開始,停經前轉移性荷爾蒙受體陽性、HER2 陰性乳癌患者也納入健保給付,相信能帶給年輕的乳癌患者非常大的幫助!
乳癌是台灣女性最好發的癌症,其中約有四成患者尚未停經。鄭翠芬醫師指出,確診乳癌後,會根據雌激素受體 ER、黃體激素受體 PR、人類表皮生長因子受體 HER2 等生物標記將乳癌分成幾種亞型,包括荷爾蒙受體陽性乳癌、HER2 陽性乳癌、三陰性乳癌等。
停經前乳癌患者以荷爾蒙受體陽性佔多數,而且癌細胞的惡性度較高,術後復發的風險也較高。鄭翠芬醫師說,由於停經前乳癌患者較年輕,在擬定治療計畫時,往往還會有生育、工作、家庭的考量。如果患者只有三十幾歲,可能要討論關於生育能力的保存。

治療停經前乳癌,一般需要讓患者進入停經的狀態,才能達到較好的治療效果。鄭翠芬醫師說,過去的作法是將卵巢切除,現在則可以用停經針,讓患者進入停經的狀態。在完成療程後,較年輕的患者還有機會恢復月經。
針對轉移性荷爾蒙受體陽性、HER2 陰性乳癌,以往只能使用化學治療,而在 CDK4/6 抑制劑標靶藥物問世後,治療成效大幅提升,是相當重要的治療工具。鄭翠芬醫師說,細胞週期素激酶 CDK(cyclin-dependent kinases)是調節細胞分裂週期的重要蛋白質,CDK4/6 抑制劑是一種細胞週期抑制劑,可以阻斷細胞分裂週期,進而抑制癌細胞的分裂複製,並延緩荷爾蒙抗藥性的出現。目前的國際治療指引建議使用 CDK4/6 抑制劑標靶藥物,搭配抗荷爾蒙治療與停經針。
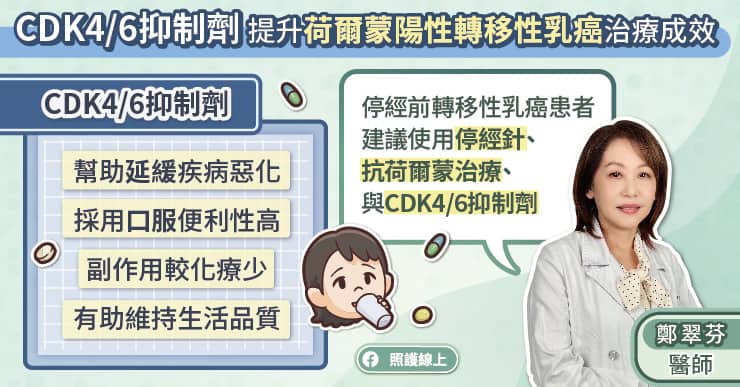
根據臨床試驗,停經前轉移性荷爾蒙受體陽性、HER2 陰性乳癌患者接受 CDK4/6 抑制劑標靶藥物,搭配抗荷爾蒙治療與停經針,能夠發揮顯著治療成效,延長存活時間。鄭翠芬醫師說,疾病無惡化存活期大概可達到 2 年以上,也有患者達到 3、4 年。
CDK4/6 抑制劑標靶藥物採用口服,便利性高,且副作用較化療少,有助維持生活品質。鄭翠芬醫師說,如今健保已將 CDK4/6 抑制劑標靶藥物、抗荷爾蒙治療與停經針納入給付,幫助停經前、停經後之轉移性荷爾蒙受體陽性乳癌患者降低經濟負擔。

停經前或正在停經乳癌婦女患者使用 CDK4/6 抑制劑,須與芳香環轉化酶抑制劑及停經針合併使用,並符合以下條件:
- 荷爾蒙接受體為:ER 或 PR>30%。
- HER-2 檢測為陰性。
- 經完整疾病評估後未出現器官轉移危急症狀(visceral crisis)且無中樞神經系統轉移。
- 骨轉移不可為唯一轉移部位。
「目前健保會給付 2 年 CDK4/6 抑制劑,在滿 2 年後,如果治療效果仍然不錯,可以考慮自費使用。」鄭翠芬醫師說,「有不少患者已經使用了 4、5 年 CDK4/6 抑制劑,病情都維持穩定,不用接受化學治療。」
貼心小提醒
乳癌早期沒有症狀,建議定期接受檢查,才能早期發現乳癌。鄭翠芬醫師叮嚀,隨著藥物的進步,乳癌的治療成效也持續提升,不但能夠顯著延長存活期,也可維持生活品質。確診乳癌後,務必和醫師配合,盡快接受治療!
- 本文轉載自 Care Online 照護線上《停經前轉移性荷爾蒙受體陽性、HER2陰性乳癌,CDK4/6抑制劑、抗荷爾蒙治療、停經針顯著延長存活期,專科醫師圖文解析》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接