• 作者/伊丹.班—巴拉克
• 譯者/傅賀
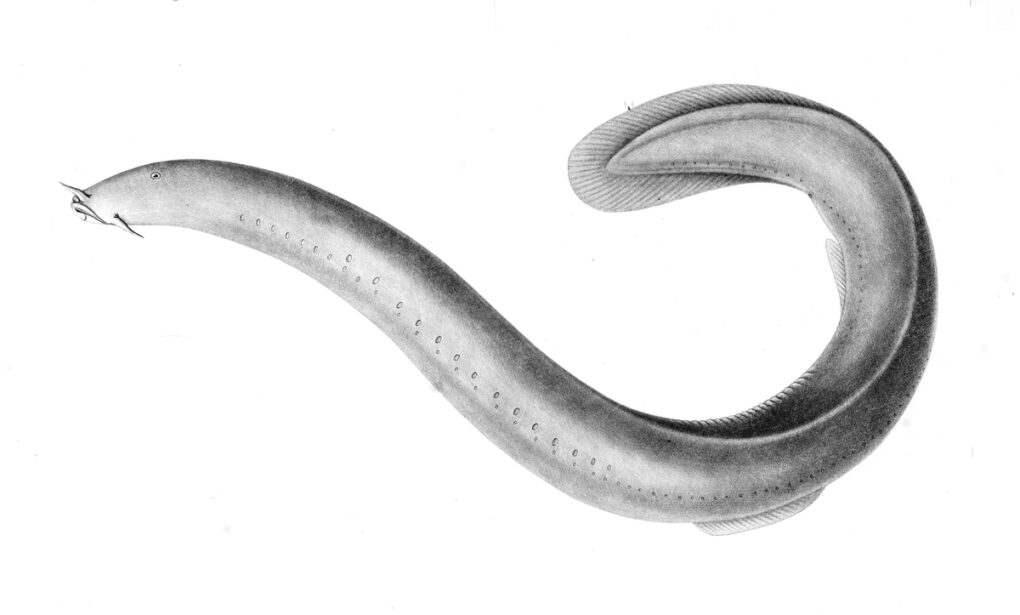
你可能聽過這個說法:鯊魚不會得癌症。事實上,牠們的免疫系統接近完美,牠們幾乎不會得任何疾病,牠們的免疫系統在過去幾億年裡都沒多大變化。是不是很神奇?
可惜,這都是無稽之談。沒錯,鯊魚的免疫系統非常驚人,全身分布有許多有趣而且有效的抗菌和抗病毒分子,牠們患癌症的概率也的確比人們通常預計的更低,但是鯊魚仍然會患上各種疾病,包括腫瘤。除此之外,數百萬隻鯊魚每年死於愚蠢。不是牠們自己的愚蠢(就智力而言,鯊魚還行),而是人類的愚蠢,特別是那些認為鯊魚軟骨產品可以「提高免疫力」、抗發炎甚至抗癌的江湖郎中。那種認為「鯊魚有完美的免疫系統」的觀念是由那些想透過賣軟骨藥而大賺一筆的藥商推動的,這背後的研究也不可靠。真正的科學研究已經揭穿了這些騙人的鬼把戲,但是依然有人在獵殺鯊魚,依然把它們的骨骼碾碎,當成「神奇的藥方」。
所謂「鯊魚的免疫系統從未改變過」的說法也經不起推敲。根據化石證據,我們的確發現今天的鯊魚跟牠們幾億年前的祖先「看起來 」 沒什麼差別,顯然,這讓一些人認為,鯊魚在其他方面也沒有任何變化。但這裡有一個重要區別:鯊魚的體型解決的是在水中穿行的問題;鯊魚的免疫系統解決的則是對抗病原體的問題。水沒有發生演化,但是病原體卻一直在演化。想必你明白我的意思了。
鯊魚有適應性免疫系統,也有完整可辨認的 T 細胞、B 細胞、抗體,以及各種其他組成。鯊魚跟人類的適應性免疫系統有許多差異,畢竟,我們分開的時間已經很久了。不過,牠們在許多基本的細節上跟我們類似,我們可以自信地說,某種類似的適應性免疫系統在四億年前(我們分開的時候)就已經出現並且發揮功能了。
牠們選擇留在水裡,發育出可以替換的鋒利牙齒,追逐魚類,而我們(更準確地說,是那些不再是硬骨魚的我們)則爬到岸上,失去了鰓,發育出了四肢,又過了許多年,我們回到海裡,拍攝了多部關於鯊魚及其鋒利牙齒的驚悚電影。儘管如此,我們的免疫系統提醒我們,在不同的外表之下,鯊魚和我們其實是失散多年的兄弟。
但是,讓我們沿著演化史再往回走一步,來到所有的脊椎動物分成兩類—有頜與無頜脊椎動物—的時間點。你也許沒聽說過還有無頜脊椎動物;老實說,這一類生物後來活得不太好,只有兩個科的動物避免了滅絕的厄運,活到了今天:七鰓鰻和盲鰻。這兩種動物長得都比較搞笑,牠們看起來像是努力要長成魚,但是好像不太合格,直到最近,人們一直都認為牠們並沒有適應性免疫系統。
也許牠們不需要:第一批有頜脊椎動物可能是掠食者,而掠食者往往會活得更久,後代更少,而且一般更注重質而不是量。同樣可以推斷,牠們在演化過程中對感染的抵抗力更強。鯊魚、人類、其他魚類以及所有有頜脊椎動物都有一個胸腺和脾臟,而且在各個物種裡無論是形狀還是功能看起來都比較類似,但是七鰓鰻和盲鰻就沒有。研究人員仔細檢查了無頜脊椎動物的基因組,發現牠們也沒有 T 細胞、B 細胞或者抗原受體的重組基因。但是問題在於,牠們實際上是有適應性免疫系統的—只是跟我們的不一樣而已。
這一點其實意義重大。我們以為我們的適應性免疫系統相當特殊,但是我們現在看到,適應性免疫系統在脊椎動物中似乎出現了兩次,而且是獨立演化出來的。
這也許是一種經典的趨同演化(convergent evolution):正如鳥類和蝙蝠各自以不同的方式演化出了翅膀,無頜脊椎動物使用一種和我們一樣的隨機重排機制,來增加抗原受體基因的多樣性,但是牠們使用的是跟我們這些有頜脊椎動物完全不同的一套基因,這種重排機制使用的是不同的酶,做著完全不同的事情。同樣地,牠們的淋巴球類型跟我們的也不一樣。不過,牠們的免疫系統看起來跟我們的一樣有效。

——本文摘自《我們為什麼還沒有死掉?》,2020 年 9 月,麥田出版。