- 作者/照護線上編輯部
- 本文轉載自 Care Online 照護線上《突破小細胞肺癌治療困境!免疫治療納入健保給付,顯著提升治療成效,胸腔專科醫師圖文懶人包》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接

「免疫治療讓小細胞肺癌的治療成效顯著提升,對擴散期小細胞肺癌而言,是相當重要的突破!」彰化基督教醫院胸腔內科主任林聖皓醫師表示,「由於擴散期小細胞肺癌的治療選項十分有限,若符合健保給付條件,建議在接受化學治療時合併 PD-L1 免疫療法,以爭取較好的治療成效。」
肺癌主要可區分成小細胞肺癌與非小細胞肺癌兩大類,根據 111 年癌症登記報告,小細胞肺癌(SCLC)的新診斷人數約為 1200 人,佔所有肺癌患者比例約 6.5%。彰化基督教醫院胸腔內科林俊維醫師分析,小細胞肺癌主要發生於 55 至 75 歲之間,以男性吸菸者為主,男女性比例約為 10: 1。林俊維醫師說,小細胞肺癌與吸菸密切相關,常發生在肺部中央區域,可能出現慢性咳嗽、痰中帶血、聲音沙啞、呼吸急促、胸痛、背痛、骨頭疼痛、體重減輕等症狀。
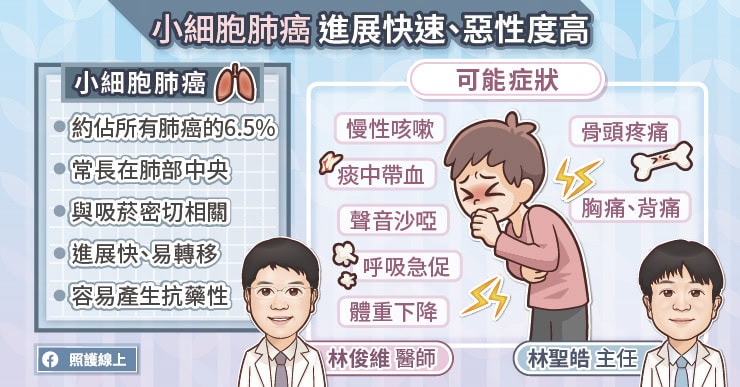
圖 / 照護線上
小細胞肺癌惡性高 生長迅速對化療易產生抗藥性 免疫治療問世打破困境
小細胞肺癌的惡性度高,癌細胞增殖速度快、進展迅速,容易出現遠端轉移。林俊維醫師說,九成以上的小細胞肺癌患者在確診時已無法開刀,只有少數小細胞肺癌患者能夠接受手術治療。針對小細胞肺癌的全身性治療以化學治療為主,再輔以放射治療。
林俊維醫師說,大約七成的病人在接受化療之後,一開始會有不錯的效果,病情會有明顯改善,不過麻煩的是大多數患者在經過幾個月之後,就會出現病情惡化的情況。當疾病進展時,代表癌細胞已對第一線化療出現抗藥性,雖然可以改用第二線化學治療,但相較於第一線化療,腫瘤對第二線化學治療的反應率會明顯下降,腫瘤受抑制的時間更短,擴散期的患者的存活期常不到一年。
隨著免疫治療的出現,終於讓小細胞肺癌的治療困境獲得顯著提升。免疫治療是藉由『喚醒』患者自身免疫系統來對抗癌細胞,林聖皓主任解釋,我們的免疫細胞原本具有辨識並清除癌細胞的能力,但是癌細胞可能利用『偽裝』來逃避免疫細胞的攻擊,也就是癌細胞利用表面的 PD-L1 與免疫細胞的 PD-1 結合,一旦兩者結合就會抑制免疫細胞的攻擊功能,使得癌細胞肆無忌憚地的生長及擴散。
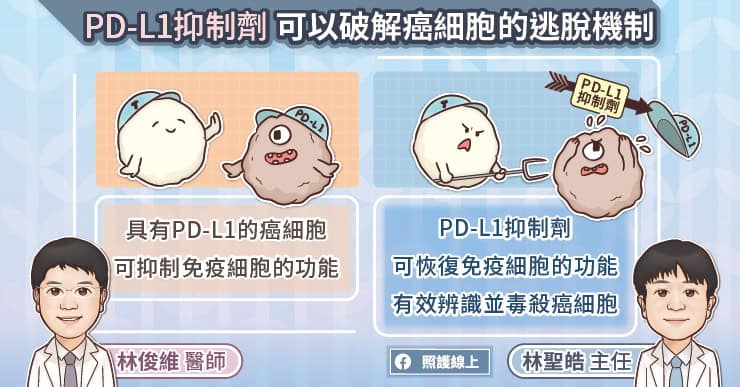
圖 / 照護線上
PD-L1 抑制劑破除癌細胞偽裝!健保給付後擴散期第一線優先考慮免疫合併化療
運用在小細胞肺癌的免疫治療–『PD-L1 抑制劑』則能夠阻止癌細胞的 PD-L1 與免疫細胞的 PD-1 結合,進而解除癌細胞對免疫細胞的抑制作用,讓免疫系統恢復正常,可以有效地辨識並毒殺癌細胞。研究證實,PD-L1 抑制劑合併化療作為擴散期小細胞肺癌的第一線治療,可顯著延緩疾病惡化時間,降低 30% 的死亡風險,具有顯著存活效益。林聖皓主任說,後續的研究亦顯示,相較於單用傳統化療,加入 PD-L1 抑制劑後可以讓五年存活率提升,且實驗中沒有觀察到特殊之不良反應發生,進一步確認了免疫治療組合之生存效益,以及用藥之安全性。
PD-L1 抑制劑合併化學治療被視為小細胞肺癌治療近二十年來重要的進展,已被國際治療指引列入擴散期小細胞肺癌的一線治療推薦,健保亦已納入給付。
此外一般來說,PD-L1 抑制劑在治療擴散期小細胞肺癌時,前4個療程合併化療後,接續僅需使用單方 PD-L1 抑制劑作為維持治療。此款 PD-L1 抑制劑目前也已研發出新的皮下注射劑型,可將給藥時間大幅縮短,跟原本靜脈滴注需耗時約 60 分鐘左右相比,改採皮下注射僅需 10 分鐘即可完成,於無須合併化療單方使用時,可帶來大幅縮減留院時間,以及無須裝設人工血管之優點。台灣目前也已引進此款新的皮下注射給藥 PD-L1 抑制劑,不過皮下注射給藥需自費,患者可視需求與醫師詢問。
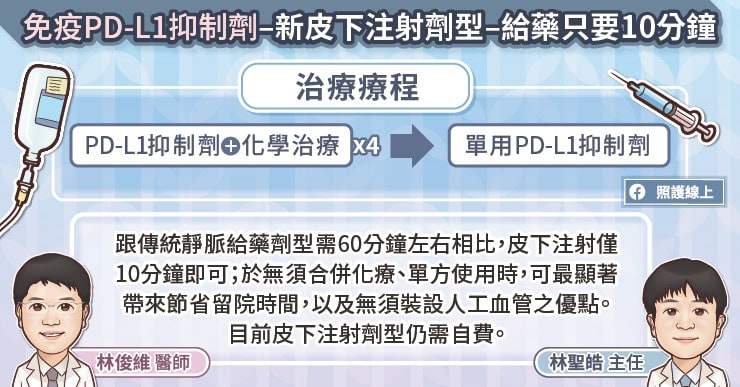
圖 / 照護線上
林聖皓醫師最後也提醒,患者雖普遍對於免疫治療耐受性高,但仍須定期回診,接受影像檢查與血液檢測,以及時評估治療反應,並適時調整治療計畫。若出現皮膚反應、疲倦、腸胃不適、自體免疫相關併發症等症狀,請務必告知醫療團隊,才能適時處理,獲得最佳治療預後。
小細胞肺癌&免疫治療筆記重點整理
此款 PD-L1 抑制劑目前也已研發出新的皮下注射劑型,可將給藥時間大幅縮短,跟原本靜脈滴注需耗時約 60 分鐘左右相比,改採皮下注射僅需 10 分鐘即可完成,可帶來大幅縮減留院時間。
小細胞肺癌主要發生於 55 至 75 歲之間,以男性吸菸者為主,男女性比例約為 10 比 1。小細胞肺癌與吸菸密切相關,常長在肺部中央區域,可能出現慢性咳嗽、痰中帶血、聲音沙啞、呼吸急促、胸痛、背痛、骨頭疼痛、體重減輕等症狀。
針對小細胞肺癌的全身性治療傳統以化學治療為主,可搭配放射治療,約七成的病人在接受化療之後,腫瘤都會有明顯的改善,但大多數患者在經過幾個月之後,就會出現疾病惡化的情況。
小細胞肺癌的治療成效隨著免疫治療的問世獲得顯著提升。免疫治療是藉『喚醒』患者自身免疫系統來對抗癌細胞,『PD-L1 抑制劑』則能夠阻止癌細胞的 PD-L1 與免疫細胞的 PD-1 結合,進而解除癌細胞對免疫細胞的抑制作用,讓免疫系統恢復正常,可以有效地辨識並毒殺癌細胞。
研究證實,PD-L1 抑制劑合併化療作為擴散期小細胞肺癌的第一線治療,可顯著延緩疾病惡化時間,降低 30% 的死亡風險,具有顯著存活效益。林聖皓主任說,後續的研究亦顯示,相較於單用傳統化療,加入 PD-L1 抑制劑後可以讓五年存活率提升,且實驗中沒有觀察到特殊之不良反應發生。
PD-L1 抑制劑合併化學治療被視為小細胞肺癌治療近二十年來重要的進展,已被國際治療指引列入擴散期小細胞肺癌的一線治療推薦,健保亦已納入給付。
- 本文轉載自 Care Online 照護線上《突破小細胞肺癌治療困境!免疫治療納入健保給付,顯著提升治療成效,胸腔專科醫師圖文懶人包》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接