本文轉載自中央研究院研之有物,泛科學為宣傳推廣執行單位
- 採訪編輯|林承勳、美術編輯|林洵安
免疫系統的過度反應
人體依賴免疫系統對抗病毒,但免疫反應如果過激,反而造成器官損傷或衰竭,直接導致患者死亡。中研院基因體研究中心謝世良特聘研究員長期研究發現,登革病毒會刺激血小板產生胞外囊泡和微泡,進而攻擊白血球,導致發炎病症。研究團隊據此研發抗體,減緩發炎反應,已成功將感染登革病毒的小鼠存活率提升至 90% ,並於 2019 年 6 月刊登於《自然通訊》 (Nature Communications) 。面對新冠病毒等新興傳染病,此種「減緩發炎」為主的創新療法,將有機會大幅降低患者死亡率。
為了維護人體的穩定與和平,免疫系統一旦偵測到外來入侵物,即啟動發炎反應,召喚免疫細胞圍剿入侵者。但發炎反應如果過度,往往會對自身臟器造成嚴重傷害。以登革熱 (dengue fever) 為例,免疫過激會造成「出血性登革熱」,嚴重將造成休克;最近新冠肺炎造成的肺纖維化,也是免疫過激的結果。
若想找出更有效的抗病毒治療策略,必須深入了解病毒與免疫系統的互動機制。
免疫反應宛如雙面刃
當病毒侵入人體,體內免疫細胞會立刻發動攻擊,如本文主角—-巨噬細胞 (macrophage) 與嗜中性白血球 (neutrophil) 兩種白血球。
嗜中性白血球,會吞吃入侵者,如果敵人太多,甚至會「自爆」釋放出自己的網狀遺傳物質 (deoxyribonucleic Acid, DNA) 黏住細菌,再由附著在 DNA 的酶將其殺死、清除,這個過程稱作嗜中性白血球胞外捕捉 (neutrophil extracellular traps, NETs) 。
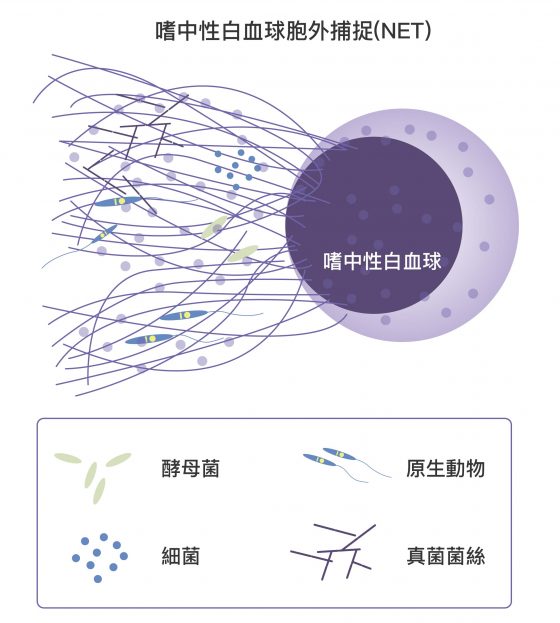
資料來源│NETosis : A Microbicidal Mechanism beyond Cell Death
圖說重製│林任遠、張語辰
巨噬細胞,也會吞噬、分解大量的病原體與受感染細胞。當病原體與細胞表面的受體結合,才能進入巨噬細胞,然後病原體會被分解成碎片排出。這些碎片會被當作抗原,活化其他種類的白血球。另外,巨噬細胞和受感染的細胞還會分泌細胞激素 (cytokine) 引起發炎反應,進一步對抗病毒。
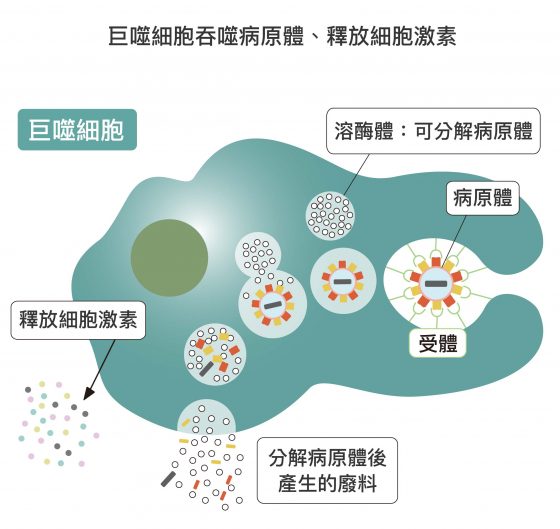
圖說設計│黃曉君、林洵安
細胞激素包括干擾素 (interferon) 、促發炎激素 (proinflammatory cytokine) 、趨化激素 (chemokine) 等等。干擾素,由受傷的細胞產生,用以警告鄰近健康的細胞,趕緊製造可阻止病毒複製的蛋白質,抑制病毒數量。促發炎激素,會增加血管通透性,讓血液中的白血球能輕易通過血管壁趕往目的地。趨化激素,會吸引更多白血球,召來更多援軍。
問題來了!受感染細胞或巨噬細胞分泌細胞激素,或是嗜中性白血球胞外捕捉,本來都是為了擊退病原體。但令人遺憾的是,發炎的副作用與白血球無差別攻擊,有時反而造成器官受損或衰竭,甚至導致患者死亡。
那麼,有沒有一種治療方法,可以抑制過度發炎反應,但又不影響免疫系統消滅病原體?早在 2003 年,謝世良即開始這項大哉問。
創新構想:抑制發炎反應,但不影響免疫力
2003 年, SARS (Severe Acute Respiratory Syndrome) 疫情爆發,其中重症患者出現肺積水、呼吸困難等症狀,均非肇因於病毒本身,而是免疫過度反應的結果。
當肺部細胞受感染出現發炎反應,促發炎激素讓血管通透性增加、血漿滲入組織中,即會造成肺積水。再加上,蜂擁而來的白血球無差別攻擊受感染或健康肺泡,甚至分泌激素呼喚更多白血球前來,惡性循環之下形成細胞激素風暴 (cytokine storm) ,讓肺泡細胞受到嚴重損害,導致病人呼吸困難、險象環生。
然而, SARS 冠狀病毒 (SARS-CoV) 從始至終沒有特效藥、疫苗,只能將重症患者安置在負壓隔離加護病房,施以「支持性療法」,期盼患者能在良好的照護下,熬過自身的細胞激素風暴,等待自己的免疫系統清除病毒。
當時醫學背景出身的謝世良,從深厚的臨床與研究經驗出發,提出創新治療觀念:
設法研發一種藥物,可減緩細胞激素風暴,將發炎反應控制在不致命的程度,又不干擾免疫系統清除病毒,將有效降低感染者的死亡率。
「現有的類固醇消炎效果很好,但有抗藥性的問題,而且完全抑制發炎、沒有細胞激素也不行,因為病原體還是需要免疫細胞來對付。」謝世良進一步分析,細胞分泌的激素裡,促發炎激素跟趨化激素是造成細胞激素風暴的主因;但干擾素不引起發炎只抑制病毒複製。因此具體任務是:如何在抑制促發炎激素及趨化激素的同時,不會影響干擾素分泌,以避免削弱患者抵抗力。
登革熱出血熱,也源自細胞激素風暴
正當謝世良著手開始研究時, SARS 疫情宣告結束,於是他將戰力火速轉移到也會讓免疫系統過度活化的登革病毒 (dengue virus) 。
圖片來源│iStock
登革病毒分四種血清型別,患者感染過某一血清型的病毒,雖然能對這型病毒終身免疫,對於其他型卻只有短暫免疫力。時間一過,抗體甚至會結合成「病毒-抗體免疫複合體」 (virus-antibody immune complexes) ,讓病毒更容易結合巨噬細胞表面的受體 (receptor) ,進入細胞內部。
這種抗體反過來協助病毒入侵的現象,稱作抗體依賴性增強反應 (Antibody dependent enhancement, ADE) ,正是登革熱疫苗研發困難的原因。因為,若是無法同時刺激人體產生對抗四型病毒的抗體,病毒跑到巨噬細胞內增值擴散,其他巨噬細胞又分泌更多細胞激素,循環之下引發細胞激素風暴,將導致高致死率的登革出血熱或休克症候群。
痊癒者體內的單一血清型登革病毒抗體,反倒會接應其他血清型病毒,引發細胞激素風暴。
細胞激素風暴的關鍵受體:CLEC5A (2008)
那麼,如何減緩登革病毒引起的細胞激素風暴?謝世良的第一步是:尋找病毒是與巨噬細胞表面哪種受體結合,導致細胞激素風暴。在他著手研究後,注意到一種受體: C 型凝集素 5A (C-type lectin member 5A, CLEC5A) 。
「CLEC5A 在生化實驗中已證明具有傳遞訊息的功能。因此我推測, CLEC5A 很可能跟後續細胞激素分泌有關。」謝世良解釋。
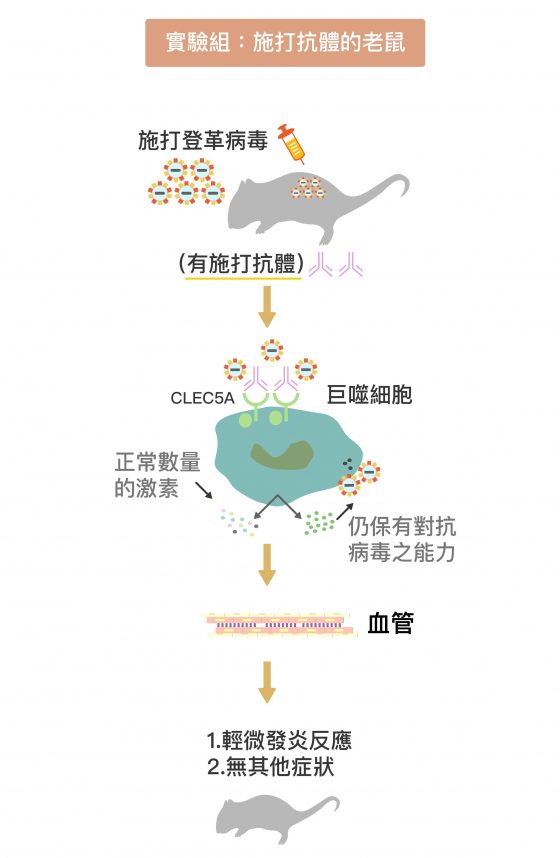
第二步,備製 CLEC5A 的拮抗性單株抗體 (antagonistic anti-CLEC5A monoclonal antibody) ,打在小鼠身上,讓這些抗體搶先佔據巨噬細胞的 CLEC5 受體位置,阻斷登革病毒感染細胞的路徑。
結果發現,沒有打入這種抗體的對照組小鼠,登革病毒果真引起細胞激素風暴,在發炎、血管通透性增加的情況下,出現嚴重的皮下、腸道出血症狀而死亡。實驗組的小鼠在注射抗體後,發炎反應比較緩和,出血症狀明顯受到抑制。更重要的是,小鼠體內干擾素的分泌正常運作,不受抗體影響。
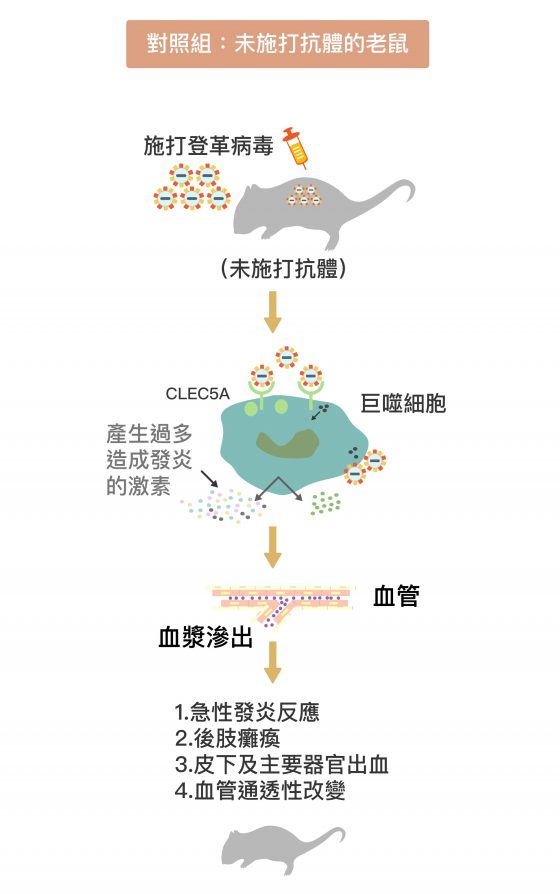
資料來源│謝世良
圖說重製│林任遠、張語辰
資料來源│謝世良
圖說重製│林任遠、張語辰
CLEC5A 拮抗性單株抗體,成功減緩小鼠登革出血熱症狀,又不影響干擾素分泌。
謝世良團隊研發的 CLEC5A 拮抗性抗體,將染病小鼠存活率一舉提高到五成,效果比其他免疫治療用的抗體顯著得多。2008 年,這項研究因著揭開 CLEC5A 是登革病毒引發細胞激素風暴的關鍵,以及成功製造出有效抗體等重大貢獻,登上科學期刊《自然》 (Nature) ,並獲多國新聞媒體報導。
其後,謝世良又發現這個機制普遍存在病毒引發人體的發炎反應中,面對日本腦炎、 H1N1 、 H5N1 等流行性感冒病毒, CLEC5A 拮抗性單株抗體均能成功提升小鼠的存活率。 2017 年,他將研究觸角擴及 CLEC5A 在對抗細菌的角色,發現受體 CLEC5A 是比過去研究焦點「類鐸受體 (Toll-like receptor 2- TLR2) 」更重要的防衛因子,論文也登上《自然通訊》 ( Nature Communications) 期刊。
登革病毒侵略人體的關鍵細胞:血小板 (2019)
雖然 2008 年的研究中,小鼠的登革出血熱已獲得緩和,但五成的存活率彷彿是謝世良難以突破的魔咒,讓他強烈懷疑還有其他免疫細胞或受體參與其中。
歷經十餘年的研究, 2019 年,謝世良與陽明大學臨床醫學所博士生宋佩珊終於解開謎底:登革病毒進入人體後,會去激活血小板表面的受體 C 型凝集素 2 (C-type lectin member 2, CLEC2) ,促使血小板分泌胞外囊泡 (extracellular vesicles) :直徑小於一兩百奈米的胞外體 (exosomes) ,以及較大、直徑數百到一千 奈米的微泡 (microvesicles) 。
其後,這些胞外囊泡分別會再跟巨噬細胞、嗜中性白血球表面的 CLEC5A 與 TLR2 結合。結合後才是災難的開始!巨噬細胞會大量分泌細胞激素,引起細胞激素風暴;嗜中性白血球則會出現胞外捕捉,釋放出酶跟顆粒,損害周圍細胞。
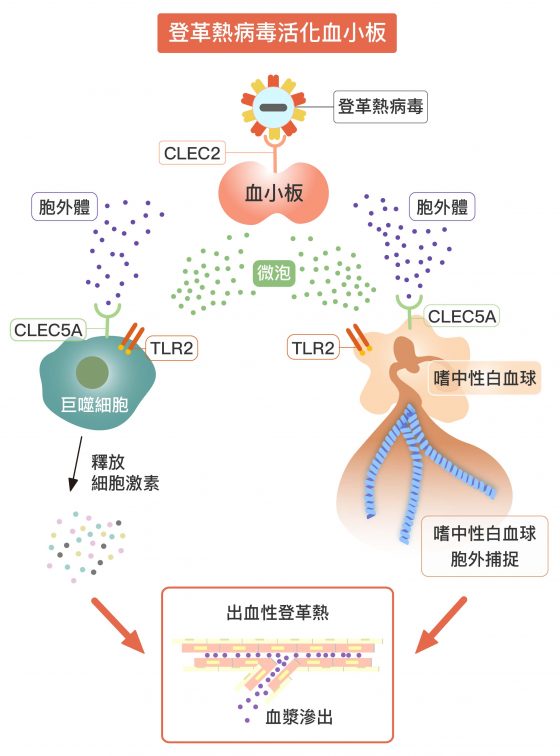
圖說原作│宋佩珊
圖說重製│林洵安
找到機制後,怎麼阻斷呢?謝世良團隊利用 CLEC5A 基因剔除鼠施打抗 TLR2 抗體,同時阻斷體外囊泡與 CLEC5A 以及 TLR2 受體結合,成功壓制登革病毒引起的免疫過激症狀,小鼠存活率也從 50% 奇蹟似的提升至 90% 。本次研究不但揭發登革病毒完整入侵途徑,並成功找出治療方法的研究成果,在 2019 年再度登上《自然通訊》 (Nature Communications) 期刊。第一作者宋珮珊博士生的研究論文獲得相當高的引用, 2020 年《免疫學趨勢》 (Trends in Immunology) 並以專文推薦這項研究揭開「嗜中性白血球的胞外捕捉乃登革熱感染機制的關鍵」,在在顯示此項成果具有突破性的意義。
目前謝世良團隊正積極發展針對 CLEC5A 以及 TLR2 的雙特異性抗體 (CLEC5A/TLR2 Bispecific antibody) ,可望於近期驗證阻斷 CLEC5A 及 TLR2 受體之效果。
同時阻斷 CLEC5 與 TLR2 兩個受體,可以有效壓抑病毒引起的過度免疫反應。
新冠病毒來襲,減緩發炎或可扭轉戰局
未來謝世良計畫將 CLEC5A/TLR2 雙特異性抗體,擴及其他病毒感染引起之急性發炎,以及自體免疫疾病,像是紅斑性狼瘡或類風溼性關節炎。如今新型冠狀病毒疫情 (COVID-19) 來襲,除了抗病毒藥物、疫苗,此種減緩發炎反應的治療,可能是更及時的救命解方。
目前,謝世量實驗室已將過去十餘年研究建立的平台,包括基因工程製造的巨噬細胞表面受體、細胞融合瘤技術生產的 CLEC5A 的拮抗性單株抗體、基因抑制小鼠等等,全力轉向 COVID-19 的研究。
謝世良指出,病毒基因瞬息萬變,可能很快就會產生抗藥性;但找出共同的致病機制就不一樣了。雖然不同種類的病毒侵入細胞的途徑不盡相同,但觸發免疫細胞的訊息傳遞路程卻大致相同。因此,找出抗體以阻斷病毒與免疫細胞結合,雖然比較耗時耗力,卻有機會一勞永逸,對抗不斷推陳出新的病毒。
對前線的醫護來說,當務之急絕對是趕緊找到能抑制病毒的特效藥;研究人員的功課,則是想辦法揭開致病原理,找到一勞永逸的解方。
一場演講邀約,催生驚人研究成果
謝世良十餘年的研究成果,源自於十七年前的一場演講邀請。
當時, SARS 疫情延燒,時任衛生署疾病管制局長的蘇益仁,致電邀請謝世良為民眾帶來一場演講,解說病毒如何引起人體的細胞激素風暴。原本只是為演講做準備的謝世良,找資料時意外發現:當時科學界對細胞激素了解甚少,反倒讓自己一頭栽入此未知領域。「一通偶然的電話,一個『錯誤』的決定,促成今天的成果。」謝世良打趣地說。
但從一個新穎的構想到具體的成果,箇中辛苦不足為外人道。謝世良表示:「一個概念只用一句話或半分鐘講完,卻要花上幾年的時間來完成。」基因工程製造巨噬細胞表面受體、細胞融合瘤技術生產 CLEC5A 的拮抗性單株抗體,皆動輒耗時數年、耗費百萬。
另外,實驗中不可或缺的 STAT1 與 CLEC2 基因抑制小鼠,必須從英國進口胚胎,研究員充當奶爸照顧幼鼠,長大後再讓小鼠交配,才能在實驗中使用,光是備至小鼠就要近一年的時間。謝世良苦笑地提到:「英國不給成鼠只賣胚胎,但胚胎必須低溫運送,第一批因為器材漏氣死亡;第二批在機場差點被海關打開檢查,險些因溫度上升導致胚胎受損,還好有貴人幫忙度過危機。」
因想法創新,實驗器材必須自己想辦法,研究路也走得格外辛苦;但也因為走在最前端,才能有驚人發現。
要當第一,去做從來沒有人嘗試過的事,這的確很累人,但流淚灑種才能歡呼收割。

圖片來源│謝世良
延伸閱讀
- 謝世良的個人網頁
- 中研院107年2月份知識饗宴「細胞激素風暴:失控的免疫反應」
- CLEC5A 是嗜中性白血球對抗細菌的關鍵
- Chen ST, Chen JW, Wu WC, Chou TY, Yang CY, Hsieh SL*, 2017, “CLEC5A is a critical receptor in innate immunity against Listeria infection”, NATURE COMMUNICATIONS, 8(1):299.
- Teng, O, Chen, ST, Hsu TL, Sia SF, Cole S, Valkenburg SA, Hsu TY, Zheng JT, Tu W, Bruzzone R, Peiris JSM, Hsieh SL*, Yen HL*, 2017, “CLEC5A-mediated enhancement of the inflammatory response in myeloid cells contributes to influenza pathogenicity in vivo.”, JOURNAL OF VIROLOGY, 91, e01813.
- Wu MF, Chen ST, Yang AH, Lin WW, Lin YL, Chen NJ, Tsai IS, Li L, Hsieh SL*, 2013, “CLEC5A is critical for dengue virus-induced inflammasome activation in human macrophages”, BLOOD, 121(1), 95-106.
- Chen ST, Liu RS, Wu MF, Lin YL, Chen SY, Tan DT, Chou TY, Tsai IS, Li L, Hsieh SL*, 2012, “CLEC5A regulates Japanese encephalitis virus-induced neuroinflammation and lethality.”, PLoS Pathogens, 8(4), e1002655.
- Chen ST, Lin YL, Huang MT, Wu MF, Cheng SC, Lei HY, Lee CK, Chiou TW, Wong CH, Hsieh SL*. CLEC5A is critical for dengue virus-induced lethal disease. Nature 2008; 453: 672-5.
- Sung PS, Hsieh SL*. CLEC2 and CLEC5A: pathogenic host factor during acute viral infections. Front. Immunol., 06 December 2019
- Sung PS, Huang DF, Hsieh SL*. Extracellular vesicles from CLEC2-activated platelets enhance dengue virus-induced lethality via CLEC5A/TLR2. Nature Communications 2019, DOI:10.
1038/s41467-019-10360-4.
- 本文轉載自中央研究院研之有物,原文為《對抗病毒另闢蹊徑!免疫過激傷敵三千、自損一萬,減緩發炎或可扭轉戰情》,泛科學為宣傳推廣執行單位
編按:CLEC2 基因抑制小鼠誤植為 CLEC5A,2020/5/19 勘誤修改。