2014年諾貝爾物理學獎頒給了藍光LED的發明,但是其他顏色LED卻沒有獲得諾貝爾獎的肯定。
你會不會覺得很奇怪?筆者曾聽過物理天龍人說 (註:指的是從大學到博士都唸物理系,後來變物理系教授的血統純正物理人),諾貝爾獎應該頒給創新並被實驗證實的概念:但是LED這個概念不但幾十年前就有,之後也還有紅光的LED產品;藍光LED不但不創新,產品推出也較慢,為什麼可以獲獎?

發光二極體(light emitting diode,縮寫為LED),是由半導體所做成的發光元件。藍光
但問題就在於,生活中很少把紅光拿來照明。我們喜歡用白光當作照明的光源,而白光可以由藍光、綠光、紅光三原色組成。難道就只是藍光LED是最後做出來的,因為終於可以混色成白光所以割稻尾,案情有這麼單純嗎?

藍光,不只是三原色之一
你或許會猜得到,當藍光、綠光、紅光LED都有時,
其實,假如現在只有藍光的LED發明出來,科學家還是可以製造白光的。
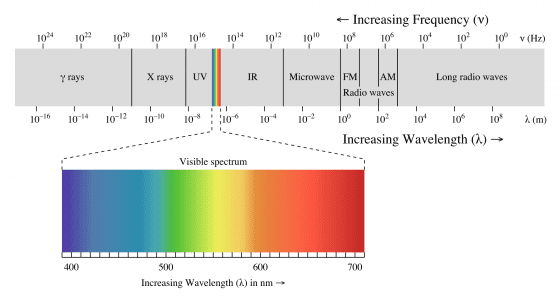
了解這件事,我們首先要有一個關於光的科學概念:二十世紀初光電效應及黑體輻射實驗中,科學家發現光的量子能量跟光強度沒有關係,只跟光的頻率(frequency)成正比而已。光是電磁波一種,在可見光中「紅橙黃綠藍靛紫」的彩虹排列中,頻率愈高,表示光能量也愈高。所以三原色中的藍、綠、紅三種顏色,藍色的能量是最高的。
藍光能量最高又怎樣?答案是它容易在發光材料裡產生低能量的綠光或紅光。當電子在發光材料裡面受到高能量的光由基態(ground state)激發到激發態(excited state)時,電子會在材料裡撞到其他電子或原子而損失能量。最後當較低能量的電子回到基態時,放出較低能量的光。所以科學家可以很容易的找到材料,受藍光激發後,會放出綠光或紅光。
目前市面上的白光LED燈泡,其實沒有用到紅光LED,
科學走入民間,需要有工程的思維
要讓技術變成商品走入人們的生活裡,就不能只有科學的思維。兩個同樣好的產品,價錢差別也不大的話,人們習慣了一個產品後,為什麼要換另一個產品?所以LED燈泡一定要比我們常使用的白熾燈泡、省電燈泡優越,才會有市場。雖然LED燈泡還有繼續改良進步的空間,但諾貝爾物理獎的委員們,已經看到了未來照明市場慢慢會被LED燈泡所取代了!
| 白熾燈泡 | 省電燈泡 | LED (Cree) | LED (飛利浦) | LEDNovation | |
| 售價 | US$ 0.41 | US$ 0.99 | US$ 9.97 | US$ 4.35 | US$ 31.50 |
| 瓦數 | 60 | 14 | 9.5 | 8.5 | 9.4 |
| 發光效率 | 14.3流明/瓦 | 55.4流明/瓦 | 84流明/瓦 | 94.1流明/瓦 | 86.2流明/瓦 |
| 壽命 (六小時/天) |
0.46年 | 4.6年 | 11.4年 | 4.6年 | 22.8年 |
| 20年電成本 | US$ 342 | US$ 80 | US$ 54 | US$ 48 | US$ 54 |
| 總成本 | US$ 360 | US$ 93 | US$ 77 | US$ 73 | US$ 86 |
來源:維基百科
在LED燈泡還沒問世之前,我們都知道省電就要用省電燈泡,所以省電燈泡是LED燈泡市場上很強勁的對手。由上表來看,要達到差不多亮度所需的電,白熾燈泡是60瓦,但LED燈泡9瓦左右與省電燈泡14瓦比起來,LED燈泡雖然有比較省,但是售價卻差好幾倍。雖然電費比較省,但是精打細算的人們,就會考慮買貴的東西是不是能用的比較久,讓省下的電費彌補買貴的價差,才符合總經濟效益。所以我們看一下每天6小時,20年總成本的比較,LED還是比省電燈泡省一些,所以才會有市場。

從上面的表,你還會發現一件有趣的事,三家LED燈泡公司有不同的策略,其實LED的壽命要超過20年技術上是沒什麼問題的,只是製造成本很高而已。壽命長的LED燈也許可以用在車燈或是戶外照明,但飛利浦公司想要主打家用市場,用了比較差但是成本低的技術,結果使用壽命與省電燈泡差不多,但大幅降低了售價,增加人們購買的意願。
你想想,家裡的燈泡是不是每天只有晚上開著,用4年跟用20年換一次燈泡你的感覺有很強的不同嗎?但是售價差7倍是不是就影響你的購買選擇了!所以科學技術與人類購買思維是很不同的,很多時候最好的產品並不會賣的最好,廠商有時候不是不會做好產品,只是為了降低成本影響人們購買選擇,另一方面產品早點壞,讓消費者再買反而賺更多!
哎呀好像扯遠了,講到這,你是不是有被說服藍光LED真的比其他顏色重要?雖然物理天龍人認為藍光LED是「工程」貢獻不是「物理」貢獻。可是諾貝爾沒有「工程」獎啊!所以筆者認為它獲諾貝爾物理獎是實至名歸,對人類的生活影響層面很廣。我們期待技術的發展,能進一步再提升LED燈泡的用電效率與製造成本,節能減碳對地球友善些!
延伸閱讀:
- 科學月刊2014年12月號,<藍光LED掀起照明的新頁>。
- 物理雙月刊2015年2月號,物理諾貝爾獎專題報導。







































