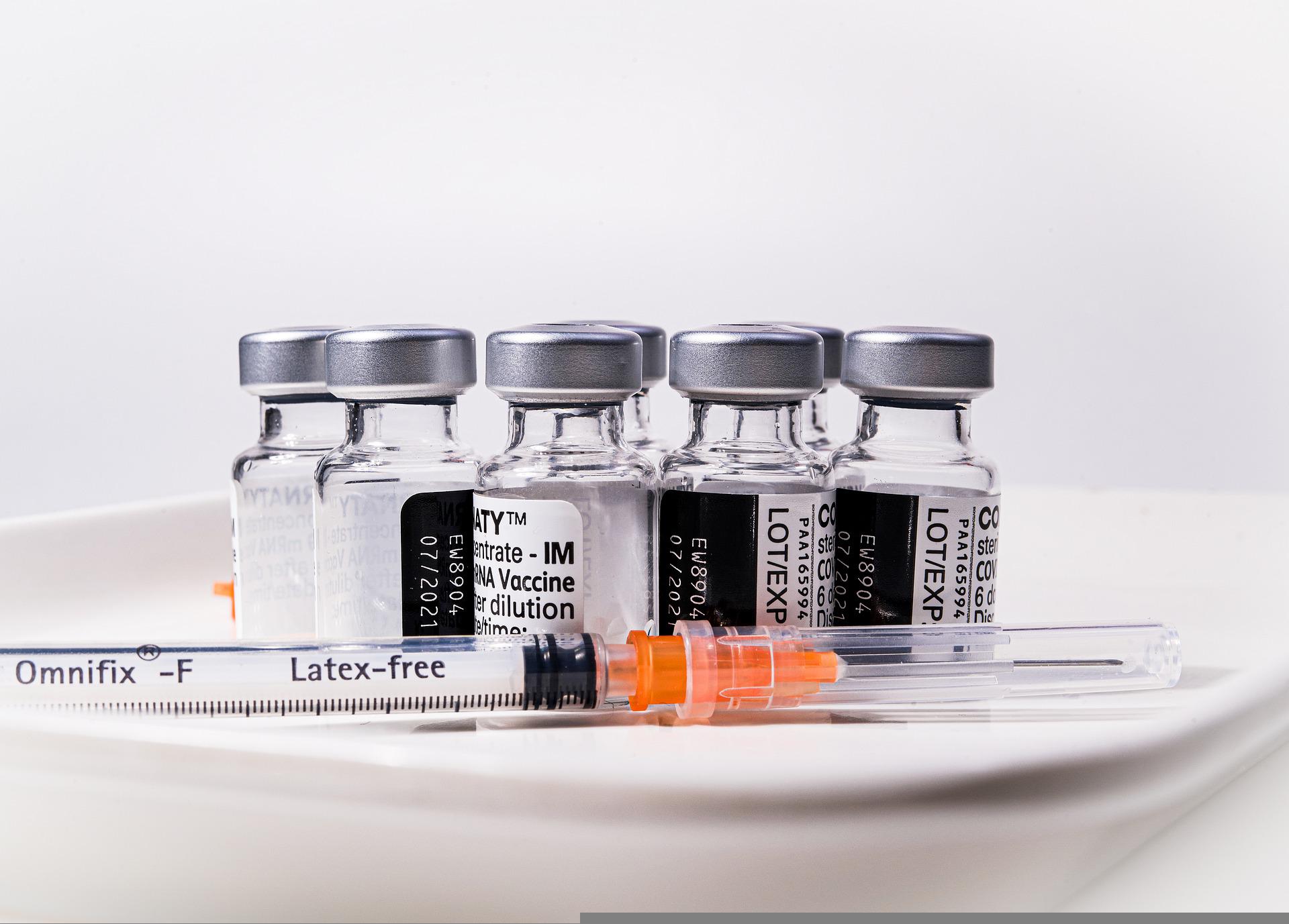
- 作者:蔡依橙

對於BNT 疫苗態度的兩極化
Pfizer / BioNTech 疫苗,在臺灣被簡稱為 BNT 疫苗。這蠻有意思的,就像是 Oxford / AstraZeneca 疫苗,在臺灣被簡稱為 AZ 疫苗。似乎我們喜歡使用簡單的英文字母縮寫,但對於 Pfizer 或 Oxford 這種發音較難且沒有簡稱的字,就會直接略過。
這說明了,人類會根據自己的教育背景與生活經驗,去簡化我們所看到的世界,以求得快速的理解與認識。為了使有限的大腦處理能量,快速掌握近乎無限的世界變遷資訊,這是演化過程中,智人必然發展出的技能。
在臺灣,BNT 疫苗跟 AZ 疫苗一樣,都是曾經造成極化意見的產品,相對來說,莫德納就比較沒經歷過這樣的挑戰。有些人認為,BNT 疫苗就是神藥,非郭董 BNT 不打,有些人則認為,其效力跟意義,可能在臺灣被特定媒體與政治人物炒作得太高了。
加上,中國上海復星早期就卡住臺灣代理權,使得臺灣取得 BNT 疫苗相當困難,在民意被鼓動後,政府邀請台積電與鴻海共同達成合作默契,經歷一番努力,終於以「可能是除了以色列之外的世界最高單價」32 元美金左右,歐盟與美國 1.5 倍的價格,買到,並緩解集體焦慮。
- 延伸閱讀:
郭董公開信喊見面,總統說好,行政院授權台積電與郭台銘,然後見面兩個人一起。
Israel said to be paying average of $47 per person for Pfizer, Moderna vaccines / The Times of Israel
鴻海、台積電買BNT疫苗 每劑價格31至34美元 / 經濟日報
Covid-19: vaccine pricing varies wildly by country and company / Pharmaceutical Technology
當時的驚滔駭浪,不知道各位是否依然記得,美國的情報體系也對當時的臺灣輿論高度神話「郭董 BNT」以及瀰漫的焦慮感到訝異,於是 AIT 緊急協調同為 mRNA 原理的莫德納疫苗 15 萬劑迅速出貨(因為輝瑞 BNT 合作的疫苗,其臺灣代理權已經被 BNT 賣給上海復星,所以輝瑞沒辦法從美國出藥給臺灣),飛航路徑刻意繞開中國,之後甚至再由三位美國參議員,搭著美軍軍機 C-130 抵台,宣布捐贈 250 萬劑莫德納疫苗!
- 延伸閱讀:
這批 Monderna 是本來就訂的,但能夠立刻撥出 15 萬支,還提前在 5/28 抵達台灣,甚至比剛跟美國峰會過的南韓,預計 5/31 號拿到 5.5 萬支還快還多,應該是有些特殊的原因。
獨家》華航載15萬劑莫德納疫苗回台 航線申請避開中國飛航情報區 / 自由時報
感謝美國之際,對國際政治敏感度高的人,會開始思考的是,是否美國的情報體系評估後認為,臺灣的狀況很險峻。險峻到他們必須從 75 萬提高到 250 萬。如果是的話,臺灣目前檯面上的那些事情,是他們認為中共滲透嚴重且對國內事務有嚴重影響的呢?
【陪你看國際新聞】美國大送疫苗,表示臺灣情勢很險峻?
這本書,就是讓我們看看,一支能夠讓臺灣民意沸騰、美中在臺灣直接較勁、上海復星以代理權卡出高額政治溢價的疫苗,早期究竟是怎麼研發的。
去除那些因我們的生命經驗所造成的簡化印象,先放下讓我們激起濃烈情感的「BNT 疫苗」一詞,回歸到這支被收藏到倫敦醫學博物館,與詹納接種牛痘以預防天花的柳葉刀並列的,世界第一支 COVID-19 疫苗。真正的認識 BioNTech 這家公司,以及其里程碑疫苗的早期研發故事。
先聲明,我個人對這幾家疫苗的看法至今不變,只要政府組成的專家團隊評估過,並會購買的疫苗,都是好疫苗,而且他們有著不同的作用原理,也各自面對不同的未知,就我們所能得到的資訊,並沒有明顯的高下。輪到我,就去打。
我的兩劑 AZ 完整接種後,加強劑打的是當時鋪貨最廣的 BNT。而我自己的學齡孩子,學校開打之後,也完成了兩劑 BNT 完整接種。
- 延伸閱讀:
我經過自己的閱讀跟評估,對疫苗的態度一直都是:目前政府買的疫苗,在世界上都是很不錯的,不管是技術、製造穩定度、效果,都很好。如果有得打,就快點去打。/ 蔡依橙的閱讀筆記(2021/5/29)
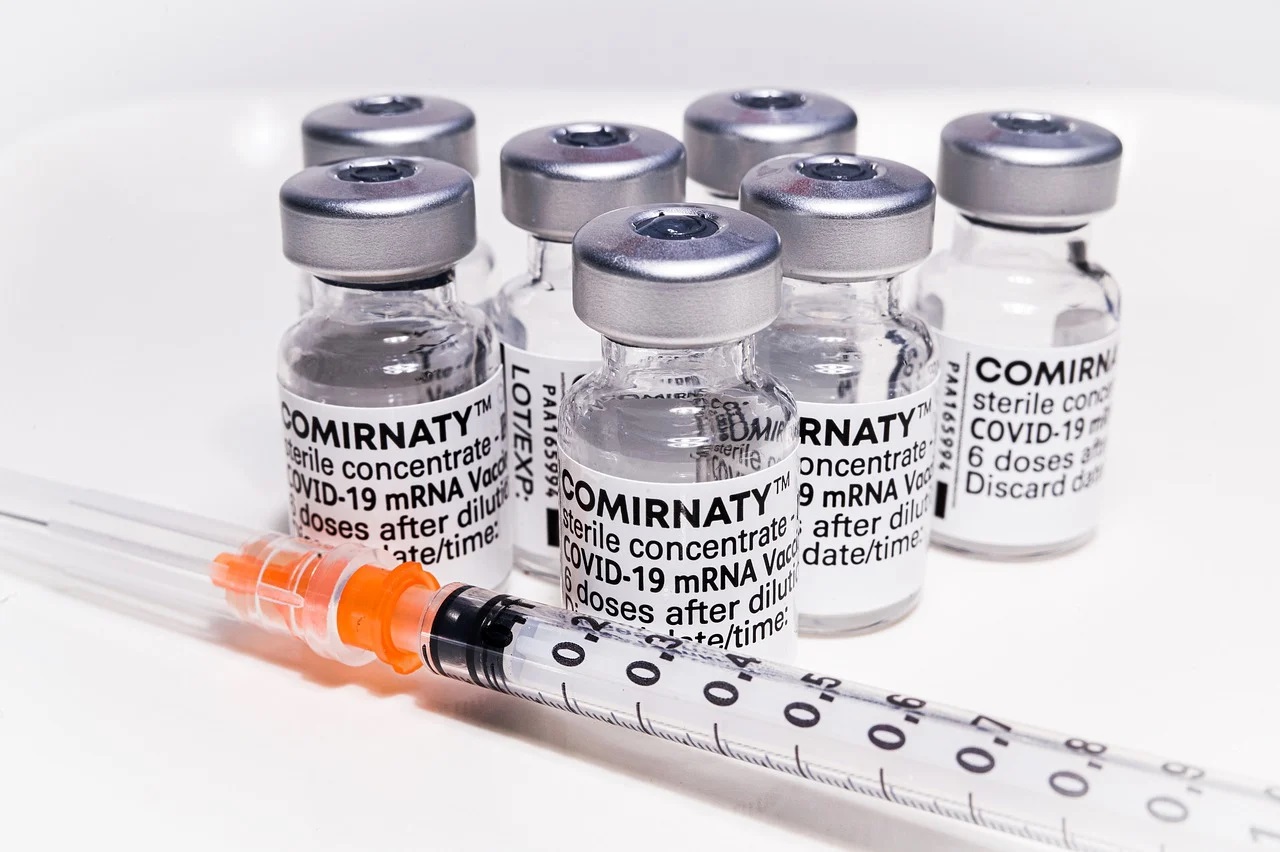
與天下文化另外四本疫苗書相比,《光速計畫》有什麼特別?
天下文化這次引進四本疫苗書,各有特色。
- 《疫苗商戰》:記者角度,綜論 AZ、BNT、輝瑞、莫德納、嬌生、Novavax。如果只想讀一本的話,這本很不錯。
- 《輝瑞登月任務》:輝瑞執行長角度,看看今天的世界級大藥廠,結合多元開放價值,能產生怎樣的力量。
- 《疫苗先鋒》:認識 AZ 疫苗背後,生物醫學研究者的真實狀況。
這次的《光速計畫》,則是介紹「輝瑞 BNT 疫苗」的 BNT 部分,也就是 BioNTech 這家低調又傳奇的公司,究竟有怎樣的老闆、怎樣的過去、怎樣的技術、怎樣的研發過程。
因為 BioNTech 過去真的很低調,這本《光速計畫》,分享了很多過去在媒體上沒有出現過的細節,如果你想要認識全世界第一支 COVID-19 疫苗,或者想要認識 BioNTech 這家未來可能會改變人類疾病治療模式的公司,都很值得讀。最有意思的幾個細節如下。
- BNT 早期的疫苗選株策略,這部分可以看出,他們強大的背景知識能力,以及在知識無法預測的風險區,如何規避風險。
- 以技術為主的小公司,決定擴廠時的艱辛。
- 與歐盟和德國政治人物的交手,發現他們寧願事後被檢討不夠積極,也不會做出需要冒風險的決策。跟現在歐盟對烏克蘭被侵略的態度類似。相對地,美國跟脫歐的英國,就積極許多。
- 與上海復星的合作過程。當初是 BNT 很想在 COVID-19 疫情最嚴重的起源地做臨床試驗,加上也希望自己的藥物能夠協助到十多億人。但 BNT 老闆夫妻,可能真的對台灣與中國的特殊狀況不瞭解,或者從中國方得到了不見得正確的資訊,才會簽出包括台灣在內的代理權。另外,作者們對中國也有很大的誤解,書中認為,中國很快就會核准 BNT 的販售與施打(324),但事實上到今天 2022 年 4 月,繁體中文版發行,上海都封城並產生人道危機了,BNT 疫苗在中國依然沒有被放行。
- 與輝瑞的合作過程。
- 最終,在以受體結合區域 (receptor binding domain; RBD) 設計的 BNT162b1 與修飾過的全部棘蛋白 BNT162b2 之間的選擇考量。以及最後的 BNT162b2,其實又從 8 變成 BNT162b2.9 的故事。前者 b1 與 b2 的差異,在學術期刊有,之前的報導也有提到,上海復星花錢買了 BNT 疫苗的研究開發權與經銷權,也嘗試過自行處理中國區的 b1 臨床研究,只是最後這株被放棄了。後者 b2.8 跟 b2.9,則是學術期刊與網路都沒出現過的,而且作者只提到「這種候選疫苗所攜帶的棘蛋白序列經過稍微修改,目的是優化細胞的轉譯工作。」並沒有提及細節,這部分的修改,可能被歸類為其商業機密。
- 作為土耳其裔德國人,作為移民,吳沙忻與圖雷西,是怎麼處理政治議題的。
如果你對於以上任何一項有興趣,這本書都很值得讀。
因為 BNT 疫苗研發過程中,分成 b1 跟 b2。上海復星擁有這兩者的研究開發權與經銷權,也嘗試過自行發展 b1 後續,只是最終出線的是 b2。這件事情被批露之後,有網軍大量把這個訊息攻擊成假訊息,但隨著《輝瑞登月任務》與 BNT 角度的《光速計畫》出版,這件事情確定就是真的了。當初為什麼會有一群瘋狂的網軍,要把這個消息洗成假的,洗到讓人都不敢再提呢?你認為是為什麼呢?
關於 b1 與 b2 的科學細節,可以參考以下兩篇。
- Viral targets for vaccines against COVID-19 / Nature Reviews Immunology
- Pfizer and BioNTech Pick a Vaccine Candidate / Science

從「個人」的角度閱讀
閱讀這本書時,我建議可以從「個人」與「系統」兩個角度來閱讀。
個人的角度是,去觀察究竟一個人,或者帶領的組織,要怎麼成功。可能是我們自己的專業人生經營,可能是我們小孩的學業或競賽,究竟有沒有什麼訊息是可以從書中萃取的。
我看到的是:
「到達成功的一整條路上,真的有太多的機緣跟運氣。我們只能隨時做好準備,等待這些機緣跟運氣,把自己推上頂峰。如果這次沒有成功,我們就繼續做好準備,等待下次更好的機緣與運氣。」
做好準備的人,有沒有可能失敗?有,像是在德國也做 mRNA,甚至得到比爾蓋茲投資的 CureVac 就失敗了,而同場競技的莫德納,更積極研發、更早進入臨床試驗,卻因為拿了美國政府曲速計劃的錢,被要求擴大研究設計與所收的資料,延遲數周,就這樣被輝瑞 BNT 疫苗超越,拿了個第二。
回頭看各種細節,CureVac 的失敗,有沒有可能發生在 BioNTech?有。
目前認為,CureVac 雖然同為 mRNA 疫苗,卻在臨床試驗失敗,是因為他們使用了自然的 mRNA 設計,而沒有使用假尿苷 (pseudouridine) 去取代原生尿苷 (uridine) 。
而這個使用原生尿苷的選項,也曾出現在 BioNTech 的候選疫苗中,甚至是吳沙忻夫婦心目中的第一候選(p.227 / 編號 BNT162a1),只是後續的動物實驗數據與概念推導,讓他們選用了使用假尿苷取代的 modRNA (modified RNA) 版本。
即使發明這個假尿苷取代法的兩位研究者,考里科和韋斯曼,其中的考里科就在 BioNTech 工作,吳沙忻夫婦也並沒有將這個最後被證明是關鍵修改的選項,放在第一指名。
這顯示,成功的科學並不是靠直覺就可以,還需要系統性的思考,系統性的避險,以及系統性的驗證。
但在這些未知的新領域,每個人所建立的系統,不管是思考系統、避險系統,還是驗證系統,並不一樣。CureVac 一定也對自己建立的決策系統很有信心,才會投注那麼多的時間與精力進入臨床研究,但結果就是不好,成王敗寇,沒辦法。
從「系統」的角度閱讀
我們也可以想想,臺灣會不會出現 BioNTech 這樣的公司。臺灣會不會塑造出這樣的醫師:當醫師時,覺得不足,於是做研究;做研究時,覺得不足,於是開公司;因為生技業的高風險與難找錢,於是股權被稀釋,覺得控制力不足;舊公司有好產品後全數賣掉,再投入新公司;從醫療轉到研究,從研究轉入商業,持續跨界並努力,一直深信自己有能力改變世界?
如果臺灣有這樣的人,他在當醫師的時候會不會過勞燒盡?去做研究的時候會不會被各種行政跟教學卡住?擔任獨立研究者時,會不會每年光是維持實驗室運作的科技部計畫申請就焦頭爛額?會不會在疲勞中,目標漸漸從創造出改變世界的治療方法,變成追求期刊 IF 以及升等委員長輩的喜好?如果真熬過這些了,在臺灣,他能募集到資金嗎?臺灣是德國那樣的生技市場嗎?連梅克爾都說德國不如美國,但臺灣跟德國相比呢?
如果臺灣有了 BioNTech 這樣的公司,會被媒體集體抹黑造謠攻擊嗎?會有首都政治人物持續開記者會嘲諷嗎?我們有建立好一個系統,去孕育出 CureVac 或 BioNTech 嗎?
這都是很值得我們共同去思考的。
不同的廠商,不同的敘事
客觀來說,輝瑞跟 BioNTech 的合作,的確快速又互相信任,但即使如此,如果對照《輝瑞登月任務》與 BNT 角度的《光速計畫》,會發現其實敘事有出入之處。我舉兩個例子。
第一,《輝瑞登月任務》中提到 (p.97-98) ,執行長博爾拉才是最終決定使用 b2 而非 b1 的決定者。但《光速計畫》明言,當初簽合約的時候,決定疫苗設計的最終決定權在 BNT 手上,而且是吳沙忻召集會議,說服兩家公司的高階主管的 (p.268-269) 。
第二,《輝瑞登月任務》全書完全避開直接批評川普,即使我們從各種博爾拉執行長的行為跟動作,都多少會推測,博爾拉本人應該很不喜歡川普,但無論如何,書中就是沒有任何直接批評。可能博爾拉本人就自己不想說,或者出版前,認真看過的公關跟法務團隊全部把負面詞彙修掉了。不過,BNT 這本《光速計畫》則是直接爆料,「博爾拉透漏自己一直在譴責川普 (p.276) 」,之後的疫苗製造廠承諾書連署,也是輝瑞針對川普的回應。很有意思。
閱讀共同的歷史
總結來說,我很喜歡這本書裡頭提及的許多細節,讓我們對這瓶世界第一支 COVID-19 疫苗、造成臺灣輿論沸騰的疫苗、結合小型尖端生技公司與世界級大藥廠合作的疫苗,有更進一步的了解。
這是我們共同經歷的歷史,藉由閱讀,也將成為我們共同深刻認識的歷史。

本文為《光速計畫:BioNTech疫苗研發之路》書評。2022 年 3月,天下文化出版。