當衰老成為一種可被治療的疾病:揭開長壽藥物的科學面紗【挺健康】
本文由 AI 協助生成
挺健康|長壽藥物的科學與現實|高齡醫學科 鄭丁靚醫師 我們從小就被教導,生老病死是自然界的鐵律。你有沒有想過,如果有一天,「變老」不再是生命的必然,而是一種可以被「治療」的疾病,那會是什麼樣的世界?想像一下,我們去醫院掛號,不是因為高血壓、糖尿病或關節炎,而是單純因為我們「正在變老」,而醫生能夠開出一張處方箋,讓你的細胞停止老化、甚至逆轉年齡。這聽起來像是科幻電影的情節,但現代醫學界正在做一件極度瘋狂的事:他們不再滿足於逐一擊破伴隨衰老而來的各種慢性病,而是想直接對「衰老」這個終極大魔王下手。那麼,現代醫學究竟打算如何把「衰老」當作一種疾病來醫治呢?
要回答這個問題,我們必須先打破一個迷思:這裡討論的抗老,不是塗塗抹抹的保養品,不是醫美診所的拉皮手術,也不是口服膠原蛋白讓皮膚看起來更緊緻。科學家正在研究的,是深入到「細胞層級」的抗老藥物。這些藥物的運作邏輯非常純粹,它們並不在乎你眼角的魚尾紋,而是試圖從分子層面干預細胞的運作機制,讓你的身體老得更慢、器官退化得更晚。既然科學家的目標不是單一疾病,學術界又是如何定義這些試圖對抗衰老本身的藥物呢?
在學術上,這類藥物有一個相對生硬卻非常精準的名字:Geroprotectors(衰老保護劑)。Geroprotectors 的核心理念在於,高血壓、糖尿病、阿茲海默症等疾病,其實都有一個更底層的共同敵人,那就是衰老本身。與其等疾病發生了才去吃降血壓藥或打胰島素,不如直接減緩衰老過程,從源頭阻斷這些疾病的發生。更重要的是,它的目標不僅僅是延長人類的「絕對壽命」,而是延長「健康餘命」(Healthspan)——讓你活到七、八十歲時,依然能健步如飛地去旅行、能自己上下樓梯、保有清晰的思考能力,而不是渾身插滿管子,雖然活著卻病痛纏身。既然目標如此宏大,這難道只是科學家關在象牙塔裡的科幻大夢嗎?
現代抗老藥物研究仰賴精密的實驗室分析(示意圖 / AI 生成) 今天這件事之所以值得我們花時間深入了解,原因只有一個:它早就不只是實驗室裡的理論了,它的發展潛力甚至已經讓全球最會計算風險的金融機構感到緊張。著名的「瑞士再保險公司」(Swiss Re)在近期的評估報告中,史無前例地把「長壽醫學」和「抗老藥物」寫進了他們的精算與風險評估框架裡。保險公司意識到,如果人類的健康壽命大幅延長,整個社會的退休金系統、醫療保險結構都將面臨天翻地覆的改變。在他們的報告中,甚至點名了一系列極具潛力的抗老候選藥物:二甲雙胍、雷帕黴素、NAD+前驅物,以及清除衰老細胞的藥物等。既然連最懂精算的商人都開始備戰,這份備受矚目的抗老候選人名單上,打頭陣的究竟是誰?
老藥新用的奇蹟:二甲雙胍的省電哲學
名單上的第一位候選人,你可能並不陌生。如果你的家族中有人罹患第二型糖尿病,十之八九都聽過、甚至吃過這顆藥:二甲雙胍(Metformin)。它是一顆歷史悠久、價格低廉、在藥局極為常見的「老藥」。但就是這顆看似平凡無奇的降血糖藥,現在卻搖身一變,站上了全球抗老研究舞台的 C 位。一顆用來控制血糖的藥物,究竟是如何跨界成為抗老明星的呢?
科學家發現,二甲雙胍的抗老秘密藏在細胞的發電廠——粒線體之中。在分子層面上,Metformin 進入細胞後,會對粒線體的發電效率「稍微踩一下煞車」。這個輕微的抑制作用,會導致細胞內的能量貨幣(ATP)濃度出現微幅下降。這時候,細胞內有一個極度敏感的「電量警報器」,稱為 AMPK 蛋白質激酶,它一旦偵測到能量下降,就會立刻響起紅燈。AMPK 一被啟動,細胞就會進入一種非常務實的「求生狀態」——這就像是你的手機電量剩下 15% 時,會自動進入低耗電模式一樣。細胞會關閉那些消耗大量能量的合成脂肪、促進細胞生長的路徑,轉而把寶貴的資源挪去進行「生存修復」與防禦。既然這套「低耗電修復模式」在理論上說得通,那麼在真實的生物體上,真的能看到效果嗎?
答案令人振奮。在 2024 年,頂尖科學期刊《Cell》發表了一項重量級研究。研究團隊讓一群雄性食蟹猴連續服用二甲雙胍長達 40 個月,並仔細追蹤牠們的生理變化。結果科學家驚訝地發現,這些猴子的大腦衰老速度顯著變慢了。透過精密的生物年齡測量,服用藥物的猴子其大腦的生物年齡竟然年輕了約 6 歲——換算成人類的壽命比例,這大約等同於大腦年輕了 18 歲!不僅如此,這些猴子的認知功能表現得更好,肝臟等器官的衰老指標也出現了逆轉。既然猴子吃了有效,那人類什麼時候才能名正言順地把它當作抗老藥來吃?
為了解答這個問題,美國醫學界目前正在推動一個極具野心的計畫,名為 TAME(Targeting Aging with Metformin)的大型雙盲臨床試驗。這個試驗的獨特之處在於,它是有史以來第一個試圖讓美國食品藥物管理局(FDA)承認「衰老本身」可以作為藥物適應症的試驗。過去 FDA 只核准藥物用來治療「特定疾病」,如果 TAME 試驗成功,這將徹底顛覆現代醫學的法規與常識,成為醫學史上的重大里程碑。不過,如果二甲雙胍是屬於溫和防守派,醫學界是否還有更具攻擊性的王牌?
激進的延壽冠軍:雷帕黴素與細胞清潔隊
接下來要介紹的這位選手,風格與二甲雙胍完全相反,它的效果更強大,但也伴隨著更高的危險性:雷帕黴素(Rapamycin)。在目前的動物實驗數據中,它是當之無愧的「延壽冠軍」。美國國家老化研究所(NIA)曾進行過一項長期且嚴謹的干預測試計畫(ITP),結果發現,Rapamycin 能夠讓小鼠的壽命延長高達 28%。更驚人的是,就算科學家等到小鼠步入晚年(大約換算成人類的 65 歲以上)才開始讓牠們服用,依然能夠顯著延長壽命。這位延壽冠軍究竟在細胞裡施展了什麼魔法?
它的原理與細胞內一種被稱為 mTOR 的蛋白質複合物密切相關。我們可以把 mTOR 想像成細胞內的一位「建築工頭」。當你吃飽喝足、營養充足的時候,這位工頭就會非常亢奮,一直對著細胞大喊:「開工啦!用力蓋房子!細胞分裂!快速長大!」對於正在發育的年輕生物來說,這是好事。但對於老年的細胞來說,如果這位工頭還是一直亢奮、一直逼迫細胞硬蓋房子,細胞就會因為過勞而開始偷工減料。更糟的是,細胞內原本應該被清理掉的代謝垃圾和損壞的胞器會越堆越多,就像一個只顧著蓋新樓卻從不收垃圾的工地,最後越蓋越亂、越蓋越髒。如果我們硬生生叫這位工頭閉嘴,細胞又會發生什麼事呢?
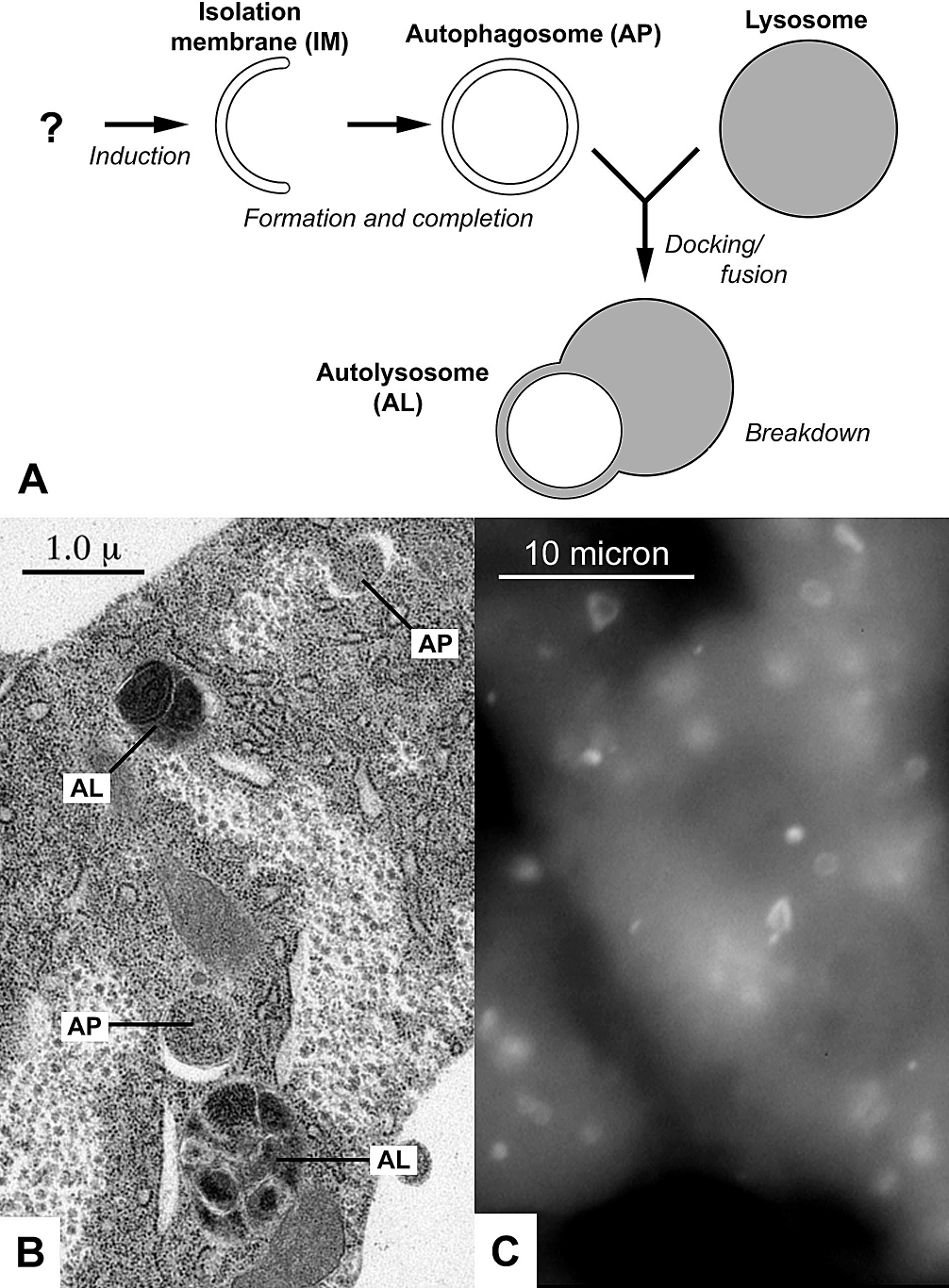
細胞自噬(macroautophagy)完整流程:從隔離膜形成、自噬體包裹,到與溶酶體融合後完成降解與回收。圖片來源:Wikimedia Commons ,Klionsky et al., PLoS Biology , 2008(CC BY 2.5) 這正是 Rapamycin 的作用機制。Rapamycin 進入細胞後,會直接對這位 mTOR 工頭下令:「閉嘴,立刻停工。」當 mTOR 的訊號被強烈抑制時,細胞就會意識到現在不是生長的時候,必須開始大掃除。於是,細胞會啟動一種名為「自噬作用」(Autophagy)的機制——細胞的身份從建築工人變成了清潔隊,把內部堆積多年的蛋白質垃圾、已經壞掉的粒線體全部打包,送到溶酶體中分解並回收再利用。透過這種深度的自我清潔,細胞煥然一新。既然雷帕黴素清垃圾的效果這麼好,為什麼醫生不立刻把它開給所有想抗老的人吃?
原因在於它的副作用。Rapamycin 原本在醫學上的用途,是作為器官移植患者的免疫抑制劑,用來防止身體排斥新器官。如果一個健康的人為了抗老而長期服用它,可能會導致免疫系統變得過度虛弱,增加感染風險;此外,它還可能讓傷口癒合變慢,甚至帶來高血糖的問題。雖然據傳矽谷有許多科技大亨已經在私下偷偷服用低劑量的 Rapamycin,但對於一般健康人類長期服用它的安全性,科學界目前仍然打著一個巨大的問號。既然這條路充滿風險,科學家有沒有其他相對安全,甚至能直接「拔除」衰老源頭的策略?
補充能源與清除殭屍:NAD+ 與 Senolytics
在抗老領域中,還有兩個近年來紅透半邊天的概念:NAD+ 以及 Senolytics。首先來看 NAD+(菸鹼醯胺腺嘌呤二核苷酸)。我們前面提到粒線體是細胞的發電廠,而 NAD+ 就是這座發電廠運作時絕對不可或缺的「必要耗材」。科學家發現,隨著人體年齡的增長,體內的 NAD+ 濃度會呈現斷崖式的下跌,導致細胞發電效率越來越差,人也跟著出現各種老化疲態。目前市面上非常熱門的 NMN、NR 等保健食品,其實就是 NAD+ 的前驅物,吃下它們的目的就是希望幫細胞的發電廠重新加滿油。然而,補充油料聽起來很合理,但如果細胞本身已經徹底壞掉,甚至變成了在體內作亂的「活死人」,單靠補充能量還救得回來嗎?
這就引出了另一個更激進、也更具革命性的概念:Senolytics(衰老細胞清除劑)。我們的身體裡每天都有細胞在分裂,當有些細胞受損嚴重,卻因為某些原因逃過了自然凋亡的機制時,它們就會變成所謂的「衰老細胞」,或者更直白地說——「殭屍細胞」。這些殭屍細胞極度討厭:它們既不肯乖乖死掉,也不再執行正常的生理功能,還會不斷向周遭分泌一種被稱為 SASP(衰老相關分泌表型)的發炎物質,感染周圍原本健康的細胞,讓健康的細胞也跟著發炎、加速老化。那麼,醫學界該如何對付這些體內的害群之馬?
Senolytics 類藥物的誕生,就是專門設計來獵殺這些殭屍細胞的。目前科學家找到的一個著名組合是「達沙替尼(Dasatinib)」搭配「槲皮素(Quercetin)」。這兩者結合在一起,能夠精準地辨識出殭屍細胞,並強迫它們啟動自我毀滅程式,從而在不傷害健康細胞的情況下,把體內的發炎源頭連根拔起。面對衰老這個牽涉數萬種基因和蛋白質的複雜問題,除了這些已經在實驗室裡反覆測試的藥物,我們還有其他潛在的盟友嗎?
從代謝總管到 AI 演算:未來的長壽藍圖
未來的抗老潛力股名單中,還有兩位不可忽視的超級巨星:GLP-1 類藥物與人工智慧(AI)。GLP-1 類藥物就是近年來爆紅的「瘦瘦針」。但科學家越來越確信,它絕對不只是一支能讓你變瘦的減肥藥而已——它更像是人體代謝系統的「總指揮」,能連帶改善血壓、逆轉脂肪肝、大幅降低體內的系統性發炎指標。在多項大型臨床研究中,甚至證明了它能顯著降低重大心血管事件的發生風險。這些改善代謝的連鎖反應,恰好精準打擊了衰老過程中的多個痛點。
AI 透過演算法在數百萬分子中快速篩選候選藥物(概念示意圖 / AI 生成) 而 AI 的加入,更是徹底改變了抗老藥物的研發遊戲規則。過去找藥就像是「大海撈針」,科學家必須把成千上萬種化合物一種一種拿來測試,耗時數十年。現在,AI 正在把藥物開發變成一門「精準計算」的科學——強大的演算法可以在短時間內篩選數百萬種分子的 3D 結構,預測它們與人體抗老標靶結合的機率,直接在伺服器裡把長壽藥「算」出來。科學正在以我們難以想像的速度,把「長壽」從一種中彩券般的基因運氣,變成一種可以被精準管理的人體工程。然而,當科學的突破即將實現,我們是不是又將面臨一個嶄新的社會問題?
這帶來了一個極其嚴肅的倫理考驗。如果這些抗老藥物真的在人類身上發揮了強大的延壽效果,這會不會最後變成專屬於「富人的長壽套餐」?當壽命可以被明碼標價,活得更久、更健康,會不會成為階級社會中新的貧富差距指標?這些問題,科學無法單獨解答,需要整個社會的法規、保險體系與道德共識來共同面對。
但可以確定的是,抗老醫學的列車已經離站。在未來的某一天,醫生真正能在診所裡開出完美無缺的「抗老處方籤」之前,身為普通人的我們,其實早已經掌握了最無副作用的抗老秘方——那就是那句聽起來老套,卻依然是科學鐵律的話:維持均衡的飲食、保持規律而適度的運動,以及,永遠對這個世界保持一顆年輕且充滿好奇的心。
參考文獻
López-Otín C et al., “The Hallmarks of Aging,” Cell , 2013.
Swiss Re Institute, “Longevity and life sciences,” 2024.
Yu Z et al., “Metformin reduces aging-related leaky gut and improves cognitive function by decreasing the LPS level in cynomolgus monkeys,” Cell , 2024.
Barzilai N et al., “Metformin as a Tool to Target Aging,” Cell Metabolism , 2016.
Harrison DE et al., “Rapamycin fed late in life extends lifespan in genetically heterogeneous mice,” Nature , 2009.
Saxton RA & Sabatini DM, “mTOR Signaling in Growth, Metabolism, and Disease,” Cell , 2017.
Yoshino J et al., “NAD+ Intermediates: The Biology and Therapeutic Potential of NMN and NR,” Cell Metabolism , 2018.
Zhu Y et al., “New agents that target senescent cells,” Aging (Albany NY) , 2017.