No one is safe until everyone is safe.
沒有人是安全的,除非每個人都安全了。
近日,出現了臺灣本土首個 δ(delta, B.1.617.2, 印度)變異株傳播鏈的群聚事件。許多人都擔心,delta 變異株有可能會再引起新一波的疫情。 delta 變異株的傳染力真的比較強嗎?目前正在施打的疫苗,能不能因應新的變種病毒呢?
delta變異株比 alpha變異株更具傳染力
COVID-19 感染了近 1 億 8 千萬人,病毒(SARS-CoV-2)也產生了無數次的突變。若突變使病毒符合下述其中一項 [1]:
- 傳染力增加,明顯變成當地優勢株
- 致死性增加或臨床病徵改變
- 原始診斷、治療、預防/疫苗的效力降低
就會因危險性過高,被世界衛生組織(WHO, World Health Organization)列為「值得關注的變異株(VOC, Variants of Concern)」。目前在表上有四種變異株,這些變異株也是讓全世界都頭痛的突變病毒。
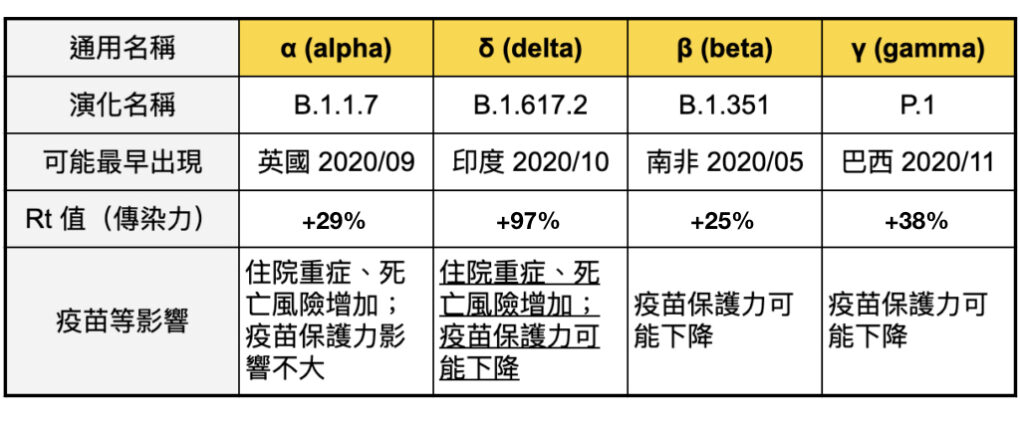
α(alpha, 英國)變異株 [3]最早在英國被發現。數月後,英國的新確診者,多數皆是被 α 變異株感染,逐漸成為優勢株,顯示其傳播力較原版病毒有所增加。
臨床統計也顯示了其棘手的特性。哈佛大學團隊研究 65 名患者(其中 7 名體內為 α 變異株)體內病毒量;團隊發現,α 變異株在人體內繁殖、被清除的時間都變長了;換言之,患者整體攜帶病毒的時間,拉長了近兩倍。
此特性使 α 變異株更有機會穿透國境管理,有更充裕的時間傳染給更多人。

而來自南亞的 δ 變異株,傳播力可能比 α 變異株更令人擔心。根據英國的研究統計發現,δ 變異株在家庭裡的傳染力,比 α 變異株更高 [4]。
專職數據研究的《歐洲監測 (Eurosurveillance)》期刊,於六月刊出各變異株的有效再生數 (Rt, effective reproduction numbe) 。如下圖,可發現各變異株的Rt值皆有增加,而其中又以 δ 變異株暴增的傳染力最令人驚訝 [5]:
- β(南非)變異株:增加 25 %
- α(英國)變異株:增加 29 %
- γ(巴西)變異株:增加 38 %
- δ(印度)變異株:增加 97 %
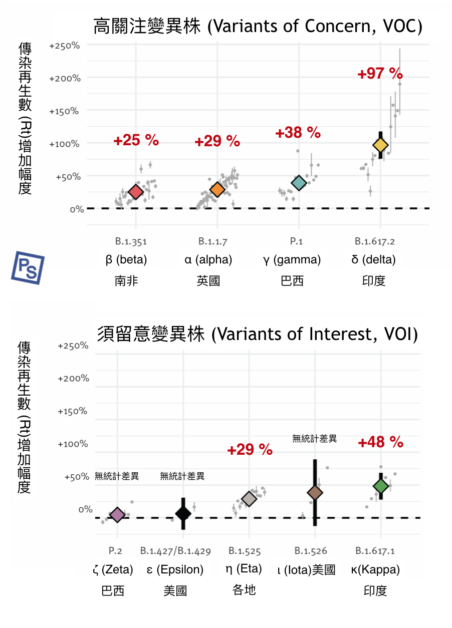
中文資訊為本文作者加註。圖/參考文獻5
流行病學數據顯示了 δ 變異株的傳染優勢,日本更預測東京奧運之前的七月中旬,現今日本主流的 α 變異株,將會被更兇狠的 δ 變異株取代。
那感染了 δ 變異株,死亡率會更高嗎?蘇格蘭研究,發現若感染了 δ 變異株,患者的重症住院風險增加(相較於 α 變異株) [6]。新加坡也顯示相同的結論,他們發現感染 δ 變異株後,更高比例的患者需要氧氣支持(肺功能嚴重降低)、急重症、死亡;而細究實驗室數據,發現其體內病毒的 Ct 值較低(病毒濃度較高),且人體清除病毒的時間需要更久 [7]。
從趨勢或數據都顯示,相較於 α(英國)變異株,δ(印度)變異株是個傳染力、破壞力更強大的對手。
英國經驗:疫苗,打好、打滿
英國(06/25)的研究報告發現,相較於 α 變異株,疫苗(未分品牌)對 δ 變異株的保護力稍稍下降。如下表所示,單劑疫苗對抗 δ 變異株僅 32% 效力,但若打滿 2 劑,保護力將上升至 79% [8]。

而疫苗的核心精神——避免重症住院,對抗 α 或 δ 變異株的能力就幾乎相同。單劑疫苗,能降低感染約八成的住院風險,若打滿 2 劑,住院風險更減少 96% [8]!
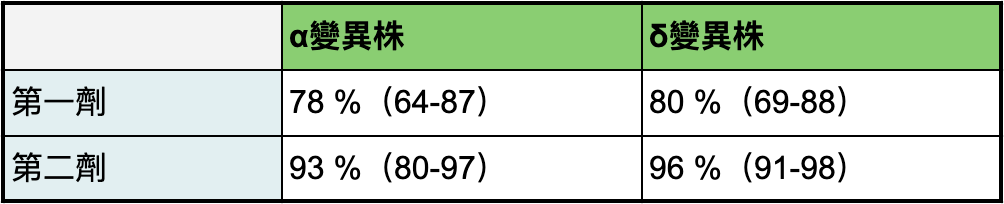
對付δ 變異株,AZ 較輝瑞-BNT疫苗弱,但仍足以抵禦重症
而疫苗品牌和保護力的關係,就預防「感染 δ 變異株且出現症狀」的效果而言, AZ 較輝瑞-BNT疫苗的保護力弱。兩劑 AZ 疫苗約 59% 的保護力,而輝瑞-BNT疫苗仍有近 87 %(表5)[9]。
此研究顯示,若想避免感染 δ 變異株,AZ 疫苗可能稍微力不從心。因此,最容易遇到 δ 變異株的機師、醫護團隊,可考慮更高保護力的疫苗,甚至接種第 3 劑,以阻絕 δ 變異株侵入他們體內。
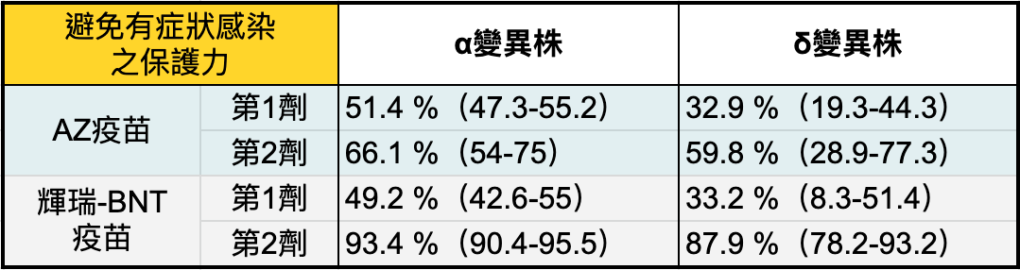
至於對預防「感染 δ 變異株後惡化成重症」而言,AZ 和輝瑞-BNT 效果相似 [10]。只要接種滿兩劑,AZ 疫苗預防重症的效力達到 92%,和輝瑞-BNT 的 96% 相似(表6)。
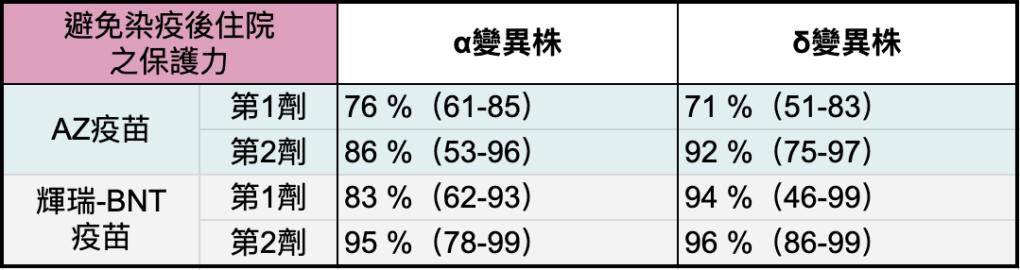
由於 AZ 疫苗是台灣最大量的疫苗。此研究顯示,只要打滿兩劑 AZ 疫苗,就有高保護力避免重症、甚至死亡。因此 AZ 疫苗,提供給台灣民眾來抵禦 δ 變異株,應該相當充裕。
換言之,英國的報告跟台灣說,對付 δ 變異株,就是「打疫苗,打滿、打好」。
No one is safe until Everyone is safe. 沒有人安全,除非每個人都安全
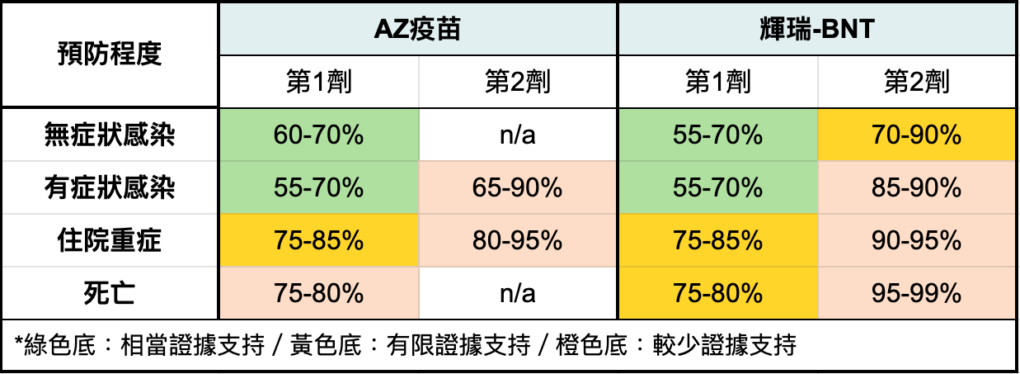
英國累積了超過半年的研究,發現疫苗的確能保護英國國民(表7)。不論 AZ 或輝瑞-BNT 疫苗,單劑就有約六成的保護力;若能打滿兩劑,避免重症、死亡的效力,更提升至約九成 [11]。
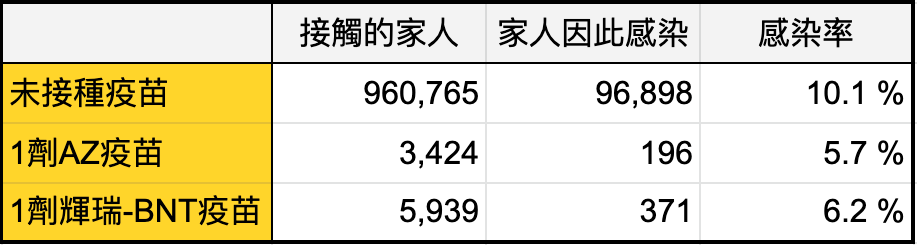
而近日於《新英格蘭醫學期刊 (New England Journal of Medicine)》的報告,更顯示了「打疫苗,更是保護家人」的概念 [12]。如表8,團隊分別追蹤了「無接種疫苗」和「接種1劑疫苗」之確診者的家人。發現:
- 沒打疫苗,若成為確診者,約莫 10% 的家人也會被感染
- 打了疫苗,即使成為確診者,家人被感染的風險降低 40-50%
疫苗之意義,不是自己從此無敵;而是有著更深層、重要的意涵——「讓家人更不容易被自己感染」。「No one is safe until Everyone is safe. 沒有人安全,除非每個人都安全了。」
COVID-19 已經深入社會,每個人幾乎都會被感染,也會變成傳染者。有鑑於病毒對年長者、孕婦等的殺傷力,每個人都應該接種疫苗。特別是若親友因故無法接種疫苗,那麼我們接種疫苗、保護親友,就成了責無旁貸的義務。
保持冷靜,繼續前進。Keep Calm and Carry On.
備註:
若某變異株,判斷基因可能影響病毒表現,並且符合下述任何一項 [1]:
- 已出現社區傳播或多個病例
- 已在多個國家/地區被發現
- 世界衛生組織評估可能有潛在危險性
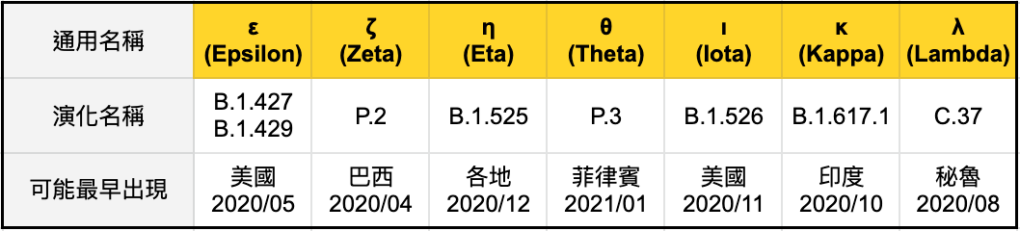
就會因為值得監控,而被世界衛生組織列為「須留意變異株 (Variants of Interest, VOI)」,即未來可能變成高度破壞力的變異株(表9)。
參考文獻
- Tracking SARS-CoV-2 variants. World Health Organization
- SARS-CoV-2 Variant Classifications and Definitions. US Centers for Disease Control and Prevention
- 蔣維倫 (2021) 進擊的病毒:變異如何影響疫情?疫苗效力會因此減弱嗎?科技報導
- SARS-CoV-2 variants of concern and variants under investigation in England: technical briefing 15. Public Health England. 2021/06/11
- Finlay Campbell, Brett Archer. et. al. (2021) Increased transmissibility and global spread of SARS-CoV-2 variants of concern as at June 2021. Eurosurveillance. https://doi.org/10.2807/1560-7917.ES.2021.26.24.2100509
- Aziz Sheikh, Jim McMenamin, Bob Taylor, Chris Robertson (2021) SARS-CoV-2 Delta VOC in Scotland: demographics, risk of hospital admission, and vaccine effectiveness. The Lancet. DOI: https://doi.org/10.1016/S0140-6736(21)01358-1
- Sean Wei Xiang Ong, Calvin J. Chiew. et.al. (2021) Clinical and Virological Features of SARS-CoV-2 Variants of Concern: A Retrospective Cohort Study Comparing B.1.1.7 (Alpha), B.1.315 (Beta), and B.1.617.2 (Delta). http://dx.doi.org/10.2139/ssrn.3861566
- SARS-CoV-2 variants of concern and variants under investigation in England: technical briefing 17. Public Health England. 2021/06/25
- Jamie Lopez Bernal, Nick Andrews. et. al. (2021) Effectiveness of COVID-19 vaccines against the B.1.617.2 variant. medRxiv. DOI: https://doi.org/10.1101/2021.05.22.21257658
- Julia Stowe, Nick Andrews. et. al. (2021) Effectiveness of COVID-19 vaccines against hospital admission with the Delta (B.1.617.2) variant. Preprint
- COVID-19 vaccine surveillance report Week 25. Public Health England. 2021/06/24
- Ross J. Harris, Jennifer A. Hall. et.al. (2021) Effect of Vaccination on Household Transmission of SARS-CoV-2 in England. New England Journal of Medicine. https://www.nejm.org/doi/full/10.1056/NEJMc2107717