- 本文於 2020/10/6 新增新興科技媒體中心所提供之內容資料。
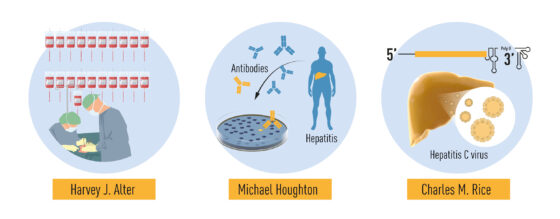
2020 年的諾貝爾生醫獎頒給了 Harvey J. Alter,Michael Houghton 和 Charles M. Rice,表彰他們發現了 C 型肝炎病毒。也因為他們的貢獻,使得病毒性 C 型肝炎的血液檢查和新藥得以出現。
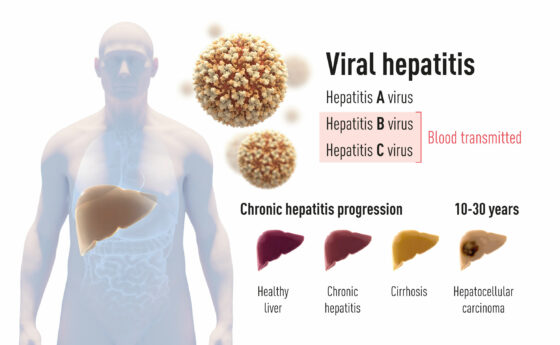
肝炎主要是由病毒感染所引發的疾病,而酗酒、環境中的毒素以及自體免疫性疾病也可能造成肝炎。在 1940 年代,有兩種主要的傳染性肝炎,第一種是 A 型肝炎,A 肝主要是透過污水和食物傳播的,通常對患者幾乎沒有長期影響。
而第二種肝炎則是通過血液與體液傳播,會導致慢性疾病,能潛伏在體內非常長久的時間,同時可能發展為肝硬化和肝癌。這種「隱性」的肝炎嚴重威脅了人們的健康,每年造成全球超過百萬人死亡。
在C肝病毒的研究時程上,科學家是先找到了病毒的基因序列,所以才有利於後續的病毒檢測及藥物治療研究與發展。成功分離此病毒,阻止病毒傳播,也就有機會研究出對抗它的方法。此研究對全球人類健康的影響深遠。

傳染源在哪裡?
要成功防止傳染病,第一步就是要確認病原體。在 1960 年代,Baruch Blumberg 發現了其中一種以血液傳播的肝炎是由 B 肝病毒所傳播的,而這項發現促進了相關診斷和疫苗的發展,而因為這項發現,Blumberg 於 1976 年獲得了諾貝爾生醫獎。
而同一時間,在美國衛生研究院 (NIH) 任職的 Harvey J. Alter 與他的同事發現:儘管檢測 B 肝病毒降低了部分因為輸血而感染的肝炎病例,但仍有不少不明病例存在,而這些肝炎的成因既不是 A 肝病毒、也不是 B 肝病毒。
未知的感染源不但透過輸血傳染給大量患者,Alter 和同事更發現肝炎患者的血能進一步傳染給黑猩猩。透過研究和觀察,Alter 將這種肝炎定義為一種新的「非 A 非 B 型肝炎」(non-A, non-B hepatitis)。
你可能會好奇,都能找到A型和B型病毒了,C型有什麼難的?長庚大學生醫系客座教授羅時成在新興科技媒體中心所舉辦的「2020諾貝爾生醫獎 線上解析記者會」中指出,因為C肝病毒在人體血液內的數量很少,一開始很難發現C型肝炎病毒。
把 C 型肝炎病毒抓出來!
找出病毒是當務之急,但儘管用了當時所有能用的技術,卻仍無法將病毒分離出來。 Michael Houghton 在Chiron製藥公司工作,並進行了分析病毒序列的工作。Houghton 和他的同事們從被感染的黑猩猩血液中提取了DNA片段,這些片段大部分來自黑猩猩本身的基因組,但研究人員預測其中有一些片段是來自未知的病毒,並假設肝炎患者的血液中存在針對這個病毒的抗體。他們使用患者血清來測試 DNA片段編碼的病毒蛋白,並在其中發現了陽性反應!而這個片段來自一種新型的RNA病毒,屬於黃熱病毒科,被命名為C型肝炎病毒。
C 型肝炎病毒的發現具有重要意義,但仍有難題尚未被解決:僅僅病毒本身就能引起肝炎嗎?
為了回答這個問題,科學家不得不研究複製的病毒是否能夠並引起疾病。 Charles M. Rice 以及其他研究RNA病毒的小組指出,C 型肝炎病毒基因組末端的一個先前未知的區域,可能對病毒的複製非常重要。Rice 還觀察到分離出的病毒樣本中有遺傳變異,並假設其中一些可能會阻礙病毒複製。
透過基因工程,Rice 製作出了 C 型肝炎病毒的 RNA 變異體,其中包括病毒基因組那重要卻在之前未被發現的區域。將這種 RNA 變異體注射到黑猩猩的肝臟中後,能在血液中檢測到病毒,並觀察到與肝炎患者相似的病理變化,這證明了 C 型肝炎病毒是能導致透過輸血引起肝炎的病毒。
C肝病毒的發現有多重要呢?
中興大學生科系特聘教授林赫表示,本次三位得主因其不同階段的貢獻,從這個疾病的臨床發現,再到臨床與基礎研究的合作,最後得到對人類有益的成果,而獲頒諾貝爾獎。作為一個基礎研究學者,很多時候研究靈感都來自於臨床觀察,兩者互相結合是非常重要的。
在過去,臺灣因輸血而得到的肝炎中,約 69% 為 C 型肝炎,但從民國 81 年 7 月起,C 型肝炎抗體檢驗納入血液篩檢項目之一後,幾乎就沒有輸血後 C 型肝炎的案例了。
而之所以能有相關血液篩檢,便要歸功於此次諾貝爾獎的三位得主。他們對於 C 肝的發現在抗疫之戰中扮演了非常重要的角色,正因為他們的研究,我們現在已經發展出了非常精準的血液檢測技術,因此大幅降低了因輸血而產生的 C 肝傳染。
另一方面,他們的發現也使得相關抗病毒藥物快速發展,目前的醫療技術已經能夠治癒 C 肝,未來,若是可以更全面地推動 C 肝檢測以及相關藥劑投放,或許能在世上消滅 C 肝。

陽明大學生科研究所退休教授周成功認為,諾貝爾生醫獎今年頒給發現C肝病毒的科學家們,很清楚告訴我們基礎研究非常重要,只有在具備扎實的基礎研究能力上,當社會出現重大的公共衛生議題時,我們才有能力找出原因,並發展有效治療的方法。從本次諾貝爾生醫獲獎得主的背景得知,國外是以循序漸進的模式來發展科學研究,台灣的科研環境還有很大的進步空間。
- 本文部分內容來自 台大新興科技媒體中心 2020諾貝爾生醫獎 線上解析記者會,相關內容的影像紀錄請參考:










































