本文轉載自中央研究院研之有物,泛科學為宣傳推廣執行單位
- 採訪編輯|歐宇甜、美術編輯|林洵安
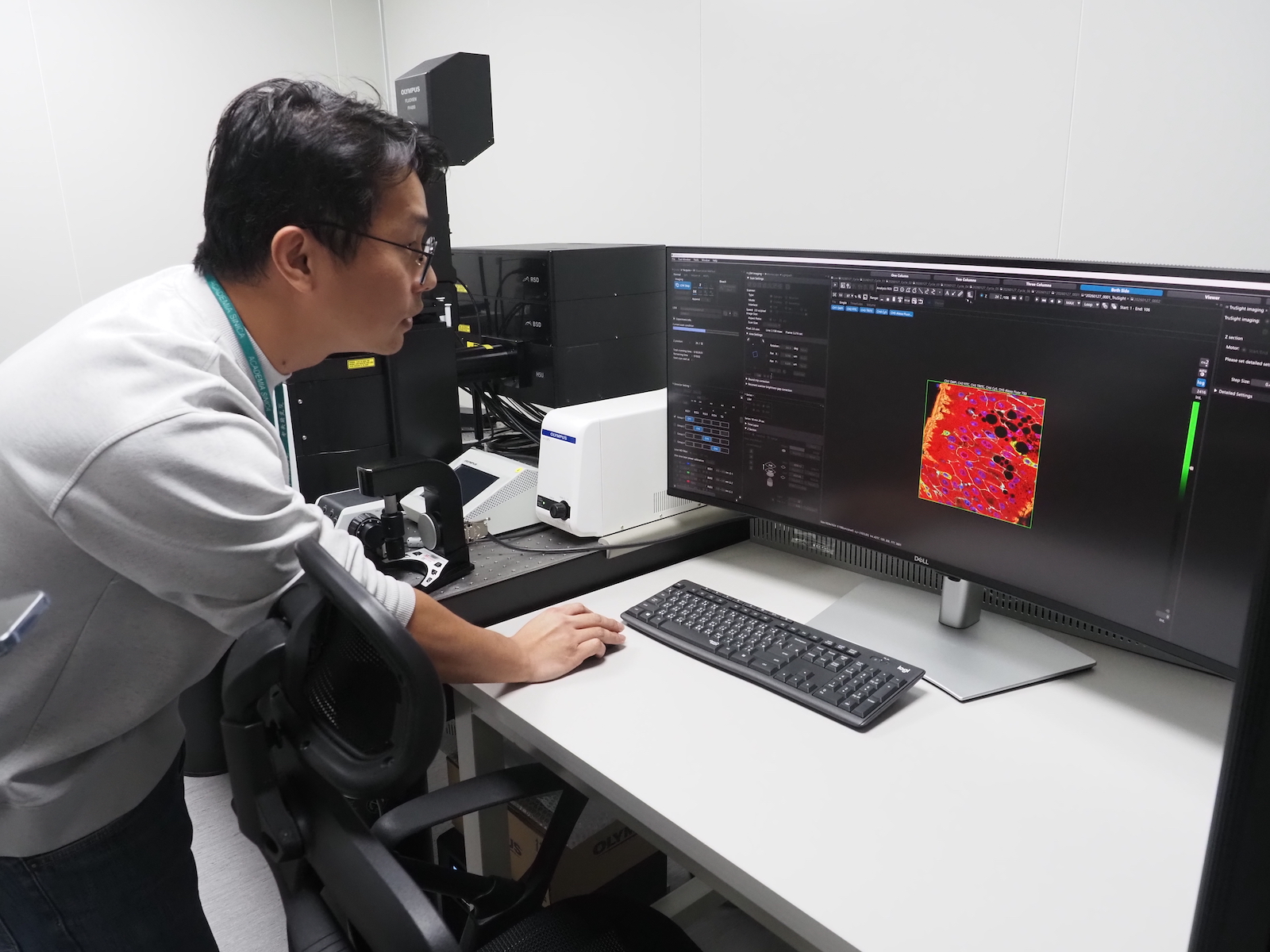
我們的動機是如何形成的?大腦如何操縱飢渴的行動?中研院分子生物研究所林書葦助研究員帶領研究團隊,發現果蠅腦中有一種名為 leucokinin 的神經傳導物質,它能調控不同的神經細胞,影響果蠅進行覓水或覓食的行為,更發現渴、餓的神經機制在果蠅腦中會交互作用,研究成果已於 2019 年 10 月登上《自然:神經科學》(Nature Neuroscience),跟著研之有物一起來了解。

為什麼要研究果蠅大腦?
「果蠅大腦雖然簡單,卻可以解決重大的問題。」林書葦一語道破。如果不是果蠅大腦,我們對於複雜的人類大腦將更加束手無策!
果蠅大腦只有 10 萬顆神經細胞,人類大腦有 1000 億顆神經細胞,宛如早期的 286 電腦對上如今的超級電腦。但果蠅的腦雖然簡單,功能卻一應俱全,有各種感覺,也能學習與記憶。如果能找出果蠅大腦的各類運作機制,將有助於了解其他更複雜的動物腦,甚至人腦。2017 年的諾貝爾生理醫學獎,即是頒給三位研究果蠅生理時鐘的科學家。
林書葦研究團隊此次的發現,則是揭開果蠅大腦關於「動機」的秘密:渴和餓的神經迴路。
「動機是種內在的驅力,影響我們的行動、感受、做決定的過程,還有學習和記憶,也與憂鬱症、厭食症、成癮症相關。」林書葦解釋:「餓與渴,即是非常基本且普遍的動機。我們想知道果蠅怎麼知道自己渴了、餓了?又是哪些神經細胞負責操控找水、覓食等行為。」
訓練果蠅大作戰
實驗目標很明確,但一開始,研究員得先訓練果蠅學會按照特定訊號找水、覓食,建立行為系統,才能觀察過程中的大腦變化。
幫果蠅「上課」,聽起來簡直匪夷所思,怎麼辦到的?研究員運用一種 T 字狀迷宮「T-maze」,先讓果蠅渴八個小時,然後進入 T-maze ,通入氣味 A、不給水,接下來再通入氣味 B 、給水喝,訓練果蠅將氣味 B 與水連結起來,產生與水有關的嗅覺記憶。
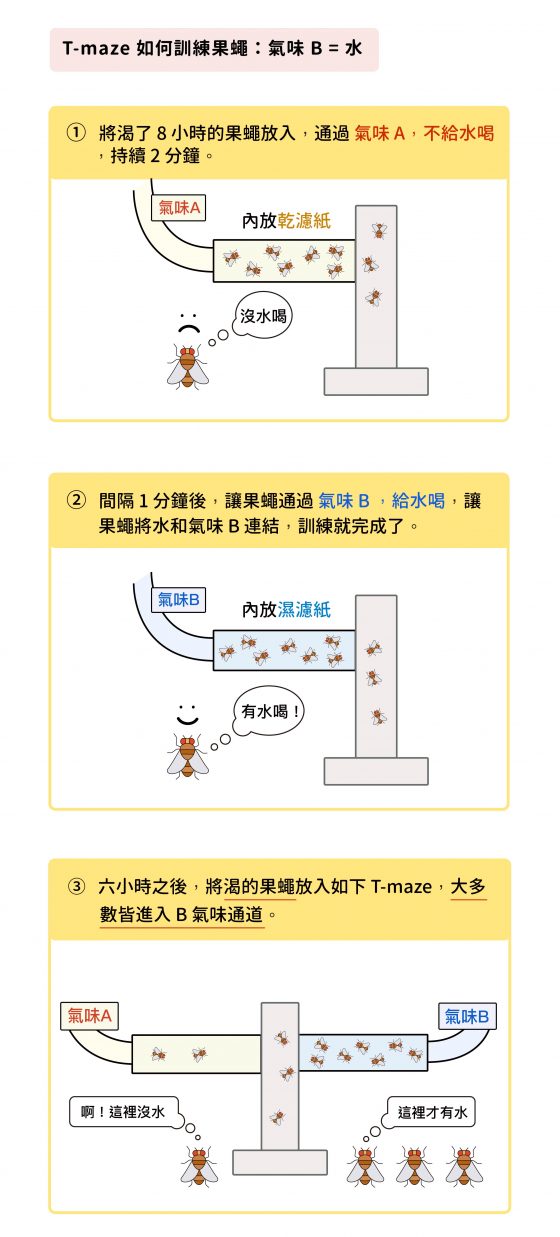
覓食的嗅覺記憶也使用 T-maze 訓練:
但實驗沒多久,研究團隊即發現果蠅只會產生短期記憶,訓練完半小時就統統忘個乾淨。他們不斷思考改進並反覆測試:如何延長果蠅的記憶?
後來發現,適合學習與記憶訓練的果蠅必須滿足一些條件。一般果蠅壽命約一到兩個月,年紀太輕的果蠅大腦尚未發育成熟,年紀大的果蠅學習與記憶力跟人類一樣會降低,所以必須挑選出生 5~7 天的「不太小不太老」的果蠅做實驗。
花了快半年時間,研究團隊又發現「讓果蠅渴得剛剛好」這件事很重要。早期他們讓果蠅渴大約 16 個小時,結果果蠅學習力很差,研究團隊猜測,長時間的缺水,可能讓果蠅身體變得太虛弱,大腦功能降低。後來他們嘗試放入乾燥劑,讓果蠅更快感覺渴,但身體狀態較好,果真產生比較穩定的長期記憶。
歷時半年多,終於訓練成功!以口渴的果蠅為例,訓練完成 6 小時(以上)之後,再將牠們放入 T-maze,大多數會乖乖進入 B 氣味通道,而且果蠅只在渴的時候才會尋找 B 氣味。
接下來,研究員即可準備觀察在果蠅大腦中,哪些神經細胞和找水、覓食有關。簡言之,他們會分別抑制果蠅大腦中不同位置的神經細胞,觀察哪些神經細胞被抑制時,將影響果蠅找水、覓食的行為。
找到與渴相關的神經細胞
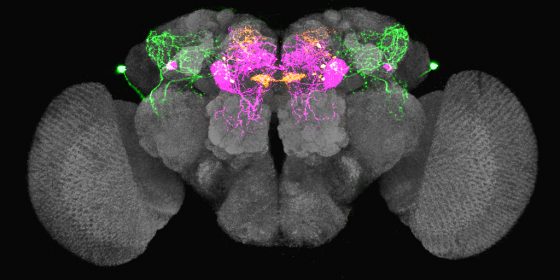
結果發現,果蠅大腦有一些神經細胞會分泌神經傳導物質「leucokinin」,是負責渴的訊號;Leucokinin 是一種短的蛋白質鏈,稱為神經胜肽,過去只知道它在其他昆蟲體內與維持體內水分平衡有關,但作用的細節並不清楚。當果蠅口渴時,leucokinin 會在腦中釋放, 促使果蠅去找水。
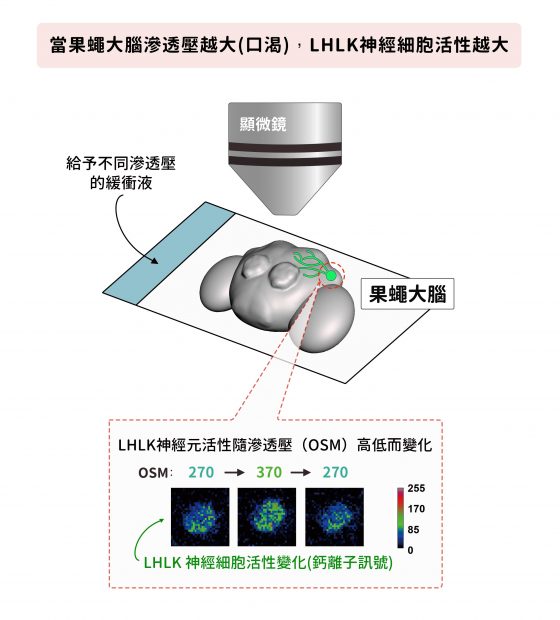
但果蠅大腦有三群會表現 Leucokinin 的神經細胞,到底哪一群才是跟渴有關呢?由於生物體內水變少了,滲透壓會上升,這通常是渴的第一個訊號。因此研究團隊將果蠅大腦「取出來」,給予不同的滲透壓溶液,看看那些細胞會根據滲透壓變化起反應。
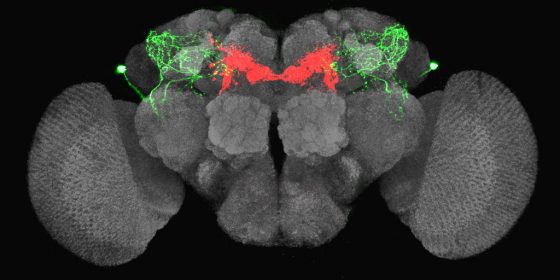
研究員將取出的果蠅大腦固定在顯微鏡開口,放入緩衝液讓腦不會乾掉,以觀察神經細胞活動。當滲透壓升高,只有一群名為 LHLK 神經細胞活性會上升,並釋放 Leucokinin;當滲透壓降低,LHLK 神經細胞的活性就恢復正常,宛如「滲透壓偵測器」,應該與渴的訊號有關。
渴與餓訊號的神秘交織
更精彩的還在後頭!當他們繼續追查 LHLK 神經細胞的運作機制,竟然發現 LHLK 神經細胞並不是專一性的,它同時和渴與餓的訊號有關,而且呈現有趣的交互作用!
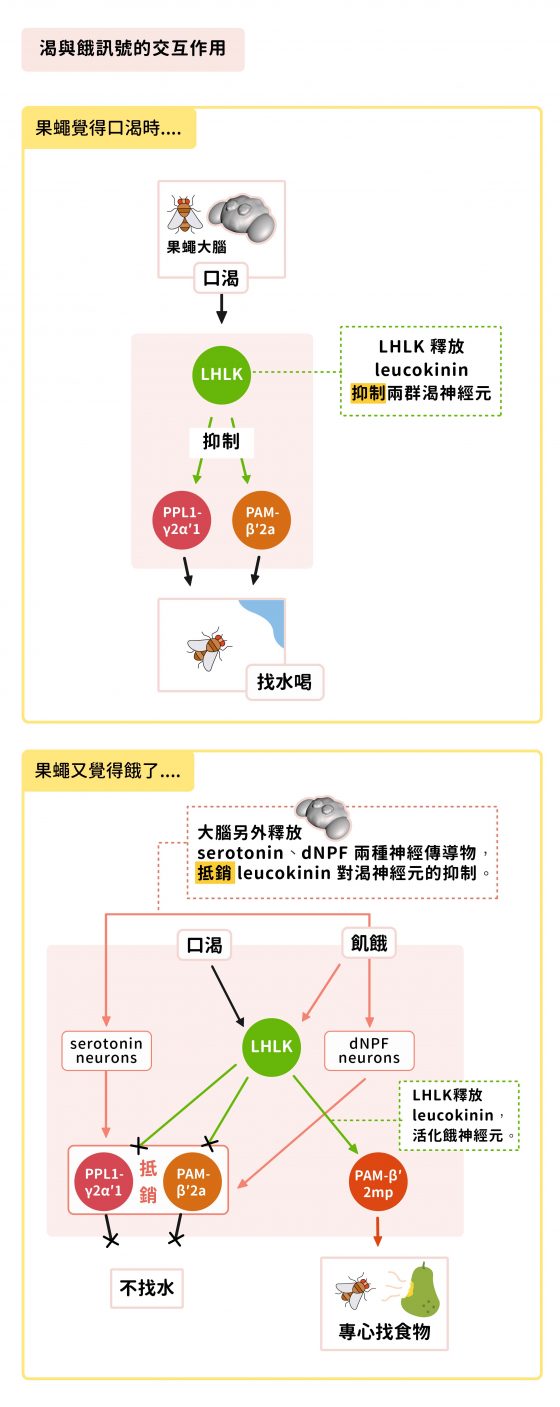
當果蠅口渴時,LHLK 神經細胞會釋放 leucokinin 前去抑制兩群渴神經元 (PPL1-γ2α′1、PAM-β′2a)。因為這兩群渴神經元 (PPL1-γ2α′1、PAM-β′2a) 屬於抑制性的神經細胞,就像一道關閉的門,會抑制覓水行為,但 leucokinin 能抑制它們活性,產生負負得正的效果,讓果蠅出現覓水的行為。
當果蠅餓的時候,LHLK 神經細胞也會釋放 leucokinin,卻是活化另一群餓神經元 (PAM-β′2mp),讓果蠅出現覓食行為。在此同時,大腦竟會釋放另外兩種神經傳導物質 serotonin、dNPF,抵銷 leucokinin 對渴神經元的抑制,讓果蠅不想找水。
原來,大腦並非單純只用一群神經細胞負責渴訊號,另一群神經細胞負責餓訊號,彼此之間還有複雜的交互作用!為何會如此?林書葦認為,LHLK 神經細胞可能是演化上較為古老的一群細胞,果蠅祖先的生活環境或許相對單純,水與食物往往並存,所以覓食尋水只需要由一個單一訊號 (leucokinin) 來調控。
後來生活環境越來越複雜,有時比較容易找到水、有時比較容易找到食物,大腦漸漸發展出比較複雜的路徑,透過多種神經傳導物質的合作、競爭,去調控不同的神經細胞,讓果蠅能在更複雜的環境中,按照生理需求做出最有效率的選擇,比方說當牠們渴了又餓,會選擇去找食物而非水。
大腦電路,解碼中……
故事還沒完!林書葦仍有更多問題想追究:當果蠅渴的時候,是不是也會抑制覓食的行為?是不是還有別的渴訊號?這些渴、餓神經細胞的下游是什麼?「雖然神經細胞最後是要傳送訊息到運動神經元、肌肉,但在這中間還有些複雜的東西,畢竟生物要面臨的事情往往不是那麼單純,像在一個危險環境中有食物,要不要過去找呢?大腦必須統合所有訊息,才能做出最好的決定。」 林書葦解釋。
沒料到一隻小小的果蠅,大腦卻比人類想像得還要複雜許多!目前大腦科學家積極想破解果蠅大腦的神經迴路機制與神經傳導物質等,一旦可以解開,「就像拿到習題的解答本,當我們碰到類似的問題,就可以去找到答案。」林書葦總結。大腦與神經的運作充滿奧祕,如同一間密室,而透過研究果蠅的大腦,一扇扇知識之窗正逐漸被開啟。
果蠅個頭小、腦袋更迷你,科學家如何觀察牠們的大腦變化?
問得好!如果把果蠅大腦想像成一塊電路板、每條神經都像一條電路的話,科學家想知道哪條電路是負責哪個功能,最好能幫每條電路做上不同的標記。
過去科學家想做神經細胞研究,通常是電極探針去測量細胞內外的電流變化,測量後再把染劑打進細胞裡,看看到底是刺激了哪一些細胞,比較複雜。後來因為遺傳學工具的大幅進展,目前可以標定出果蠅大腦的每顆神經細胞——讓細胞發光、在顯微鏡下無所遁形,研究起來簡單許多,稱為 GAL4-UAS 系統。
簡言之,GAL4(蛋白質)是從酵母菌而來的一種轉錄因子 (transcription factor ),科學家把 GAL4 的基因放到果蠅體內,並藉由改變 GAL4 基因的上游 DNA 序列,讓 GAL4 能在果蠅大腦不同的神經細胞中表現。這樣所產生的基因轉殖果蠅株,稱為 GAL4 line。UAS 則是一種特殊基因序列,當 GAL4 和 UAS 結合之後,它們可以驅動 UAS 下游基因的表現,比方說表現綠色螢光蛋白。
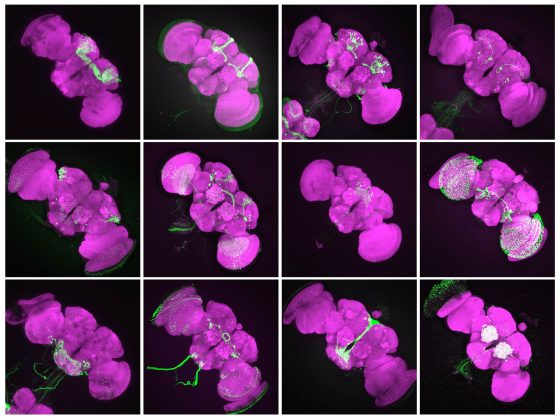
綠色螢光蛋白 (Green Fluorescent Protein,縮寫 GFP) ,是一種很方便進行基因追蹤與標記的工具,可以用來標記果蠅的神經細胞。舉例來說,如果公果蠅身上帶有標號 A1-GAL4 的基因,讓牠和帶 UAS-GFP 基因的母果蠅交配之後,子代同時帶有 A1-GAL4 和 UAS-GFP ,於是大腦中可以表現 A1-GAL4 的神經細胞,即可發出綠色螢光。
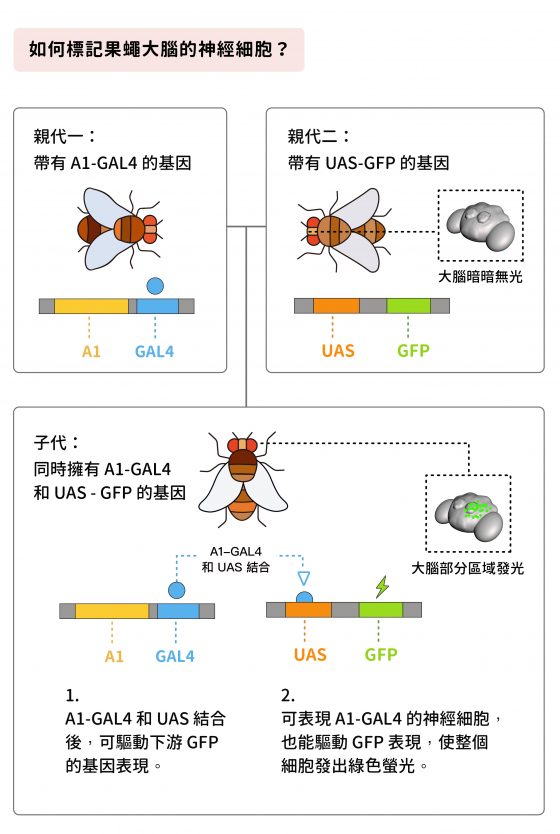
以此類推,帶有 A2-GAL4 的公果蠅和母果蠅交配之後,子代大腦中可以表現 A2-GAL4 的神經細胞會發光……。科學家透過不同種類的 GAL4 line、UAS 和螢光蛋白,將果蠅大腦的神經細胞全都做出標記。
目前科學家已經建立一萬多種 GAL4 line,每種 GAL4 line 都有它的名字,就像每個神經細胞都有代號,而且全球通用。如果我們跟人家說這個是 R58E02-GAL4 ,所有人都知道被標定的是哪些神經細胞。
幫大腦標好分區後,只要果蠅一行動,就能知道是哪些腦細胞控制嗎?
還沒還沒!在觀察每條神經負責什麼功能之前,科學家還需要一些其他的「工具」,能夠人為啟動或關閉特定神經細胞,才能確定這些神經細胞對於果蠅行為的影響。
例如:當表現 leucokinin 的神經細胞受到人為抑制、失去活性,果蠅的行為就會出現變化,即使是渴,也不會去找水;相反的,如果人為活化、刺激這些神經細胞,果蠅的行為會出現異常,明明已經喝很多水,還是會去找水,如此我們才能確認這些神經細胞與渴有關。
這類工具很多,如 Shibire 、TrpA 蛋白質, 它們對於溫度很敏感,Shibire 會抑制神經傳導物質的釋放、TrpA 則會刺激神經傳導物質的釋放。如果把 Shibire 接在 Gal4-UAS 系統的序列後面,然後將溫度升高,即可讓神經細胞失去作用;如果接上的是 TrpA ,將溫度升高時反而活化神經細胞。
還有像 CsChrimson、GtACR 蛋白質。CsChrimson 是一種陽離子通道,照射紅光時會打開,讓鈣離子等正電離子進入,造成神經細胞的膜電位上升,使細胞被活化。GtACR 蛋白質則是一種氯離子通道,照射綠光時會打開,讓帶負電的氯離子進入,造成神經細胞的膜電位下降,使細胞被抑制。
科學史上的重大突破,工具的進展往往是成功的關鍵。GAL4-UAS 系統等工具原理看似單純,但對於果蠅大腦研究影響甚鉅,足以促成當代大腦科學飛躍性的進展!

延伸閱讀:
- 林書葦個人網站
- <A neural mechanism for deprivation state-specific expression of relevant memories in Drosophila>
本文轉載自中央研究院研之有物,原文為大腦如何操控渴與餓的行動?小小果蠅來解密!,泛科學為宣傳推廣執行單位