繼 SARS 和 MERS 之後,引發武漢肺炎(WHO 定名為 COVID-19),致死人數已經超過兩位前輩的第三種冠狀病毒,國際病毒研究社群日前命名為 SARS-CoV-2,突顯它類似 SARS 的特色,也就是「SARS二世」;為方便閱讀,接下來本文提及此病毒,亦以「SARS二世」稱呼。
SARS二世從何而來,為什麼能感染人類?最近分子演化學方面又有新的進展。1
相關分子演化分析可參考前文:
武漢肺炎(即 COVID-19)為一快速變化的議題。最早由 WHO 暫定名為 2019 novel coronavirus,簡稱 2019-nCoV,中文「2019新型冠狀病毒」,但使用上相當拗口。因此本系列前面文章提及此一疾病與其病原,內文均簡稱為「WARS」,將 SARS 的第一個字 Severe 替換為 Wuhan。
本文內容豐富,先提示重點在此:
- SARS二世至少有兩處關鍵的遺傳變異,使其能有效傳染人類,其中一個變異已知存在於自然界。
- 沒有有力證據支持穿山甲為中間宿主。
- SARS二世很適應人體,但是無法確定是在動物,或是人類體內完成適應過程。
影響感染能力的關鍵位置,不照牌理出牌?
絕大部分冠狀病毒都不會感染人類,至今只知道 7 種有這個能力。除了 SARS、MERS、以及 SARS二世外,還有另外 4 種:HKU1、NL63、OC43、229E,不過它們只會小打小鬧,疫情都沒有前三種嚴重。
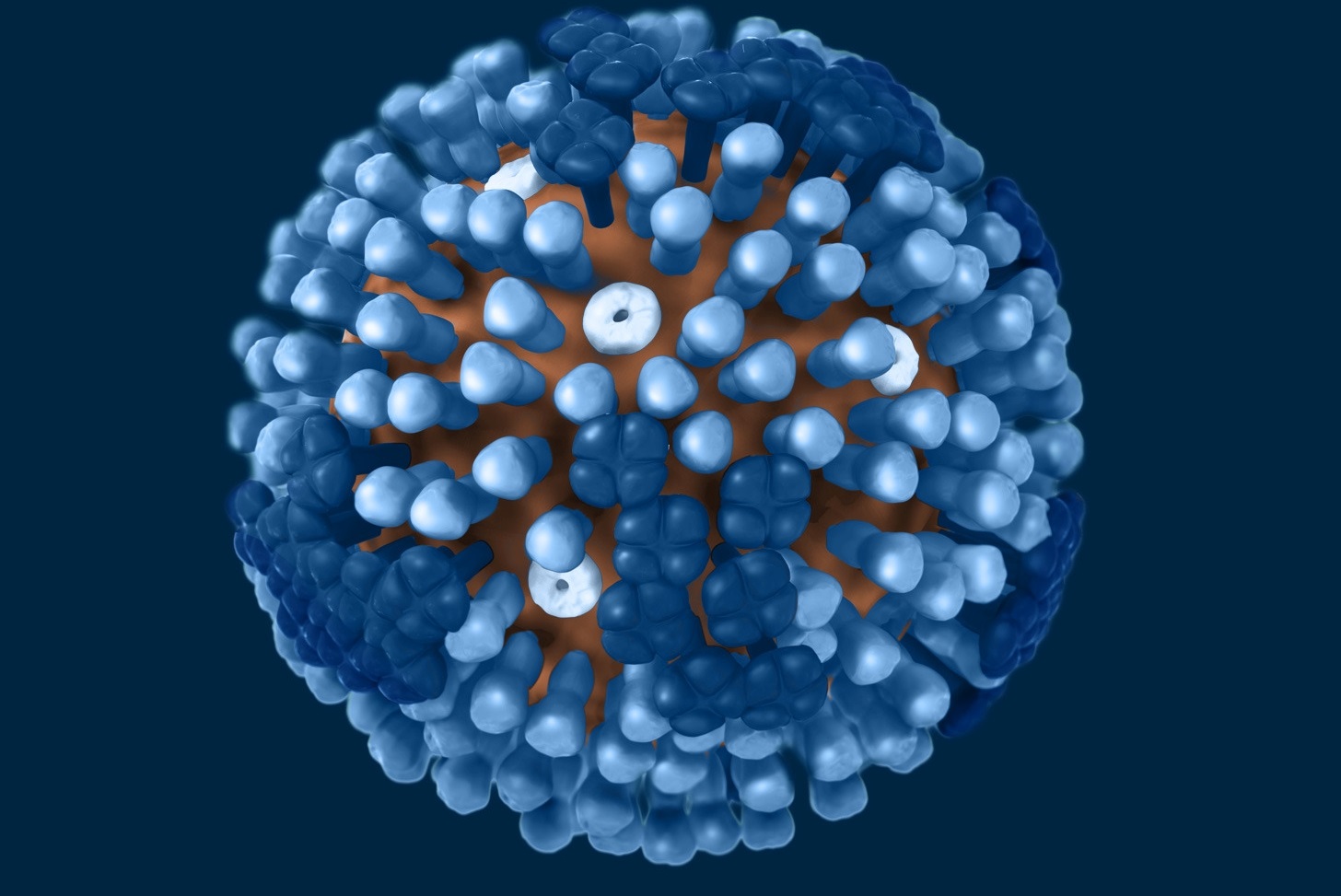
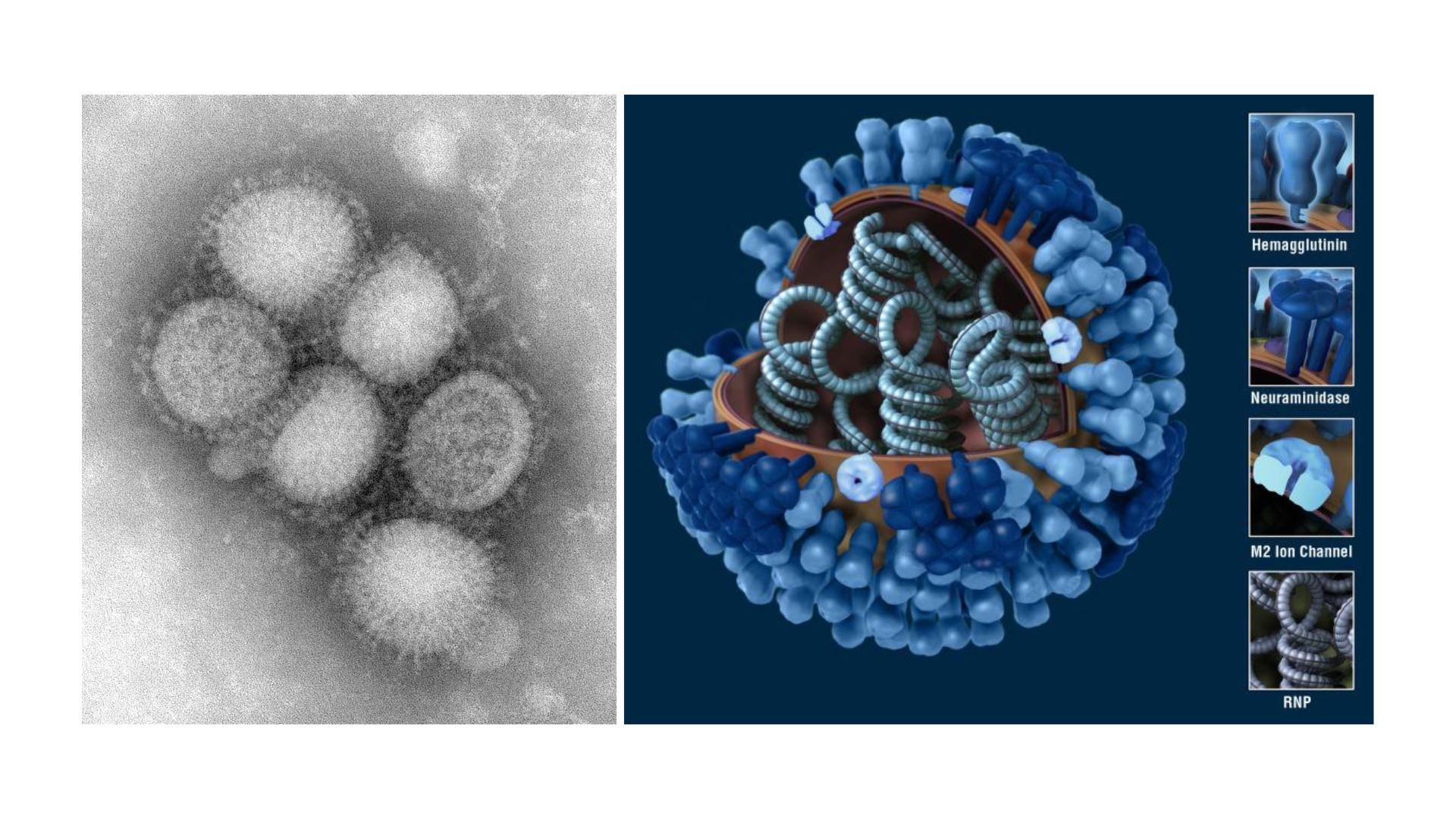
這些病毒感染細胞時,spike 基因的產物「S蛋白質」非常關鍵。S蛋白質會和宿主細胞的 ACE2 受器(angiotensin converting enzyme 2 receptor)結合,兩者的親和度,深深影響病毒的感染對象以及能力。
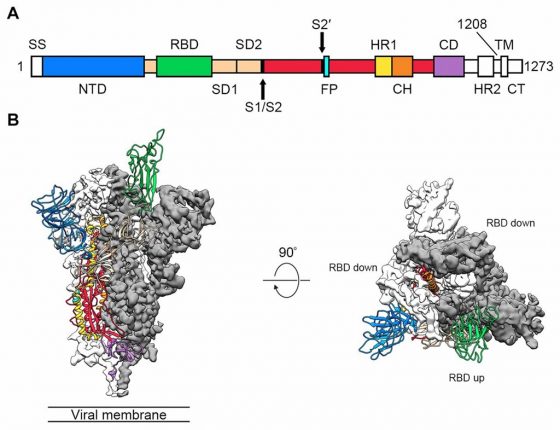
SARS二世的 S蛋白質和親戚相比比較特殊。S蛋白質可分為 S1 和 S2 前後兩部分,S1 上頭有一段約 200 個胺基酸長的序列稱作 receptor binding domain,簡稱 RBD,會直接與受器互動,對病毒感染細胞相當重要。
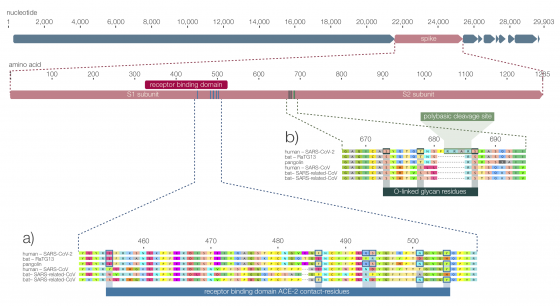
之前研究發現,SARS 這段序列上頭有 6 個位置的影響較大,分別是(字母是胺基酸、數字是 S蛋白質上的位置)Y442、L472、N479、D480、T487、Y491;而對應到 SARS二世的這 6 個胺基酸則是 L455、F486、Q493、S494、N501、Y505。
可以看出,儘管 SARS一世與二世皆以人類為宿主,整個基因組的相似度為 79.5%,兩者 6 個關鍵位置中卻有 5 處不一樣。至今已知遺傳上最接近的冠狀病毒是取自雲南蝙蝠的 RaTG13,整個基因組有高達 96.2% 一樣;然而,兩者這 6 個胺基酸中仍有 5 處不一樣。
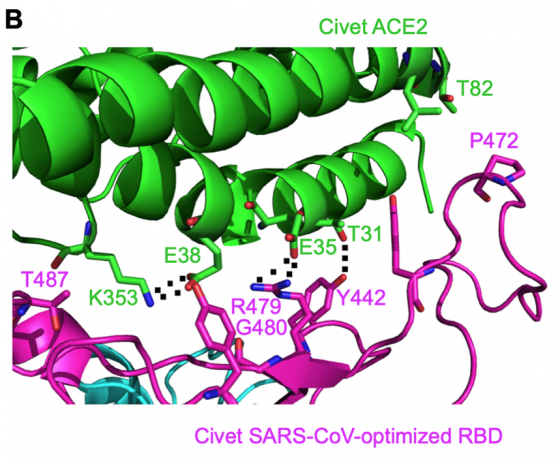
根據模型預測,除了智人以外,還有紅毛猩猩、猴子、鼬獾、豬、貓的 ACE2 受器與 SARS二世的親和性都不錯;與 SARS 的宿主果子貍卻沒那麼好,而不會感染 SARS 的小鼠、大鼠,其親和性都不佳。不過這只是電腦作業,不見得符合現實;SARS二世對動物的感染力究竟如何,仍需要實際做實驗才能證明。2
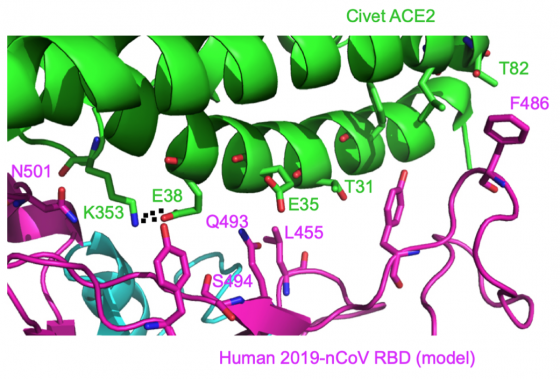
已經超過 7 萬人受到感染,這件事實告訴我們:它感染智人細胞的能力非常好。但是很有意思,根據人類對結構化學的理解,SARS二世關鍵位置上的某些變異,其實並非最佳選擇。也就是說,假如根據智人現有的理論認知去設計病毒,應該不會製造出這支病毒,因為理論上這些變異並不理想。
顯而易見,沒學過分子生物學、病毒學、結構化學、生物化學等智人學問的冠狀病毒:
在感染智人的演化適應之路上,沒有按照智人已知的牌理出牌,而闖出了一條自己的路。
武漢肺炎的傳播,和穿山甲有關嗎?
然而,SARS二世的 S蛋白質上特殊的 RBD,事實上並非獨一無二,2 篇尚未正式發表的論文報告,在取自穿山甲的樣本中也見到它,這又是怎麼回事!?

疫情爆發以來,研究冠狀病毒成為最熱門的顯學。一群科學家以鍵盤辦案,從過去發表過的資料庫中尋找冠狀病毒的蹤影,結果在 2019 年發表論文的一項資料庫,取自走私到廣東的 2 個穿山甲樣本中(可能原產於東南亞),偵測到類似的目標。3, 4
將定序片段拼裝起來得到的「穿山甲冠狀病毒」,整個基因組與 SARS二世的相似度為 90.5%;但是光看 S蛋白質的 RBD 上,第 435 到 510 共 75 個胺基酸長,最關乎親和性的 receptor binding motif(簡稱 RBM)部分卻有高達 98% 的胺基酸相似度(以及 89% 的核苷酸相似度)。更重要的是,上述提到的 6 個關鍵位置,穿山甲冠狀病毒竟然與 SARS二世完全一致!
差不多同時問世,另一尚未正式發表的論文,則是從 2017 到 2018 年查獲,冰在冷凍庫的穿山甲,總共 9 個樣本中偵測到冠狀病毒,而且順利取得活的病毒(活病毒這部分研究尚未發表)。這批病毒與 SARS二世的整體相似性介於 85.5 到 92.4%,RBD 卻有高達 97.4% 的胺基酸一致,關鍵胺基酸則通通相同。5
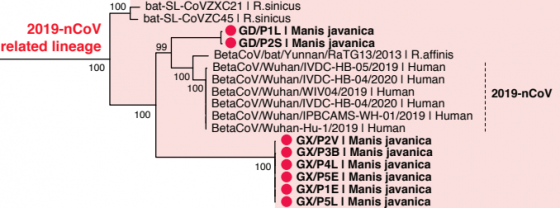
綜合上述發現可以確定,可能原產於東南亞而被走私到中國南方的穿山甲,有多隻個體感染冠狀病毒,而且病毒彼此間的遺傳不太一樣。由此推論,穿山甲感染冠狀病毒也許是長期而普遍的現象,而且這群病毒與宿主受器互動的關鍵位置,和 SARS二世極端相似。可是該如何解釋這個情況?
關鍵位置相似是由於遺傳重組,還是趨同演化?
儘管雲南蝙蝠的 RaTG13 整體遺傳上更接近 SARS二世,影響致病力的關鍵變異處卻和穿山甲的病毒一模一樣,對於這一點,兩篇論文的作者分別提出同樣的論點:這段序列,可能是與感染穿山甲的病毒親戚遺傳重組而來。
但是除了「遺傳重組」以外,很可能發生的「趨同演化」也能解釋這個情況。
這類與感染能力高度相關的序列,深受天擇影響,假如某種冠狀病毒的感染對象,其受器結構與人類類似,那麼在選汰壓力下朝向類似的序列改變,也就是台灣高中生都知道的「趨同演化」,只是剛好而已。
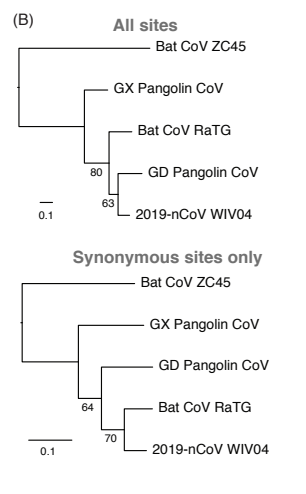
鍵盤辦案的研究分析中,可以發現兩者這部份的胺基酸序列有 98% 相似,但在核苷酸序列只有 89% 的相似度,暗示此處面臨強大的選汰壓力,使得即使核苷酸改變,也要維持胺基酸不變,也就是淨化選汰(purifying selection)──很典型取決於功能,而非親緣關係的特徵。冷凍穿山甲研究的序列分析,也高度支持趨同演化的可能性。
總之,兩群獨立的作者,似乎經趨同演化提出「SARS二世的祖先與穿山甲冠狀病毒經過重組」之論點,沒有充足的證據支持,明顯還有更合理的可能性。現在看來,要認識冠狀病毒的多樣性,必須重視穿山甲,不過要追尋 SARS二世從前的宿主,暫時不用特別考慮穿山甲。
不論穿山甲的冠狀病毒跟 SARS二世是否有直接關係,有一件事倒是非常清楚:
冠狀病毒與人類受器親和性高的遺傳變異,其實原本就存在於自然環境!
獨一無二的遺傳特徵,或許會讓致病力增強
SARS二世有一處變異倒是真的是獨一無二,沒有在已知病毒上見過(包括最近親 RaTG13 和穿山甲冠狀病毒),它位於 S蛋白質中央的 polybasic cleavage site(暫譯:多鹼基分割位點)。S蛋白質分為 S1 和 S2 兩個部分,在 SARS二世這中間多出了一小段「PRRA」的胺基酸,程式模擬指出,此一變化會明顯改變原本的蛋白質立體結構。值得一提,這也是之前被誤會為與 HIV 有關的 4 段序列中,SARS二世唯一真正與眾不同之處。
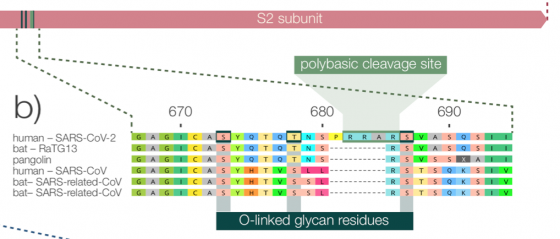
之所以值得注意,是因為流感病毒在對等的位置上,倘若發生類似的變化,會讓本來感染力微弱的病毒大幅強化攻擊力;另外導致禽鳥傳染病「新城病(Newcastle disease)」的病毒,此一位置改變也會讓病毒變得更加凶險。不過此處變化對 SARS二世會有什麼實際影響,無法光靠鍵盤辦案釐清,還需要更多實驗分曉。
如此適應人類,到底是如何演化而來的?
所有 SARS二世的基因組都非常相似,表示它們都來自非常近期的共同祖先。由序列差異估計,共同祖先的生日約為 2019 年的 11 月底到 12 月初(不同估計方式的結果不太一樣,不過第一位已知病患至少能追溯到 12 月 1 日),顯示 SARS二世在這個階段已經相當適應人類。
兩位前輩 SARS 和 MERS 的祖先都是感染蝙蝠的病毒,但是傳染給智人以前,SARS 的宿主是果子狸、MERS 是駱駝。從蝙蝠到智人的路上, SARS二世是否也有過類似的中間宿主?現在如此適應智人,究竟是在其他動物、或是智人身上修煉成功的呢?
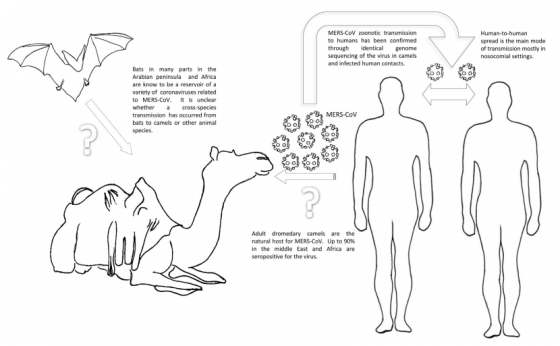
可能一:透過(未知的)中間宿主演化
一種可能是, SARS二世的祖先先以某種動物為宿主,在這種不是蝙蝠的動物體內,漸漸變得適合感染智人,真正跳到智人身上後隨即能無縫接軌。
這套劇本中,該動物宿主的細胞受器應該與智人相當相似,才能使之發展出對智人受器的高親和性。若是如此,族群數量較大的動物會是比較可能的中間宿主(例如鼬獾?),因為病毒能感染較多個體,更有利於天擇進行。
- 延伸閱讀:武漢肺炎當流感,傷害遠勝SARS
而數量稀少、瀕臨絕種的穿山甲,乍看不像適合病毒天擇作用的舞台。但是目前資訊非常侷限,沒有人知道真相。既然提到穿山甲,也順便請大家重視瀕危生物的保育 QQ
可能二:直接在智人體內完成升級?
另一種可能是, SARS二世早已能由動物傳染給人類,經歷一番掙扎以後才順利適應智人細胞,演化適應是直接在人類身上完成。

8 年前出道的前輩 MERS 就是走這套劇本,至今累積約 2500 個病例,不過到現在仍尚未「破關」,一直不算真正適應智人。主因是原本以駱駝為宿主的這款病毒,人傳人的能力整體不強,致死率又超過 30%,導致傳播很容易中斷,阿拉伯半島的疫情每次都要從駱駝重新開局。
MERS 難以融入智人的社會,也令它對人類的危害遠不及這次源自武漢的 SARS二世(謎之聲:瘟疫公司新手嘛)。如果 SARS二世也是如此起源,它顯然已經突破這道關卡,開拓出冠狀病毒的全新天地。
我們所知太少,需要更多資訊
根據現有證據,無法判斷哪套劇本才是對的,仍需要更多研究才有機會回答問題。例如可以從不同地區的各種動物與環境採樣,更全面認識冠狀病毒的多樣性;或是檢測人類血液對冠狀病毒的血清反應(seroreactivity),了解是否早已有人感染過冠狀病毒。
釐清 SARS二世的來歷與適應過程,不只有學術價值,也能提供我們相當實際的指引。畢竟這已經是本世紀第三起冠狀病毒暴走事件,而動物傳人的跨物種傳染病,一直都是人類的強大威脅,假如能及早預防,價值不遜於研發出新藥或疫苗。
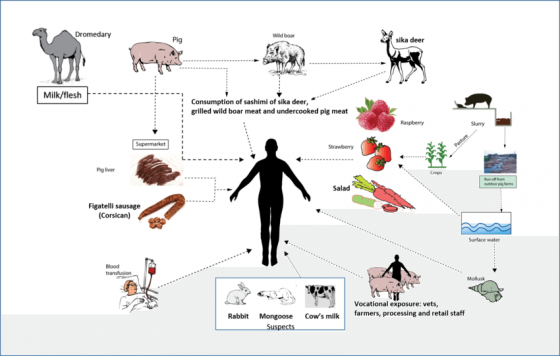
SARS二世的適應過程若是在動物體內完成,意謂控制住這次疫情後,未來類似的傳染病將很有機會再度出現,需要更全面的監測。如果病毒是在人類體內才升級成功,那麼即使時常發生動物傳人,在病原獲得適應人體的關鍵變異以前,都不需要太過擔心。
不論如何,一連串疾病帶來的教訓是:
我們必須更積極認識野生動物與生態環境,主動尋找潛在的風險。
另一方面,疫情蔓延時,也有許多 SARS二世經歷過人為操縱之類的陰謀論流傳,還有人懷疑武漢的病毒研究單位與疫情脫不了關係。對於 SARS二世是否經過人為變造這點,以斯克里普斯研究所(Scripps Research)的 Kristian Andersen 為首的研究團隊,抱持強烈否定態度,認為從遺傳序列上看不出人為介入的跡象。至於中國研究人員是否導致病毒外洩,沒有直接證據,當然無從證實或是推翻,說穿惹,這不是科學問題,無法以科學解答。
劃重點:
- SARS二世至少有兩處關鍵遺傳變異,讓它們能席捲人類。
- 其中一個變異本來就存在野外,穿山甲身上的病毒也有。
- 可是穿山甲和武漢肺炎多半沒有直接關係。
- 另外一個變異為 SARS二世獨有,具體作用不明。
- SARS二世很適應人體,但是不確定是在動物或人類體內升級完成。
- 未來要更積極注意野生動物,及早認識可能的威脅。
- 有陰謀嗎?隨便啦大家高興就好。
延伸閱讀
- 演化樹怎麼長出來,怎麼看?
- 用模型推疫情,如何避免誤用、正確解讀?
- 武漢肺炎恐在中國外廣傳,台灣需嚴陣以待
- 《瘟疫公司》:站在人類的對立面,思考傳染病這檔事
- 咖啡因生產線的趨同演化
- 從海洋移民到淡水的魚類,製造DHA的基因多更多!
- 曾經有50億鳥口的「旅鴿」,遺傳多樣性卻低得嚇死人?
參考文獻
- The Proximal Origin of SARS-CoV-2
- Wan, Y., Shang, J., Graham, R., Baric, R. S., & Li, F. (2020). Receptor recognition by novel coronavirus from Wuhan: An analysis based on decade-long structural studies of SARS. Journal of virology.
- Evidence of recombination in coronaviruses implicating pangolin origins of nCoV-2019
- Liu, P., Chen, W., & Chen, J. P. (2019). Viral Metagenomics Revealed Sendai Virus and Coronavirus Infection of Malayan Pangolins (Manis javanica). Viruses, 11(11), 979.
- Identification of 2019-nCoV related coronaviruses in Malayan pangolins in southern China
本文亦刊載於作者部落格《盲眼的尼安德塔石匠》暨其 facebook 同名專頁。