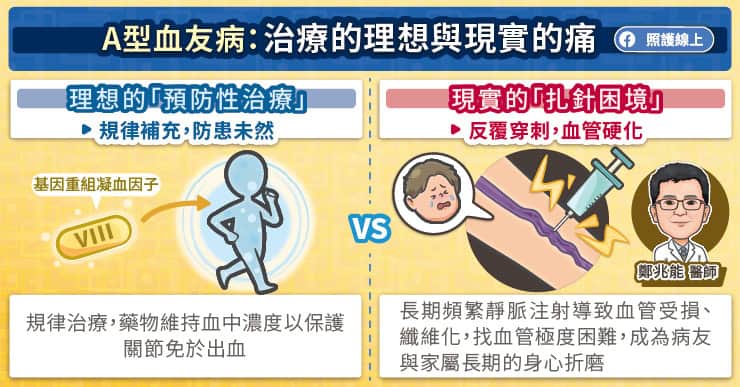
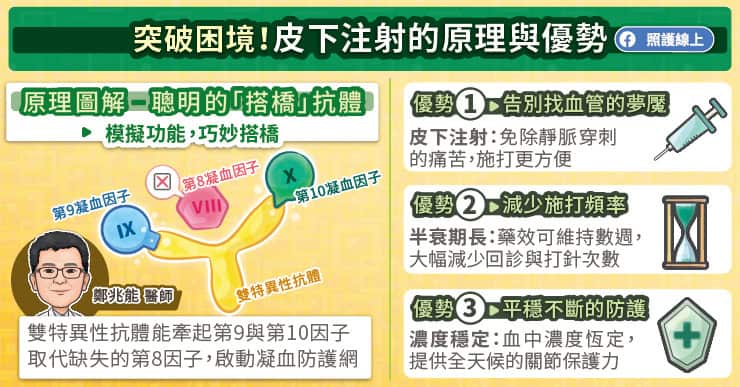
DNA 是由四種核苷酸 A、C、G、T 所組成,這四個「密碼」的排列順序也蘊藏遺傳的訊息。這些訊息需先轉錄成 RNA,再編輯轉譯成蛋白質,才能運作生命機制。
為何某些有害突變能在演化中保存至今?
過去相關研究在討論基因突變的致病性時,未曾考慮過 RNA 編輯機制的影響。
近期,中央研究院基因體研究中心莊樹諄研究員團隊,將生物資訊結合大數據分析,探討「A-to-G RNA編輯 (RNA editing) 機制」註1與基因突變的關係——「在判斷基因突變的危害性時,也應考量 RNA 轉錄資料」。
莊樹諄表示,A-to-G RNA 編輯機制的正常與否,和自閉症、癲癇及阿茲海默症等複雜的神經疾病有密切相關,此研究結果將有助於瞭解相關疾病,可望減少探討基因突變時對其致病及危害程度的誤判。此研究已於今 (2019) 年 9 月發表於《基因體研究》(Genome Research)。
「RNA 編輯機制」 是豬隊友還是神救援?
基因突變即是基因中的 A、C、G、T 排列發生變異。
如果某個位置本應是「A」,卻變成「G」,即是發生「A/G 點突變」。如果突變發生在重要的基因位置,影響到後續產生的蛋白質功能,便會對生命體造成危害。而 A-to-G RNA 編輯機制可以在 DNA 轉錄成 RNA 時,將RNA中的「A」,轉換成「G」。
莊樹諄因此好奇,這套機制對 DNA 上的 A/G 基因突變而言,究竟是提油救火的「豬隊友」,還是雪中送炭的「神救援」?
他大膽假設:A-to-G RNA 編輯機制,可使某些 A/G 點突變的危害性下降。
研究團隊首先整合了 447 位不同人類個體的 DNA 及 RNA 序列資料,進行大數據統計與演化分析,並評估 A/G 點突變的危害程度、在群體中的發生頻率,及其與 A-to-G RNA 編輯機制間的關係。接著,再深入分析「千人基因體計劃」(1000 Genomes Project) 蒐集到逾 2000 人的 DNA 序列資料後證實:
A-to-G RNA 編輯事件確實和 A、G 兩種核苷酸的發生率有關,尤其當 A/G 點突變所造成的危害越大,相關性就越大。
RNA 編輯機制與基因突變的關係
分析結果顯示,基因突變危害的程度跟 A-to-G RNA 編輯機制密切相關:
- 當 A 突變成 G (A→G),而且這樣的點突變有害時,A-to-G RNA 編輯機制便會受到抑制;而當 G 突變成 A (G→A),且突變有害時,該機制的發生率則明顯提高。
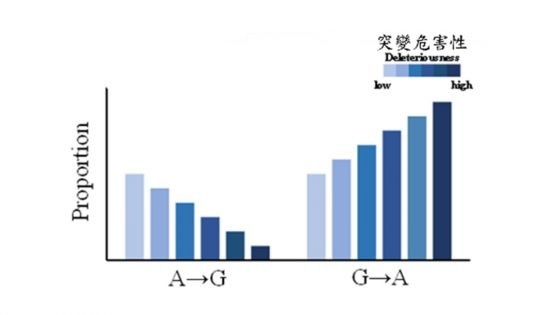
- 當 A→G 突變越有害,該突變的所佔比率就越低;而當 G→A 突變越有害,G→A 所佔比率則越高(下圖)。
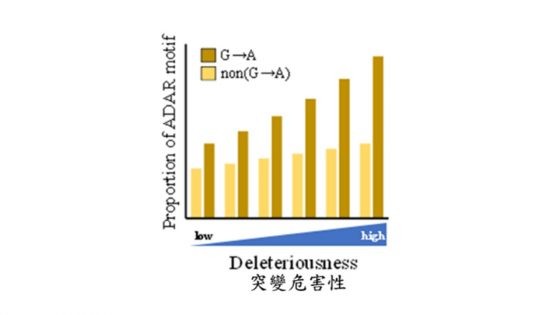
當錯義突變越是有害時,A→G 突變所佔比率越低,而 G→A 突變所佔比率則越高。圖/中研院提供 - 經由 A-to-G RNA 編輯機制的辨識序列 (ADAR motif)註2 分析顯示,若 G→A 突變發生在 DNA 的位點越重要,亦即該突變越危害,則該點發生 A-to-G RNA 編輯機制的可能性也會越高 (下圖)。
圖二、A-to-G RNA 編輯機制的辨識序列 (ADAR motif) 出現率和突變危害程度的比較。圖/中研院提供
從以上結果可推測,當 A→G 突變對生命有害時,生命體就降低 A-to-G RNA 編輯機制發生率,以減少A變成G;相反地,如果造成危害的是 G→A 突變,A-to-G RNA 編輯機制就可能會「神救援」,把原本有害的 A,回復為 G。
莊樹諄表示,本次研究成果有賴大數據、生物資訊與堅實的演算邏輯推導(下圖)。
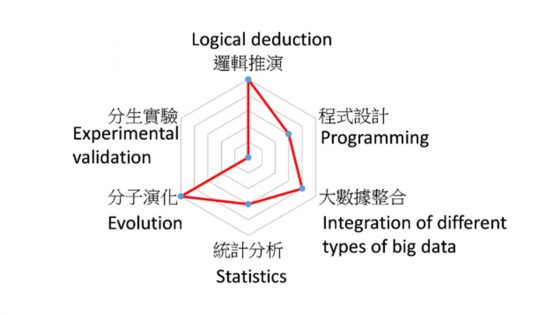
在人類 DNA 序列上 30 億個鹼基被解碼之後,科學家得以藉此探索人體內各種生命機制的變化與 DNA 之間的關係。這些大量且多樣的定序資料,若經過大數據的處理,可以協助醫療診斷的判讀,因此,生物資訊分析愈形重要。

- 本文改寫自中研院新聞稿,原標題為〈大數據看出端倪 基因突變的豬隊友神救援〉。
論文:《A-to-I RNA editing contributes to the persistence of predicted damaging mutations in populations 》 - 此論文成果於 2019 年 9 月發表於《基因體研究》(Genome Research)。
- 本論文第一作者為基因體研究中心麥德倫博士。
註解:
- A-to-G RNA 編輯事件常見於多細胞生物,其功能造成的影響是好是壞在學界仍有爭議。它一方面有機會增加序列多樣性,讓蛋白質產生新功能,另一方面也可能使蛋白質功能受損而導致「錯義突變」。許多研究顯示,這個機制的失調和自閉症、肌萎縮側索硬化症、顛癇、阿茲海默症等神經疾病有關。莊樹諄團隊除了開發新的 A-to-G RNA 編輯事件尋找方法 (ICARES) 之外,也對 A-to-G RNA 編輯事件在不同多細胞動物間做了廣泛的探討。(詳見 2018 年發表在 Genome Biology and Evolution 的論文:https://academic.oup.com/gbe/article/10/2/521/4774976)
- A-to-G RNA 編輯機制是透過「ADAR 蛋白質」得以運作,而本分析即是透過 ADAR motif 來預測 A-to-G RNA 編輯機制是否發生。