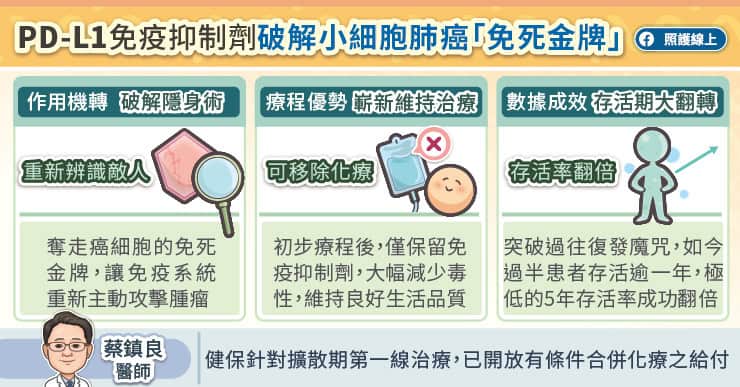
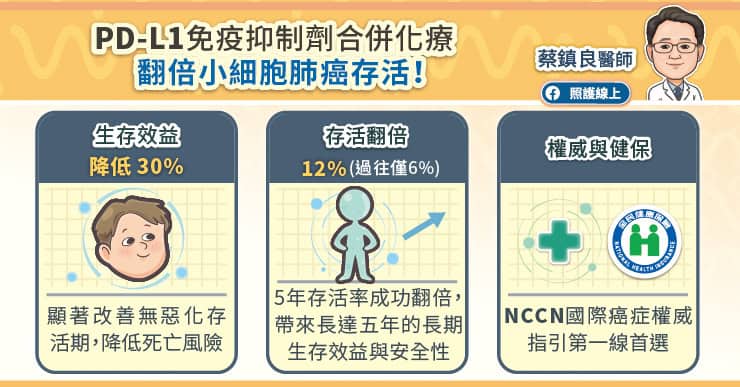
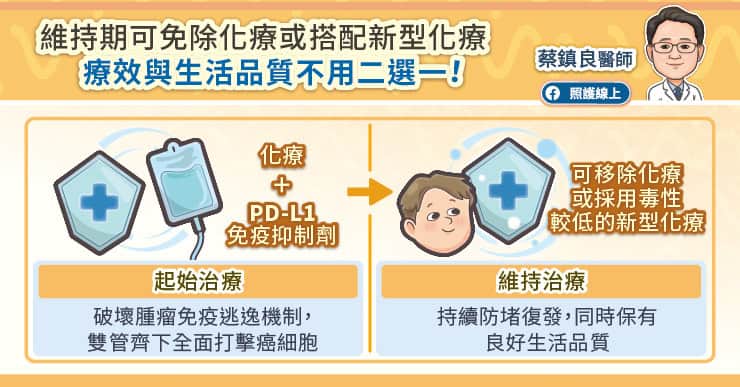
前一陣子有很多食安問題,像是食品添加物超標、輻射超標、空氣汙染超標⋯⋯你所能想到可以超的標都超了,這時候少不了的就是「震怒」、「痛批」、「恐致癌」之類的戲劇性字眼。在林林總總的食安問題中,也曾發生日本食品進口的問題,電視上某位「良心立委」揭露某些食品進口商偽造(或是未標示清楚)食品生產地,導致福島災區食品流入市面,民眾食毒而不自知,左批政府管制不嚴,右批進口商黑心無良,最後眼角帶點憤怒、混著悲天憫人的淚水高喊「不信公義喚不回」,呼籲民眾一定要一起抵制黑心、支持良心(的立委,就是我本人)。通常民眾看到這種場景都會覺得非常感動,沒想到在這個亂世中,居然有一位出淤泥而不染的良心政治家守護我們的健康⋯⋯接著進入政治操作的層次這裡就不多談了。
「超標」的迷思
回歸到科學的問題,什麼是「超標」?政府是依據什麼訂定標準?超標就會死嗎?如果連這些都沒搞清楚,我們根本無法了解現在的法規究竟是「視民如親」,還是「作繭自縛」。
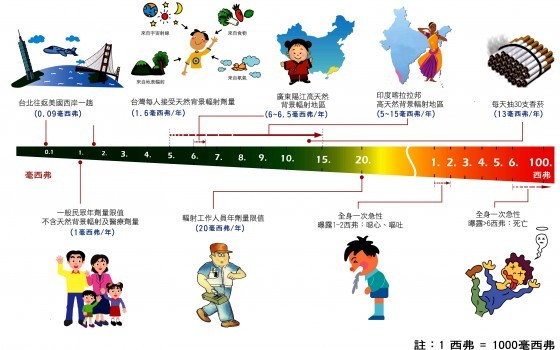
《游離輻射防護安全標準》對於輻射場所工作人員的規定(每連續五年週期之有效劑量不得超過100 西弗,且任何單一年內之有效劑量不得超過 50 毫西弗。)原則上是參考1990 年國際輻射防護委員會發布的第 60 號報告書所制定的,細讀一下會發現,輻射工作者的年度劑量容許值是一般民眾(有效劑量不得超過 1 毫西弗)的五十倍,難道說有受過輻射專業訓練的人體質比較好,比一般人更耐輻射曝露嗎?
首先要思考輻射工作者的規定是哪來的?我們都知道,所有的工作都有死亡的風險,不管你是開計程車、打籃球,還是當總統,都有「因工殉職」的可能性(機率大小是另一回事),當然,擔任輻射工作人員也可能會因為工作而死亡,因此國際輻射防護委員會所建議的劑量限值是參考一般性工作的職災身故機率,然後將輻射限值設定在風險相當的劑量值。如果輻射工作者在這樣的限制之下,最壞的情況也就和其他的工作差不多而已,事實上這可說是一條「極度安全的線」,因為我們現在都非常清楚,在短時間內接受低於 100 毫西弗輻射曝露的人身上幾乎看不到任何的生物效應,如果低於 50 毫西弗當然也是看不到,更別提從來沒有人在年劑量 260 毫西弗的伊朗拉姆薩觀察到居民有任何異常的生物效應了。
單次曝露劑量與累積劑量
目前我們手中的輻射劑量與生物效應的資訊來自於廣島、長崎原爆,而原爆造成的輻射曝露是非常短時間之內所發生的,因此有一個問題一直困擾著我們,那就是:「雖然短時間之內曝露 100 毫西弗以下,並沒有顯著性風險,但是長時間累積到 100 毫西弗以上的話,會不會有相當於短時間曝露的風險?」世界衛生組織底下的國際癌症研究機構(International Agency for Research on Cancer, IARC) 在 2015 年引述他們發表在英國醫學期刊、針對核電廠工作人員的三十年追蹤研究指出,雖然長期累積劑量低於 100 毫西弗的劑量仍無顯著性,然而我們仍需要注意累積劑量可能產生與短時間曝露類似的癌症風險。事實上 IARC 的這份研究報告爭議很大,因為從資料中顯示,即使是在累積高劑量的群體中,信心區間都不及一般公認的95%。不論如何,至少從這個研究當中知道,不論是短時間或累積曝露,低於 100 毫西弗的劑量都不具臨床意義。
說到這裡就不得不提日本發生的一件職災申訴案例。有一名東京電力公司雇員曾經在東日本大震災後於福島第一核電廠的三、四號機周邊(發生事故的是一號機)以及玄海核電廠擔任作業員,不料離職後經醫師診斷罹患急性骨髓性白血病,於是他就向政府提起職災申訴。日本的勞動標準監督署(類似我們的勞動部)展開一連串的調查後,最終認定這是一個「職災事件」。國內一些媒體就以「日本政府終於承認福島核災輻射致癌」做為標題報導這件事情。我當時看到這個報導標題的第一個反應就是:「劑量是多少?」於是我查了日本媒體的報導,發現該作業員在兩年間職場生涯所接受到的輻射曝露不到 20 毫西弗,然而在學理上要在短時間內接受高達 500 毫西弗的曝露才有可能導致急性白血病,難道這位作業員打破科學知識之壁了嗎?
當然不是。真相是「日本政府並沒有承認福島核災輻射致癌」,日本在 1976 年訂定了一個「放射線業務勞災的規則」,只要符合(1)一年被曝露 5 毫西弗以上,(2)在工作時被曝露後超過一年以上患病,(3)排除其他除了放射線以外的患病理由,可以被認可為勞災。
因此日本厚生省(類似我們的衛福部)真正在記者會上所說的是:「這次的認定『並不是』從科學證明被曝與健康影響的關係,一年 5 毫西弗以上的曝露也不是白血病發病的門檻,以保險精神的角度而言,並沒有任何需要補償的地方,然而 1976 年訂定的規則是依照一般民眾年曝露限值5 毫西弗而決定的。」也就是說,這個認定純粹是跟著法令走,並不是什麼科學新發現。
從這些事件裡,我們會發現一件事情,那就是法規通常都是比較嚴格的,甚至有時候並沒有什麼科學道理可言,因為我們通常希望防範始於未然,所以會把「那條線」訂在「絕對不會發生意外」的範圍內,這樣才能讓我們不小心越過那條線時還有補救的空間。當我們讀到一則輻射相關報導時,一定要有立刻有「劑量是多少?」的敏感度,不然會很容易陷入「超標恐○○」的迷思,然後就被那些靠煽動帶風向的人給騙了。
「超標」不等於危害,關鍵在劑量。
最受大家__的台灣鯛民來啦!
.只要是插電或裝電池的東西都有輻射?
.微波爐加熱的食物吃了容易致癌?
.用手機上網的人容易腦殘?
本書以輕鬆有趣的方式講述有關輻射與放射線的基本知識,各篇均輔以幽默插圖和清晰易懂圖表,讓讀者對日常生活中與輻射相關的事物能有正確的認識,並能因了解真相而得以安心。