文/廖英凱
「放射線治療」是個在今日醫學界被廣泛使用的醫療技術。從最常見用於診斷用的X光、核磁共振,到利用游離輻射體外照射或是體內植入核種暴露。特別是在今日癌症的治療上,放射線治療已能有效縮小癌細胞,提升外科手術的成功率。我們可以很輕易地想像,大部分的癌症腫瘤都在身體內部,因此透過體外照射的方式,接收到最多游離輻射的往往是表面的組織,而非真正需要消滅的癌細胞。因此,如何讓能放出游離輻射的「藥物」能精確地放在體內癌細胞的附近,如何讓這些藥物能傳達適當劑量的輻射,以及確保這些藥物不會有過多的副作用,就是放射線治療當前的研究重點。

今日,核能研究所的李德偉博士及其團隊,目前正陸續成功開發出用於治療腫瘤的放射性藥物。核能研究所位於桃園龍潭,是隸屬於行政院原子能委員會,專責各項與核能、能源和輻射應用、放射治療有關的研究機構。李博士目前針對癌症中排名第二高的肝癌,開發出188Re-HSAM,做為治療肝癌的藥物。188Re-HSAM分由三個部分組成,分別為能放出游離輻射的「核種188Re」、利用配位共價鍵與核種結合的「人類血清白蛋白微球體」(human serum albumin microsphere, HSAM),以及能將兩者順利結合的「配方緩衝劑」。
在核種的部分,188Re有一些很適當的特性能作為放射線來源。它的半衰期為17小時,因此在體內衰減的時間快。且188Re能放出兩種游離輻射,分別是能量為155KeV的γ射線和能量是2.1MeV的β粒子。γ射線的能量低,且能夠穿透人體,因此醫生可以藉由從體內射出的γ射線來分析腫瘤的所在位置與狀況,也由於放射線同時對所有細胞都有影響,因此先透過低劑量低能量的投藥來觀察,依據病患腫瘤與正常組織比例、肺分流百分比、肝功能及腫瘤大小來訂定最佳劑量,以確保對癌細胞的劑量是對正常細胞劑量的一倍以上,是作為治療前期的精確診斷。
而藉由γ射線的前期分析結果,接下來就能提高劑量利用能量較高的β粒子來消滅癌細胞。與γ射線能穿越人體不同,β粒子是高速運動的電子,僅能穿透人體組織平均0.25公分,因此β粒子所攜帶的能量,就會完全被人體組織所吸收,達到消滅癌細胞的功效。再考量到原料的來源,188Re的半衰期短,自然無法從國外進口,需要有相關核能工業的配合。而李博士所採用的188Re,可利用「發生器」內的188W(半衰期69天)衰變而來,為核研所能自行製造量產。相較其類似的核種,如半衰期90小時的186Re,就需要從核反應爐中取得,除須配合反應爐的安全管制,製造步驟也較為繁瑣。雖然母核種188W也必須取自核反應爐,但由於半衰期長,所以可以減少反應爐內作業的頻率。

在核種確定後,李博士選定了HSAM作為攜帶核種的藥劑。早年的體內放射線治療,多是利用植入膠束、導管或金屬片在患部。這樣的缺點是植入取出過程的手術會對身體有害,且當癌症腫瘤過於分散的時候,會大幅提高植入難度,而異物在身體內也會對病患造成不適。而HSAM是一種胜肽化合物,他能在人體內被自然降解而不留下殘留物。再搭配「肝動脈栓塞手術」,讓188Re-HSAM能被聚集在動脈與微血管的交界處。這是利用HSAM的直徑約20μm大於微血管的直徑6~9μm的特性。因此利用肝動脈導管,將藥劑注入供應肝臟癌症腫瘤養分的血管中,並因無法通過微血管而被截留,就能以近距離由內而外給予有效的高輻射劑量殺死腫瘤。
總括今日對於癌症治療的方式,體外放射治療受限於腫瘤數量、體積與腫瘤深度。體內放射物植入有異物不適感且無法應付過於分散的癌症腫瘤。而以肝癌來說,傳統化學治療在目前約可使10~30%晚期肝癌病患的腫瘤明顯縮小,但卻無法使病人在化療後得到存活的優勢。這是因為肝癌細胞本身的抗藥性,加上患者肝功能低落時更難承受化療藥物的副作用。而核研所李博士所開發的188Re-HSAM,結合既有低風險的手術技術又能避免化療副作用,並對腫瘤細胞做精確診斷與治療。在近年來,也開始有越來越多醫生採用核醫藥物作為診治的方式。李博士表示,近期核研所自行研發的核醫藥物,在腫瘤抑制上已取得非凡的成果,未來搭配既有的外科技術與化療,希望能對癌症的治療上,能有更多的突破與助益。
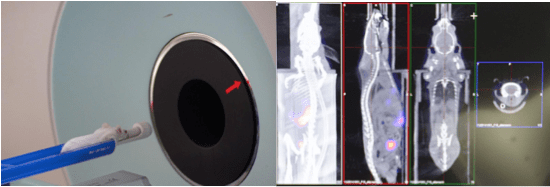
從核反應爐的產物,到注射物身體內的藥物。李博士的團隊也匯集了原子科學、分子生物、動物與生命科學等人才,並與醫學界和藥廠合作,從核種的試驗到藥物的合成,從動物試驗到人類臨床。對於生技醫藥產業尖端研發並不蓬勃的我國來說,李博士仍滿懷使命感地說:「事在人為,不做一定失敗,做了還會有成功機會」,相信在不久的將來,這項成功的技術,將成為人類維繫健康減少病痛的新希望。
更多資訊請參考解密科技寶藏