
瑪麗亞.斯克沃多夫斯卡-居禮(Maria Skłodowska-Curie,1867-1934),看姓氏不難聯想到,她就是我們所熟知的居禮夫人。她開創了放射性理論,發明分離放射性同位素技術,以及發現兩種新元素,是第一位獲得諾貝爾獎的女性,也是首位獲得兩座獎項的學者,在科學上的貢獻對後世影響深遠。

艱難困苦的童年
瑪麗生於波蘭華沙的書香世家,排行老么,家中有布朗斯拉娃(二姐)與索菲亞(大姐)兩位姊姊。父親是一名中學老師兼理事,母親原為一名校長,祖父亦是位受人尊敬的數學與物理教師。
當時的波蘭已被俄羅斯帝國佔領,在沙皇的統治下,波蘭人民的生活處處受限,也影響了瑪麗一家的命運。瑪麗的父親因濃烈愛國精神而被俄國上司打壓,校方撤除了他的理事一職,並將他們全家趕出宿舍;加上雙親的家庭參與波蘭獨立民族起義,家中又遭遇投資失利,經濟頓時陷入困境。
隨後瑪麗一家搬進廉價的住所,父親為貼補家用便招收了多名寄宿生,平時除供應食宿外,從學校下班後還替他們補習來賺取更多收入。生活看似漸漸好轉,但遺憾的是,短短三年內瑪麗的大姐及母親皆因病去世。
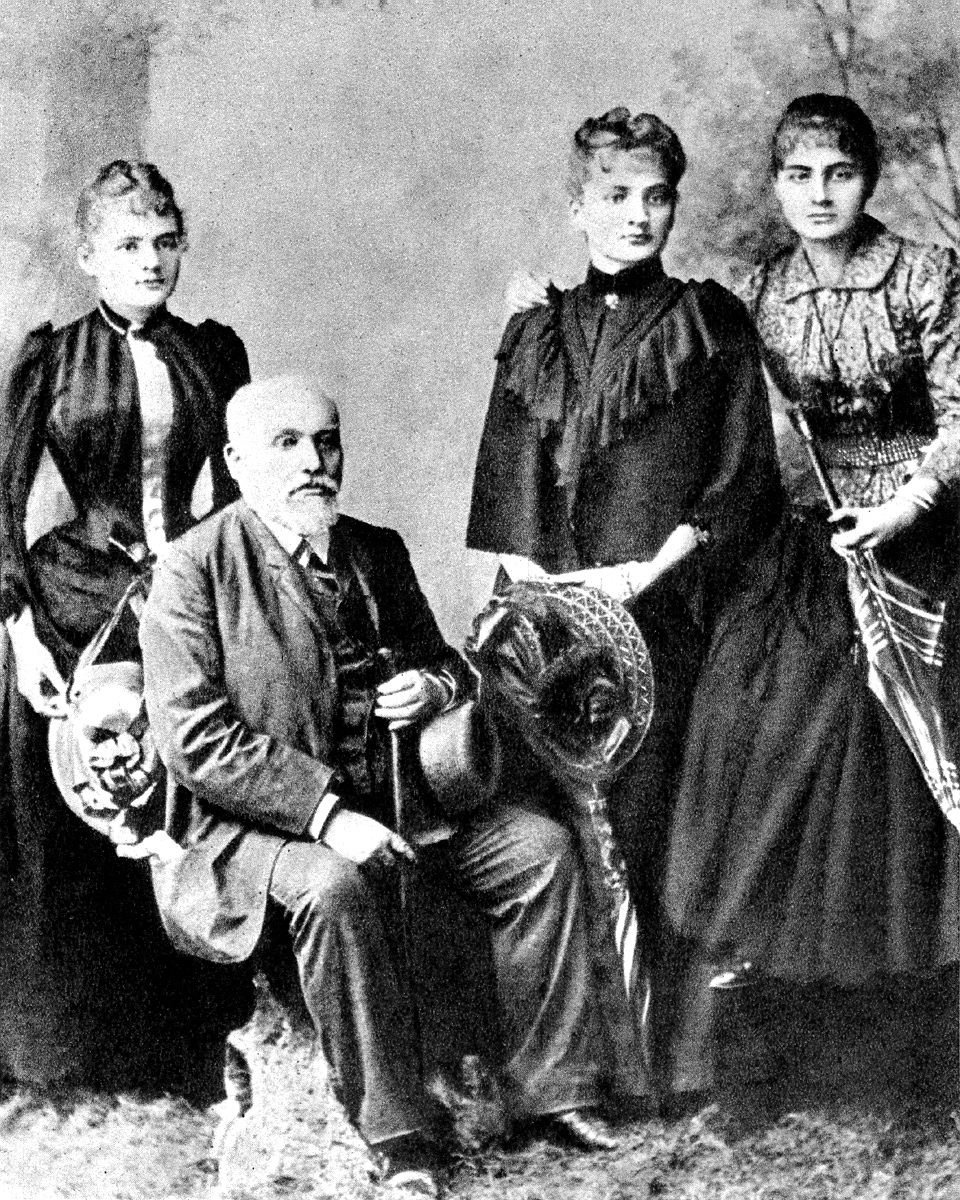
因性別在求學路上受阻
天資聰穎的瑪麗亞自幼就是個相當用功的學生,尤其在數理方面更是表現亮眼;在她 15 歲那年,便以第一名的成績從女子文理學校畢業。
然而,因當時波蘭的正規高等院校拒收女性學生,波蘭女子若想繼續接受正規的大學教育,唯一一條路就是出國留學,但這對瑪麗家中的經濟條件而言,是筆相當大的開銷且難以負擔。
成績同樣優異的二姐曾想過前往巴黎學醫,夢想成為一名懸壺濟世的醫師,但礙於家中經濟狀況遲遲無法如願。瑪麗想幫姐姐盡早完成學業,決定先當家教來資助其學費,兩人也約定,待畢業後再協助瑪麗出國求學。在瑪麗的支持下,二姐終於得以前往巴黎一圓醫師夢。
爾後的幾年,瑪麗一面做著家教工作,一面自學,期間閱讀了大量化學相關書籍,也是在這時獲得了第一份實驗室工作機會,這消息對她相當振奮;儘管實驗室設備簡陋,但能把在書中讀到的知識親手實作就已心滿意足,此經歷也影響了她未來將走上科學研究這條路。晚年瑪麗回憶起這段的時光:
「就是因為這第一次的實驗室工作,使我肯定自己在實驗研究上的興趣。」
突破重重阻礙取得學位
1891 年,24 歲的瑪麗在進行實驗室工作的同時,也終於踏上留學路,前往巴黎大學修讀物理學。剛到巴黎的她人生地不熟,對語言不熟悉外,又因過往在波蘭所受的教育無法應付大學課程,初期學業表現遠遠不及同儕。瑪麗便在課業上下足功夫,閒暇時間也都泡在圖書館裡,終於皇天不負苦心人,靠著清晰的思維加上勤奮苦讀,成績漸漸有了起色。
1893 年瑪麗以第一名的佳績成功取得了物理學碩士學位,原先是想再取得一個數學學位,但此時她已將留學用的積蓄花光,也就放棄了這份念頭。幸運的是,在友人的協助下,華沙當局頒發給瑪麗海外優秀留學生「亞歷山大獎學金」,使她得以重返巴黎大學繼續深造,並在隔年順利取得第二個碩士學位。值得讚揚的是,在畢業的幾年後她將這份獎學金歸還給委員會,這舉動令人相當震驚,從未有任何一名學子歸還過,而瑪莉是第一位。
科學界的佳偶——居禮夫婦
學成後,瑪麗留在法國並開啟了她的科研生涯。當時為了能夠順利進行工作,正尋找著合適的實驗室;在同鄉物理學家約瑟夫.科瓦爾斯基介紹下,她結識了未來的丈夫,法國青年科學家——皮耶.居禮。對科學滿懷熱情的兩人情投意合,彼此欣賞著對方的個性及才華。
1894 年,瑪麗返回波蘭生活,原以為能在家鄉繼續從事喜愛的科研工作,然而波蘭的大學仍以性別為由將其拒絕。在皮耶的說服下,瑪麗回到巴黎並協助他完成了磁性研究,兩人也在同年結為連理。
當時總有人打趣得說:「皮耶最大的發現就是瑪麗」。

帶領科學邁向新篇章
婚後夫婦倆一面養育女兒,一面做科研。瑪麗首要目標就是取得博士學位,她選定了當時剛發現的X射線以及鈾射線作為研究主題。後續在研究鈾礦時,透過驗電器的測量結果,瑪麗推斷鈾礦必定含有其他活性比鈾大的物質,於是開啟了她尋找其他放射性物質之路。
皮耶對瑪麗亞的工作越來越感興趣,隨後也加入了太太的行列。他們用酸液分解研磨過的瀝青鈾礦,再用化學分析方法分離出瀝青礦中可能含有比鈾更具放射性的物質。不久後,成功從實驗裡發現了比鈾的活性高 300 倍的新元素。隨後居禮夫婦發表了一篇聯合署名論文,正式宣布以「釙」(Polonium)命名所發現的新元素,以紀念波蘭。
在發現釙之後不久,她從實驗中發覺似乎有更強烈的放射性物質,便認定這也許是另一個新元素,這時物理學家亨利.貝克勒也加入了居里夫婦的研究行列。他們終於找出這個放射性比鈾大 900 倍的物質,三人將新元素命名為「鐳」(radium),拉丁文意為「射線」,也在研究過程中創造出單詞「放射性」(radioactivity)。
在當時居禮夫婦聯合及單獨發表的 32 篇論文中,其中一篇就為:在鐳輻射下,病變或腫瘤細胞比健康細胞死得更快。可說是若沒有這份的研究成果,就不會有現在用來治療癌症的放射性療法了。
得來不易的諾貝爾獎
在一系列研究及發現後,1903 年瑪麗終於獲得巴黎大學物理博士學位。同年瑞典皇家科學院授予居禮夫婦及亨利.貝克勒諾貝爾物理學獎,起初委員會僅表彰皮耶和貝克勒,不過有位倡導女性科學家權利的委員通報並向上申訴,瑪麗亞才能獲得提名,成為了首位獲得諾貝爾獎的女性。

隨著瑪麗亞成功從金屬中提煉出鐳,1911 年瑞典皇家科學院授予她第二座諾貝爾獎(此次為化學獎),以表彰:「發現了鐳和釙元素,提煉純鐳並研究了這種引人注目的元素的性質及其化合物」。此次的獲獎肯定也使她能夠說服法國政府支持並建立鐳研究所,該研究所於 1914 年建成,研究領域涉及化學、物理、醫學等。
將自己毫無保留地貢獻給科學與社會
一戰期間瑪麗為協助戰地外科醫生,便在靠近前線的地方設立了戰地放射中心。她的身影穿梭在戰地醫院中,指導著 X 光裝置的組裝及使用,據估計,超過 100 萬受傷士兵受過她的流動式 X 光機治療。

在戰後的歲月裡,瑪麗亞將時間奉獻將所學與經驗傳授給學生,也包括許多遠從世界各地慕名而來的後進學者。在她的指導下,鐳研究所培育出了四位諾貝爾獎得主,女兒伊倫.約里奧-居禮及女婿弗雷德里克.約里奧-居禮也在其中。
1934 年,瑪麗亞因再生不良性貧血逝世於療養院,後世普遍認為是因長時間暴露於輻射中而造成的,當時科學上並未了解到游離輻射會對人體產生危害,也未開發任何防護措施。瑪麗亞的生活處處充滿放射性物質,幾十年間患上了多種慢性疾病,然而一直到去世,她從未意識到這會危及自己的健康甚至是生命。
瑪麗亞.斯克沃多夫斯卡-居禮一生不慕名利,奔波於科學研究、教育學子,將畢生毫無保留地貢獻給科學與社會。直到今日,世人仍持續讚賞她的付出與貢獻,紀念這位偉大的科學家。
參考資料:
- 維基百科—瑪麗.居禮
- 科學名人堂—居禮夫人
- 居禮夫人:大家都聽過的科學家,與她充滿波折的人生和感情路
- 科技大觀園—開啟輻射醫學大門的居禮夫人
- 傑出的科學貢獻與多舛波折的人生:瑪麗.居禮誕辰|科學史上的今天:11/7









































