儲能發展的關鍵未來:鋰離子電池的展望與課題——專訪台科大永續續能源發展中心黃炳照主任
鋰離子電池除了在當今的數位產品中佔有重要的角色,隨著全球氣候變遷、節能減碳的強烈需求,未來的再生能源技術,也需要鋰離子電池發展出足以配合的儲能系統,才能真正帶領我們走向「零碳排」的未來。本次科技大觀園專訪國家講座教授,國立臺灣科技大學永續續能源發展中心黃炳照主任,帶領我們一窺鋰電池技術的發展與未來。
如今,隨處可見各式輕便的電子用品,只要好好充個電,就能用上一段時間,這種習以為常的便利生活,就必須仰賴良好的電池,而 2019 年的諾貝爾化學獎,正是頒給現在最常聽到的「鋰離子電池」。
鋰離子電池除了在當今的數位產品中佔有重要的角色,隨著全球氣候變遷、節能減碳的強烈需求,未來的再生能源技術,也需要鋰離子電池發展出足以配合的儲能系統,才能真正帶領我們走向「零碳排」的未來。本次科技大觀園專訪國家講座教授,國立臺灣科技大學永續續能源發展中心黃炳照主任,帶領我們一窺鋰電池技術的發展與未來。
黃炳照主任。(圖/曹盛威攝影) 剛剛於今 (2021) 年獲得德國宏博研究獎的黃炳照,研究專長為各種能源材料研發,包括鋰離子電池、燃料電池及太陽能電池。他說明,鋰離子電池在設計的精進,已經接近學理上的極限:「鋰離子電池材料的單位體積電容量,從 1991 年生產到今天,其實進步並沒有太多。」如果要繼續發展,重心之一著眼於新電池材料的研發。
用於 iPhone 的鋰離子聚合物電池。(圖/Wikipedia ) 鋰離子電池的過去
摩爾定律 (Moore’s law) 預測電晶體效能,約在每十八個月會翻倍提升,相較來說,鋰離子電池進步的速度就緩慢許多。鋰離子電池上市至今的三十年間,我們所見越來越小、容量越來越大的電池,多數的進步主要來自於組裝技術,以及附帶組件的壓縮改良。常被簡稱為「鋰電池」的鋰離子電池,電池材料中並非直接有鋰金屬進行氧化還原作用,而是運用鋰離子在正負極間的移動與嵌入,來儲存電能。
正極半反應:
負極半反應:
鋰電池結構可以大致分解為正極、負極、電解液、隔離膜四大部分。所有的電池皆是利用正極與負極間的化學能電位差儲存電能。史丹利·惠廷安 (M. Stanley Whittingham) 在 1970 年代提出充電式鋰離子電池的概念;金屬鋰的反應性高,有機會能較其他使用於負極的金屬儲存更多的能量,可來取代笨重的鉛酸充電電池。惠廷安在早期的實驗中,採用二硫化鈦 (titanium(IV) sulfide; TiS2 ) 為正極,鋰金屬為負極,能夠產生二伏特的電流,證實了鋰離子電池的構想可行。然而此正極二硫化鈦易與水氣形成劇毒的硫化氫 (H2 S),且鋰金屬接觸空氣時的穩定度相當低,由於安全顧慮無法商業應用。而至古迪納夫 (John B. Goodenough) 於 1980 年改採鈷酸鋰 (lithium cobalt oxide; LiCoO2 ; LCO) 為正極,使鋰離子電池展現了高電位、高電容量密度、低自放電率與循環穩定性高的特性,至今這類材料仍常見於商業產品中。而適用於負極的材料,則在日本時任旭化成株式會社研究人員的吉野彰 (Akira Yoshino),改以石油焦炭製成石墨電極,終成就鋰離子電池能夠上市的重要突破。這三位在鋰離子電池上的貢獻,讓他們於 2019 年獲得諾貝爾化學獎。
吉野彰與 John B. Goodenough、M. Stanley Whittingham 於 2019 年獲得諾貝爾化學獎。(圖/The Nobel Prize ) 1991 年,首款鋰離子電池正式上市,引發了電子用品革命的起點:可攜帶的筆記型電腦指日可待,即將席捲全世界的 MP3 播放器、智慧型手機與平板電腦也躍躍欲試。由此之後,鋰離子電池的進步不脫材料以及組裝的改良研究,在顧及安全性的前提下,將各種組件輕薄化,盡可能塞入更多的電極材料,提高能量密度。
鋰電池更具電力的未來
現在的電池技術在能量密度上,大約在 200-250 (Wh/Kg),現階段如特斯拉等廠商希望透過組裝、大數量串連等方法提升至約 300 (Wh/Kg) 左右。黃炳照表示:「因為工程、物理上的限制,再要有突破就需要材料上的革命。」
如果要進一步提高單位體積的能量密度,還可以怎麼做呢?
概念上可以回歸 1970 年代的設想,使用鋰金屬做為電池的負極,運用鋰金屬有超低還原電位的特性,大幅提升能量密度。但該如何克服鋰金屬低穩定度低的缺點,在科技發展追求更高能量密度的同時兼顧安全性?黃炳照為我們介紹了「無負極電池」的概念:生產階段不需要鋰金屬,於電池正極材料中帶有的鋰離子,在完成組裝後充電,才離開正極,嵌入負極還原為鋰金屬。如此設計的電池不需組裝負極,因此理論上製程簡化成本較低,也避免了組裝使用鋰金屬所需的繁複安全措施。
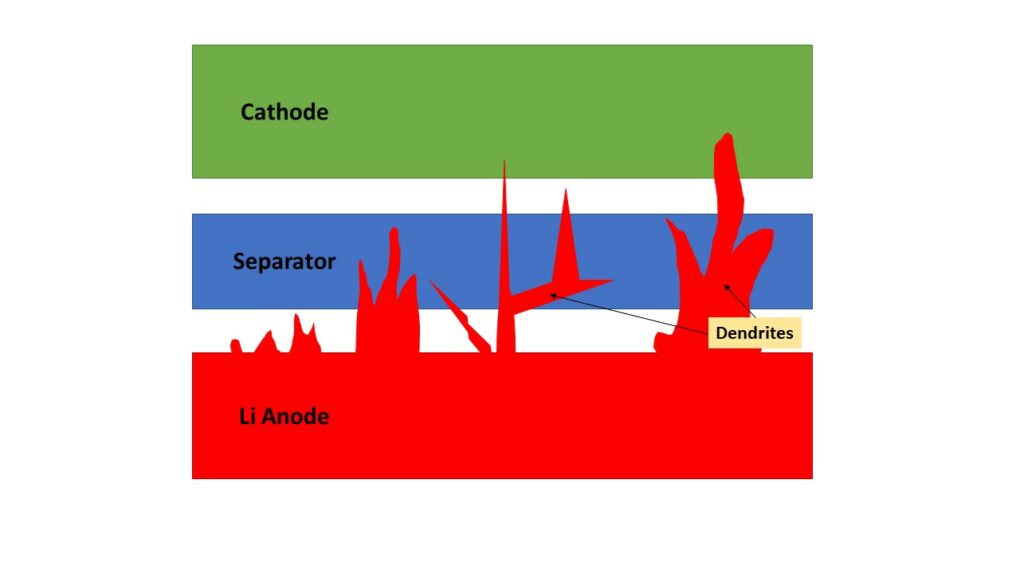
儘管令人期待,但無論是「無負極電池」或是「鋰電池」,仍需要回過頭以現今的材料技術,攻克過去使用鋰金屬於負極容易發生的安全議題。黃炳照挑戰的課題之一,便是鋰金屬負極循環充放電時,沉積不均勻會導致鋰枝晶形成 (Dendrite Formation)。當鋰金屬表面有缺陷,其界面就容易由於電場不均勻而發生鋰枝晶,此類狀況輕則提高電池內部阻抗,減少循環壽命;嚴重則枝晶會穿刺隔離膜,導致電池發生內短路 (Internal Short Circuit) 而失效甚至起火的安全疑慮。
黃炳照率領團隊從電解液與「固態電解質介面」 (Solid Electrolyte Interface,SEI) 的角度著手。固態電解質介面為電池首次充放電的時候,電極與液態電解質之間會自然形成的特殊隔層,可容鋰離子通過並且保護電極材料。「在這個(負極)石墨表面形成一個『薄紗』,就像一個濾網。沒有這個薄紗就沒有我們今天的鋰離子電池。」
因此發展最恰當的電解質配方,以形成穩定電解質介面,並抑制鋰枝晶的成長、及降低電解液的分解,最終提昇效率以及電池的循環壽命,即是黃炳照團隊努力的主要目標。
鋰電池的未來發展,還包括許多人期待的「固態電池」研發。將電解液由原本的液態改良為固態,也是許多人矚目的焦點。由於鋰對水的活性極大,因此鋰電池的電解液成分以有機溶劑為主,卻有著易燃的缺點。黃炳照表示,現階段材料科學已發表許多固體的電解質材料,鋰離子在其中的傳導的效率可比在液體中還要快。
「就像提供給鋰離子的高速公路。」黃炳照解說,固態電池將可望取代始終具有一定安全性疑慮的鋰電池,但完成組裝正式商業化,至今仍有許多挑戰需要克服。
黃炳照研究的主題除了鋰離子電池,主要為創新奈米結構能源材料研發。其中「同步輻射臨場光譜技術」就扮演了重要的角色。以此技術研究電池,就像幫材料照 X 光拍影片,可以即時觀察充電時材料的變化,以了解並優化電池運作的諸多細節。
「同步輻射就像是一個航空母艦,上面的不同光束 (Beamline) 就像戰鬥機群。」黃炳照比喻,相較於同步輻射提供的設施,各校系的貴儀(貴重儀器設施),就像是無人機,所能提供的「火力支援」有所不及。此技術對於各種電池材料,包括鋰離子電池、燃料電池及太陽能電池等未來的發展都極具影響力。
綠色能源的未來:更安全、更便宜、環境友善
臺灣正在走向能源轉型的階段,再生能源佔比將越來越吃重。考慮到綠能天生不穩定的弱點,需要儲能設施做為輔助。未來的儲能設備將著重在哪類的技術呢?黃炳照認為,能源的使用一直都是多元化的,無論是鋰電池、氫能、燃料電池等儲能技術,都各有其特性。重點仍在於發展出適用、更便宜、性能穩定,且對環境友善的技術,支持各種應用場景的需求特性。
舉例來說,交通工具的電動化將是未來的趨勢,但現行以鋰離子電池為主的儲能設備,其馬力跟續航力有一定的關聯性;相對來說燃料電池則有機會如油車採「油箱與引擎」的分開規劃。又或者受限於電池載重,難以發展電池動力飛機,但氫能如能有效應用其能量密度有潛力供綠色航空起飛。
電動車的充電停車場。(圖/Wikipedia ,Epattloamer的作品,CC BY-SA 3.0) 黃炳照表示,環境友善、永續將會越來越重要。未來隨著各國對於環境保護的需求越來越強烈,使用可再生的綠能將不再只是企業自願性可選擇的作為,終將成為是否具備競爭力的重要環節。臺灣身為全球供應鏈的一份子,要保持商業競爭力,積極發展綠能與相關的基礎建設,很快將迫在眉睫。
要做到環境友善,未來電池的回收、循環經濟勢必成為重要的議題。黃炳照認為,首要的關鍵之一,當然在於研發階段就考量到回收需求而做出對應的設計;其次在後端的回收機制上仍有許多研發的空間,待有志之士投入。但環境友善的精神不應只著眼於最終的回收,還需考慮盡可能最大化產品的使用效益。如應用於電動車的電池需要高端品質,淘汰後可應用於儲能系統,而後或可裝置於緊急照明系統等邊緣設施,如此層層重複利用,對於資源的使用才可達到最佳化。
環境永續將會越來越重要。(圖/Wikipedia,Tomasz Sienicki 的作品 ,CC BY-SA 3.0) 而這樣最大化、共通共用的概念也可以用於儲能基礎設施的規劃,如將公共電網的儲能需求與電動車充電站共用,在支持電網的同時,電動車用戶也有機會透過售電賺取外快。這類綠能基礎設施的設計形式,將考驗未來城市規劃者的創意與巧思。
鋰離子電池的發展,不僅促成不燃燒化石燃料的電動車成真,也讓我們見識到科技正幫助人類邁向節能減碳,甚至是零碳排的未來。未來,在科學家不懈的努力下,「環境友善、永續發展」終有機會不再是個口號,百尺竿頭再進一步,就讓我們一起拭目以待吧!
資料來源