- 作者/照護線上編輯部
- 本文轉載自 Care Online 照護線上《乳癌標靶治療,生物相似性藥幫助降低醫療負擔》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔

乳癌是台灣女性最好發的癌症第一名,每年新診斷的罹患乳癌人數約 1.4 萬名[1]。
衛服部桃園醫院外科主任周佳正醫師解釋,手術治療與放射線治療可以用來處理局部的癌組織;在手術前或手術後,還需要配合荷爾蒙治療、標靶治療、與化學治療等全身性治療,以降低癌細胞擴散、復發的機會,提升患者的預後。周佳正醫師建議,「若人類表皮生長因子受體 (HER2) 陽性,就要考慮標靶治療。」
在多種治療工具輔助下,乳癌整體存活率有長足的進步。若能接受定期篩檢, 並與醫師好好配合,早期乳癌的五年存活率可達 95% 以上[1]。
標靶治療可改善預後,但給付條件比較嚴格
周佳正醫師說明,近年來「標靶治療」的使用愈來愈廣泛,標靶藥物可以與特定受體結合,如同其名稱一般,是專一性較高的治療方式,對正常細胞影響較小,副作用較少。常用於乳癌的標靶藥物,是針對人類表皮生長因子受體 (HER2) 來發揮作用,當患者確診為具有 HER2 陽性的乳癌,若接受標靶治療能減少復發、轉移的機率、改善預後。然而,標靶藥物屬於生物製劑,開發藥物的成本高,製作過程較傳統化學藥物複雜許多,因此反映在藥價上就會比較昂貴,也比較耗費健保資源。

「目前全民健保的規定是,當乳癌有淋巴轉移,且具有人類表皮生長因子受體 (HER2),才符合健保使用標靶藥物的條件。」。HER2 陽性的患者必需已淋巴轉移或乳癌細胞擴散,才會符合健保給付規定,未符合的患者若想接受標靶治療,就需自費使用,經濟負擔較大。
生物相似性藥幫助降低醫療負擔
周佳正醫師指出,部分標靶藥物已經上市多年,當專利到期之後,其他有能力研發生物製劑的藥廠便能依據其胺基酸序列來製作「生物相似性藥」。然而,這可不是一件容易的事情,畢竟要利用活體細胞生產出蛋白質四級結構,過程也是困難重重。

研發目標是製作出與參考藥物藥效、副作用皆無臨床顯著差異,相等的「生物相似性藥」。生物相似性藥廠需要經過六到八年的研發,大量比對、分析、篩選與製程調整,並進行臨床試驗,多次確認生物相似性藥是有效且安全的,才有辦法通過歐美審核上市。
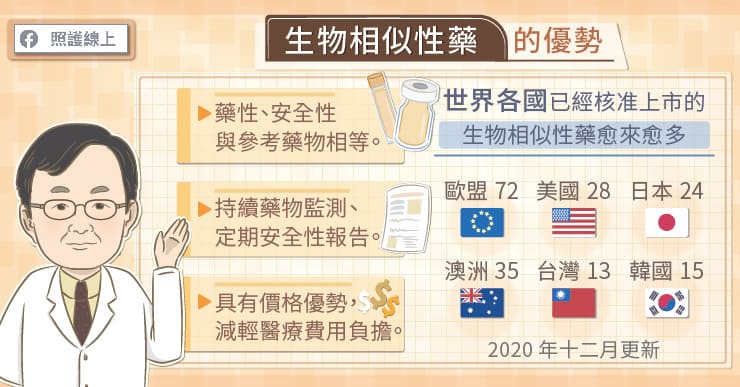
周佳正醫師指出:「目前國際上普遍都能夠接受生物相似性藥的概念,包括日本、歐洲、美國、台灣、韓國等,都有越來越多的生物相似性藥核准上市。」生物相似性藥本身就是生物製劑,分子量是傳統化學藥物的千百倍大,構造、製程皆複雜許多。上市之後,就跟一般創新的生物製劑一樣,會由世界上各國政府把關,持續進行藥物監測和定期安全性報告,以確保品質與用藥安全。
生物相似性藥讓更多患者受益於標靶治療
「生物相似性藥帶給患者最大的幫助就是經濟上的幫忙。」周佳正醫師表示:「畢竟標靶藥物頗為昂貴,生物相似性藥的價格低於參考藥物,做完整個標靶治療的療程,使用生物相似性藥的費用大約是參考藥物的六至到八成左右,降低患者的經濟負擔。」
周佳正醫師提醒,要戰勝乳癌,患者務必與醫師好好溝通,了解腫瘤特性並擬定適當的治療計畫,才能減少復發、轉移的機率。生物相似性藥的問世,等於多了種新的治療選擇,讓更多有需要的患者能夠受益於標靶治療,不再因為經濟因素而放棄治療,期許未來有更多患者能因此戰勝乳癌!
參考資料
- 衛生福利部公布癌症發生資料,2020/06/02TW-02481-BIO-2021-MAR
- 本文轉載自 Care Online 照護線上《乳癌標靶治療,生物相似性藥幫助降低醫療負擔》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接