面臨喪屍大爆發,老梗電影劇情常見的對應之道無外乎兩種:其一是尋找安全的地方,躲避喪屍;其二是找出喪屍病毒來源,開發疫苗拯救全人類。
如果台灣爆發了喪屍病毒,這座四面環海的島嶼似乎無處可躲,疫苗看起來是唯一的救命稻草。那麼問題來了,如果出現了有效的疫苗,需要有多少人接種才有機會消滅可怕的喪屍病毒呢?

求生必備!武器與免疫於喪屍的夥伴當然越多越好
影視劇裡喪屍的可怕之處,除了會失去理智、狂暴、極度攻擊性並且沒有疼痛感;更嚴重的是,一旦正常人被咬,就會立刻感染成為新的喪屍繼續傳染給下一個人。總是不會被咬的主角只能拿起槍炮武器,將喪屍群一個個爆頭來求得一絲生機,這時候若是有更多的同伴對病毒免疫、手上有武器,就越能保護手無寸鐵的弱勢個體。
相同的道理可以延伸在使用疫苗預防傳染病:當接種了疫苗、對傳染病有抵抗力的人越多,越能保護少部分沒有抵抗力的人。這在流行病學上稱之為群體免疫(herd immunity/ community immunity),表示在一群人當中,對某種傳染病具有免疫力的人數占了大部分,使得無免疫力的少部分個體被感染的風險也隨之降低、可受連帶保護。想像一下,沒武器的你正在逃命,有越多身邊的夥伴免疫於喪屍,當然比起他們隨時有可能受感染來得更為安全、生存率更高。

一傳十,十傳百:傳染病的傳染力怎麼計算?
因此防止喪屍病毒的傳播,除了將喪屍爆頭之外,還可以透過接種疫苗,讓人不會被傳染成新的喪屍,理論上就能逐漸控制喪屍病毒的傳播。但這裡重點來了,如果被喪屍咬到必然百分之百變成新的喪屍,除了消極的避免被咬,就必須全部的人類都打疫苗才能消滅喪屍病毒。
幸好,真實世界裡不同疾病的傳染力有高有低,而且也不太可能達到百分之百的接種率。根據疾病的傳染力,就能夠計算出達到群體免疫最低接種的人數門檻,推廣疫苗達到此門檻才是合情合理的可行辦法。為了計算出群體免疫門檻,在流行病學上有個專有名詞稱為「基本再生數(basic reproduction number, R0)」,是一種代表疾病傳染力的指標。當 R0 越大代表疾病傳染力越強,其定義簡單來說,是指一個感染者平均會傳染給幾個不具免疫力的健康者(沒有得過此病或沒有打過疫苗的情況)。
基本再生數可以用另一種比喻來設想,若是想要比較不同人傳播謠言的能力(簡稱八卦力),例如小明每次只會把謠言告訴身邊的 2 個人,而小強每次卻可以告訴身邊的 10 個人,顯而易見小明的八卦力等於 2,而小強的八卦力等於 10,小強傳播謠言的能力遠遠大於小明,要防堵小強傳播謠言的困難度也會比較高。
不同的人會有不同的八卦力,同理,不同的疾病也有著不一樣的 R0,如下表所示,其中麻疹病毒有著相當嚇人的傳染力,R0 高達 12–18。
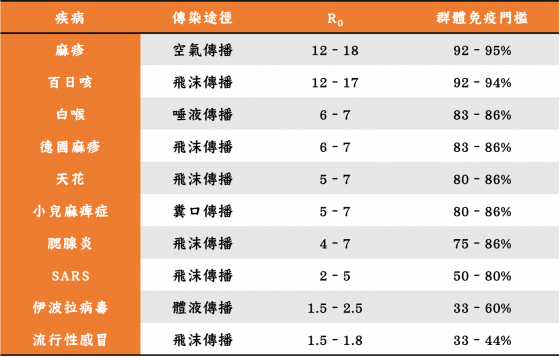
傳染病百百種,群體免疫門檻各不同
看過表格後,眼尖的你應該已經發現,這些耳熟能詳的疾病其 R0 都大於 1,每名患者平均可以感染超過一個人,所以新增患者的個數將呈指數式增長,這也是病原能夠對全體人類造成毀滅性傳染的因素。因此,在數學邏輯上,只要能將 R0 降低到小於 1(R0 < 1),就有機會撲滅該疾病。
目前降低 R0 已知的辦法有三種:
- 增加人群間的距離:停止上班、上課或管制特定場所之出入,以減少人群彼此接觸。
- 治療或隔離患者:降低感染者的傳染力,以及減少傳染給別人的機率。
- 疫苗接種或抗病毒藥物預防性投藥:增加未感染者對該疾病的免疫力或抵抗性。
三個方案中最為治本、有效且經濟的辨法,就是疫苗接種了。人類歷史上就是藉由疫苗接種,成功撲滅了「天花病毒」這種可怕疾病,早在 1980 年世界衛生組織(WHO)就已宣布撲滅天花,1986 年所有國家更停止了天花的常規疫苗接種。
所以需要多少人接種疫苗才能達到群體免疫?其計算方法也是圍繞著 R0,其推算過程較複雜,讓我們直接跳到結果公式:
疫苗接種比例 = 1-1/R0
不同疾病的群體免疫門檻(即最低疫苗接種率)也列於上表,用不著我說,聰明如你應該已知道 R0 越大,群體免疫門檻值越高。
所以說,到底要有多少人接種疫苗才有機會消滅喪屍病毒?
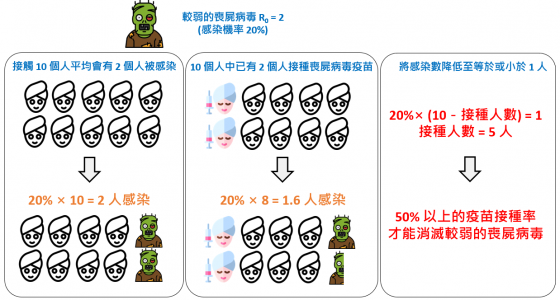
不喜歡公式夥伴們,讓我們以想像中的喪屍病毒舉例說明,可能比較容易理解。
每位和喪屍接觸的人都有可能感染喪屍病毒,不過這裡舉例設定的喪屍病毒比較弱一點:R0 = 2,代表一名喪屍出現後,平均會有 2 個人被感染。這裡我們假設每名喪屍在成為喪屍後到被爆頭前平均會接觸到 10 個人,最後會有 2 個人被感染,感染率就是 20%。但如果這 10 個人中已有 2 個人接種過喪屍病毒疫苗,則接觸到病毒能受感染的人只餘 8 個人(10-2 = 8),以接觸後的感染率計算,則每名喪屍只能感染 1.6 個人(20%×8),意即感染數就可以由 2 降為 1.6 人。
要撲滅疾病,就需要將感染數降低至等於或小於 1 人,我們可以得出運算式為 20%×(10-接種人數)= 1,此處接種人數的解答為 10 個人中至少要有 5 個人接種過疫苗,這意味著對抗這種(R0 = 2)喪屍病毒的有效群體免疫,必須要達到 50% 以上的疫苗接種率。
妥善利用疫苗對抗疾病,達成群體免疫的重要目標
不論今天面對的傳染病是否為喪屍病毒,疫苗的數學邏輯目標十分單純,只要達到「R0 < 1」,就能控制住傳染病。利用四則運算獲得解答後,接下來只要努力讓接種疫苗人數超過最低門檻,就能達到有效群體免疫。不過,真實世界當然不是數學題,還有變數層出不窮需要解決,例如:現階段的登革熱疫苗還有安全性疑慮,也尚未在台灣核准上市;腸病毒目前並沒有特效藥,而疫苗也還在研發階段。這也是為什麼面臨登革熱或腸病毒爆發,必須積極採取隔離或環境消毒措施。
一旦爆發沒有疫苗或藥物可以對付的傳染病時,人類能夠做的事情其實並不多,而這些慘痛的教訓並不遙遠。惡名昭彰的西班牙流感距今也不過 100 年(1918年),爆發當時全球三分之一人口受感染,造成約 5,000 萬人死亡;另一個記憶猶新的教訓,則是僅僅十幾年前(2002年)爆發的嚴重急性呼吸道症候群(severe acute respiratory syndrome, SARS)。
近幾年的喪屍影視劇裡,怕觀眾看膩了血肉橫飛的畫面,為了增加戲劇性及可看性,常常會再加油添醋引入「僵屍無腦但人心叵測」的劇情。可笑的是戲如人生,真實世界裡在面對傳染病這樣的「天災」時,若有疫苗能作為對抗的武器,我們應該要心懷感激並感到慶幸,盡力讓群體免疫得以實現。
然而,實際上目前世界各地有許多反對疫苗的流言蜚語,下篇文章我們接著談談,防疫工作遇到了哪些流言「人禍」?又該如何看待呢?
參考資料
- History and epidemiology of global smallpox eradication.
- Biggerstaff M, et al. BMC Infect Dis. 2014;14:480. Estimates of the reproduction number for seasonal, pandemic, and zoonotic influenza: a systematic review of the literature.
- Wallinga J, et al. Am J Epidemiol. 2004;160:509-16. Different epidemic curves for severe acute respiratory syndrome reveal similar impacts of control measures.
- Althaus CL, et al. PLoS Curr. 2014 Sep 2;6. Estimating the Reproduction Number of Ebola Virus (EBOV) During the 2014 Outbreak in West Africa.
- Diekmann O, et al. J Math Biol. 1990;28:365-82. On the definition and the computation of the basic reproduction ratio R0 in models for infectious diseases in heterogeneous populations.
- 疾病管制局 98年,流感大流行疫情模擬介面建置
- Pennington H, et al. Bull World Health Organ. 2003;81:762-7. Smallpox and bioterrorism.
- WHO Factsheet. Smallpox.
- Quanta Magazine, How Math (and Vaccines) Keep You Safe From the Flu
- 衛生福利部疾病管制署–登革熱
- Gretchen Vogel. Science. Apr. 19, 2018. A new dengue vaccine should only be used in people who were previously infected, WHO says.
- 衛生福利部疾病管制署–腸病毒
- Short KR, et al. Front Cell Infect Microbiol. 2018;8:343. Back to the Future: Lessons Learned From the 1918 Influenza Pandemic.
- 衛生福利部疾病管制署–嚴重急性呼吸道症候群