【2018 諾貝爾化學獎】化學的革命性進化:酵素定向演化
化學的革命性進化 演化的力量是透過生命來顯示的。2018 年的化學諾貝爾桂冠頒給阿諾(Fances H. Arnold)、史密斯(George P. Smith)和溫特(Gregory P. Winter),表彰她/他們透過演化的控制為人類謀取了最大的福祉。運用人工定向演化(directed evolution)所製造的酵素,現在已被用來生產包括生質燃料和藥物等等的物質。抗體的演化可以透過一種噬菌體顯示(phage display)的方法來對抗自體免疫的疾病,以及在某些特定的例子中治癒轉移性癌症。
我們活在一個由強大的力量:演化,所主導的星球。在頭一批生命的種子於 37 億年前出現時,幾乎地球上的每一個裂縫都充滿了能適應身處環境的生物體:生長在光禿禿山脈的地衣、於溫泉茂盛生長的古菌、能存活於乾燥沙漠的多鱗爬蟲類以及能在黑暗深海中發光的水母。
學校裡我們在生物課學習到這些生物,但讓我們戴上一副化學家的眼鏡,並換個視角來觀察,地球上的生物之所以能夠存在,是因為演化解決了無數複雜的化學難題,所有的生物都有能力從其環境的利基取得材料和能量,並用來建立它們的組成所特有之化學創造品。魚能在極地海洋中悠遊,是歸因於其血液中的抗凍蛋白質,貽貝能攀附在岩石上,乃因它們發展出了能在水中運作的分子黏膠,而這只是眾多例子中的幾個而已。
生命化學精彩的地方在於它被設計在基因的程式碼中,並讓它能被遺傳且不斷進化。一個小小的基因隨機變化,就能改變其化學,有時這導致產生較弱的生物體,但也有可能產生一個很強壯的個體。新的化學慢慢的發展,而地球上的生命隨之變得愈來愈複雜。
這個過程現在已經演化出了三個非常複雜的人類個體,具有能掌控演化的能力,2018 年的諾貝爾化學獎之所以頒給這三位科學家,乃因為她/他們透過定向演化革新了化學以及新藥物的發展。讓我們先從酵素工程的明星:阿諾(Fances H. Arnold)開始介紹。
2018 的諾貝爾化學獎得主們能控制演化,並進一步的在她/他們的實驗室中向前開拓。圖/諾貝爾化學獎專題系列 酵素──生命的化學工具中之利器 即便在 1979 年,身為一位剛取得機械與航太工程學位的新鮮人,阿諾就已經具有了一個憧憬:透過新科技的發展以謀求人類的福祉。美國已經決定在 2000 年要有 20% 的能量是來自於再生能源,而她剛好是在研究太陽能,不過這個產業的未來前景,於 1981 年的總統大選後,產生了巨大的改變,因此她將眼光改為投注於新興的 DNA(去氧核糖核酸)科技,她自述「很明顯的,對於我們每日生活上所需要的材料和化學品,可以利用改寫生命密碼的能力,來創造新的製造方法。」
用傳統方式製造藥物、塑膠和其它化學品需要強力的溶劑、重金屬和腐蝕性的酸,她的想法是捨棄這些方法而改用生命的化學工具:酵素,它們催化在地球生物體中發生的化學反應,如果她能掌握設計新酵素的方法,就可從根本改造化學。
人的思考是有限的 最初就如同在 1980 年代末期的許多其他學者一般,阿諾企圖使用推理的策略來重塑酵素,讓它們具有新的性質。然而酵素是極端複雜的分子,它們是由 20 種不同的結構單元──胺基酸──以幾乎無限種可能的組合方式結合而成的,一個單一的酵素分子可以包含數千個胺基酸,它們連結成長鏈的型態,進一步摺疊成三維的立體結構,用來催化特定化學反應的局部結構,是建立在整體結構的內部。
運用邏輯推導來決定如何將這一個精密的構造重新調整,以賦予其新的功能,即便是運用現在的知識以及電腦能力來看,亦是非常困難的。在 1990 年代初期,謙卑的折服在大自然的優越能力之下,阿諾決定放棄上述她所謂「有些傲慢」的策略,取而代之,她獲取的靈感來自於使用大自然優化化學的方法:演化。
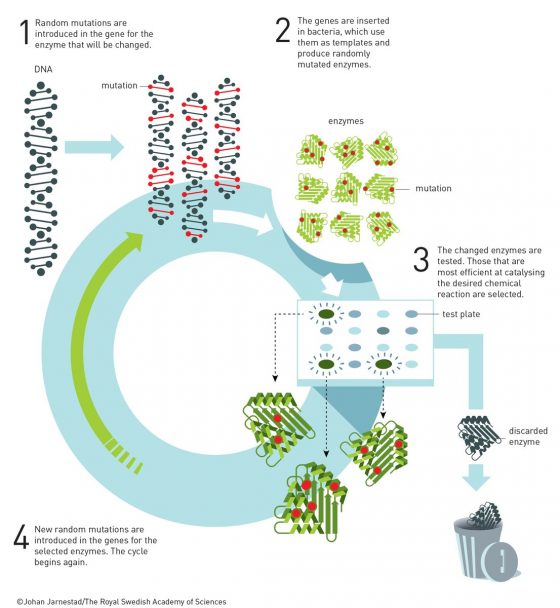
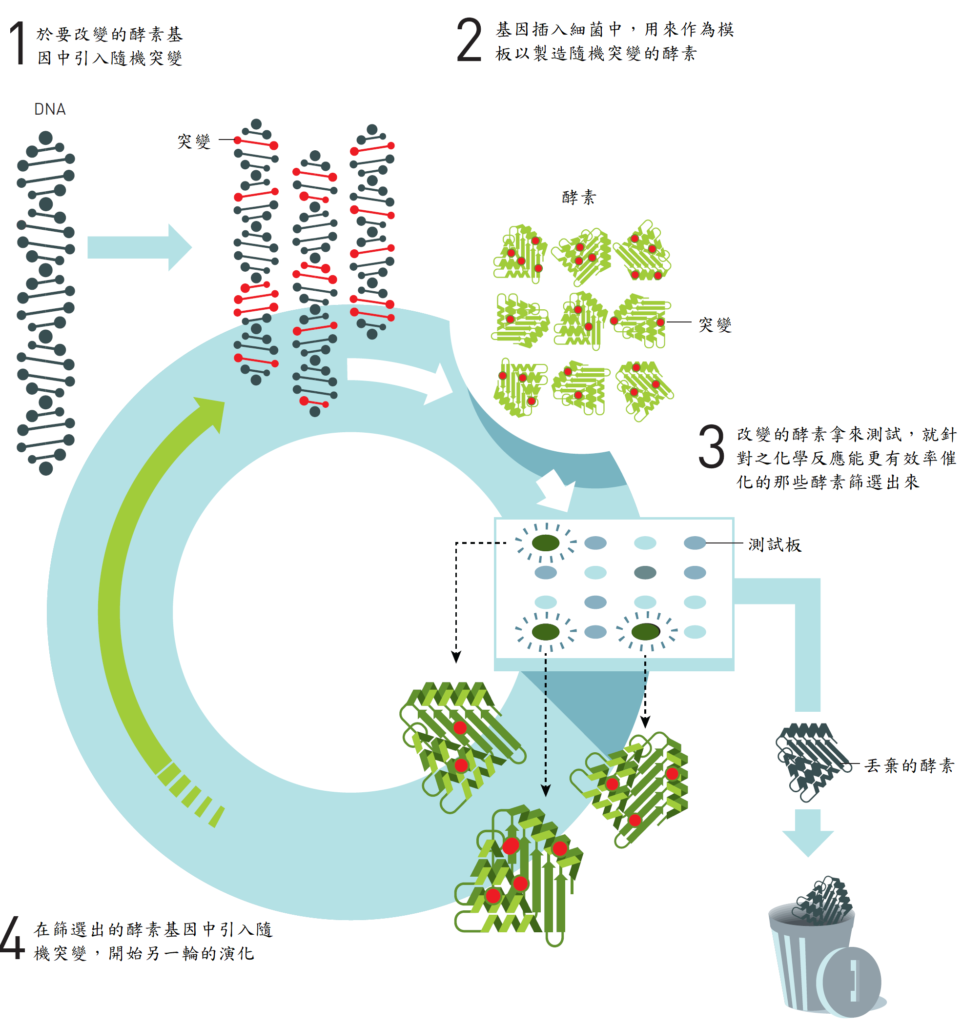
阿諾開始操弄演化 有好些年,她試圖改變一個稱為「枯草桿菌蛋白酶」的酵素,讓它不是在水溶液中催化化學反應,而能在一個有機溶劑:二甲基甲醯胺(簡稱 DMF)中運作。此時她刻意在酵素的基因密碼中製造隨機的變化──突變──然後將這些突變的基因引入細菌中,並產出數千種不同變體的枯草桿菌蛋白酶。
在這之後的挑戰是如何從如此眾多的變體中,找出在該有機溶劑中運作效率最高的那些酵素。在演化學中,我們說的是適者生存;在定向演化學中,這個階段稱為「選汰」。
阿諾利用枯草桿菌蛋白酶能切割一種牛奶蛋白質──酪蛋白──的能力,在一個 35% DMF 水溶液中,先選汰出切割酪蛋白最有效率的枯草桿菌蛋白酶變體,接著在這個變體中進行下一輪的隨機突變,得到另一個在 DMF 中運作效率更高的變體。
於第三代的枯草桿菌蛋白酶中,她找到了一個變體,其在 DMF 中的運作效率比原始的酵素要高 256 倍。這個酵素的變體總共含有十個不同位置的突變,最終造成的優異效果是沒有人能夠事先預測的。
透過這些實驗,阿諾展示了若要掌控新酵素的研發,僅憑藉人的推理能力,將遠遜於讓機率以及定向(人為)選汰來運作的力量。這是我們現在所見證的革命性發展之第一步,也是最具決定性的一步。
接下來的另一重要步伐,是由一位荷蘭研究人員及發明家史坦姆(Willem P. C. Stemmer)所邁出的,但他已於 2013 年過世。他引進了另一個酵素定向選汰的維度:試管中的交配。
定向選汰背後的運作原理:在數個定向選汰的輪迴之後,一個酵素可能增加數千倍的效率。圖/諾貝爾化學獎專題系列 交配──為了更穩定的演化 一個自然演化的先決條件是不同個體的基因可透過交配或授粉的方式混合,有用的性質可藉此結合,而得到更強壯的生物體,在此同時,較不具功能的基因突變,將於代代相傳的過程中消失。
史坦姆運用的是交配的試管對等法:DNA 改組(DNA shuffling)。在 1994 年,他將基因的不同版本切割成小片段,然後透過 DNA 科技的工具,將這些片段重新組合成一個完整的基因,就好像是原始基因的一個馬賽克版本。
透過好幾輪的 DNA 改組,史坦姆將一個酵素改變成比原始版本更有效率。這顯示利用基因的交配──研究人員稱之為「重組」──可達成更有效率的酵素演化。
新酵素製出永續生質燃料 那些 DNA 科技的工具自 1990 年代初期開始不斷的優化,用於定向演化的方法亦倍數成長。阿諾在這些發展中一直具有領先的優勢;現在她的實驗室所產出的酵素能催化的化學反應,甚至於根本不存於大自然中,而能製造出全新的材料,她裁製出的一些酵素也成為製造不同物質(例如藥物)的重要工具。化學反應不但可被加速,且減少不要的副產物。在某些例子中,可以去除透過傳統方法須使用的重金屬,大幅減少對環境的衝擊。
事情的發展更回歸了原位,阿諾又重新回頭開始研究再生能源的製造。她的研究小組研發出一些酵素,能將簡單的糖轉化成異丁醇,那是一種高能量物質,可用於製造生質燃料和較永續的塑膠。一個長程目標是製造出的燃料能讓運輸業更為環境友善,另類燃料──用阿諾的蛋白質所製造的──能用在車輛或飛機上。以這樣的方式,她的酵素促成了一個更永續的世界。
至於 2018 年諾貝爾化學獎所表彰的另一份工作,則是將定向演化導向了製藥,所產出的藥物能中和毒素,或對抗自體免疫疾病的進展,甚至在某些病例中治癒轉移的癌症。這是由一個能感染細菌的小小病毒所扮演的重要角色,而這個方法被稱為「噬菌體顯示」(phage display)。
史密斯運用噬菌體 經常發生的情況是,科學走了一條無法預測的路徑。在 1980 年代的上半期,當史密斯開始使用噬菌體──能感染細菌的病毒──主要是期望它們能用在基因選殖。此時 DNA 科技仍未成熟,而人類基因體仍是一塊未開發的土地,研究人員知道製造身體所需蛋白質的所有基因都存於其中,但是想要指認某一個蛋白質的基因,就好像在大海中撈針一樣困難。
不論如何,對能找到那個基因的科學家而言,將具有極大的益處。運用當時最新的基因學工具,基因可以插入細菌中──靠著一點運氣──該細菌能製造出大量想要研究的蛋白質,這整個程序被稱為基因選殖。而史密斯的想法是,尋找基因的研究人員可以透過一個巧妙的方式,運用噬菌體來做到。
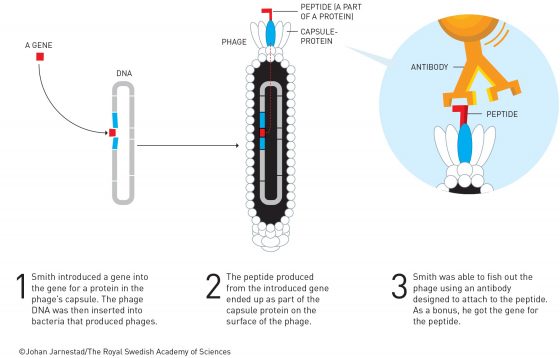
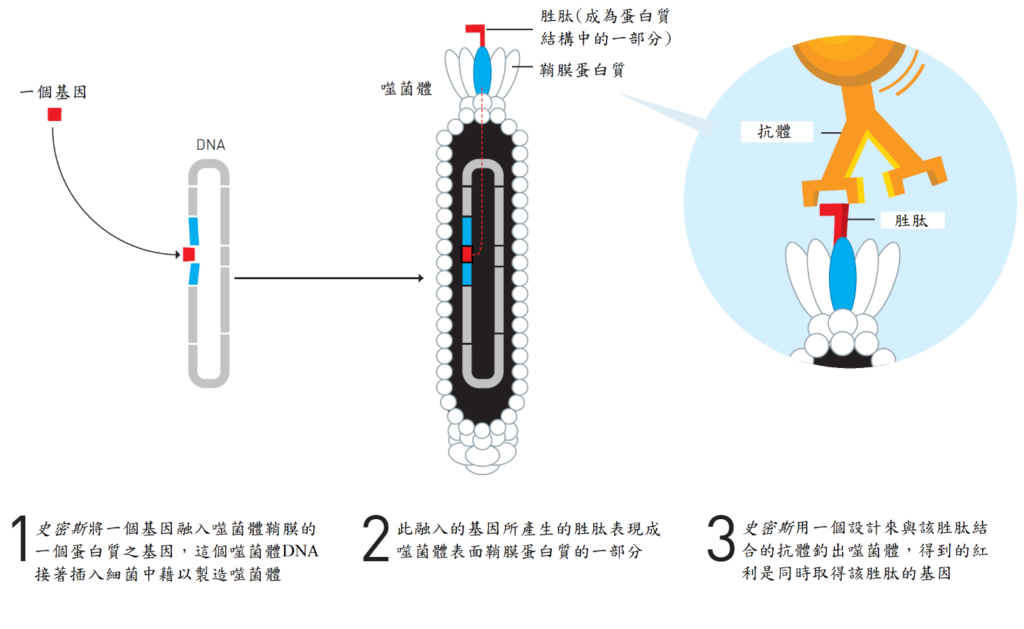
噬菌體:一個蛋白質與其未知基因的連結 噬菌體本質上具有很簡單的構造,它含有一小段的基因物質,封裝在一個由保護蛋白質形成的鞘膜中。當複製時,會將它們的基因物質注入細菌中,綁架細菌的代謝系統,接著利用細菌製造出噬菌體基因物質的拷貝,以及形成保護鞘膜需要的蛋白質,由此產生新的噬菌體。
史密斯的盤算是研究人員應可運用噬菌體的簡單構造,找出一個已知蛋白質的未知基因。在此時,已經有一些大型的分子庫存在,其內含有許多各種未知基因的片段,他的構想是這些未知基因的片段,可與形成噬菌體鞘膜的一個蛋白質基因融合,當新的噬菌體製造出來時,這個未知基因對應的蛋白質,就會出現在這個噬菌體的表面,與形成鞘膜的一個蛋白質結合在一起。
抗體可釣出正確的蛋白質 這個做法會導致生成一個噬菌體的混合物,各帶有許多不同的蛋白質於其表面。史密斯推論在下一個階段,研究者應能利用抗體,將帶有各種已知蛋白質的噬菌體,自這碗湯液中釣出。抗體是一些具有導向飛彈功能的蛋白質;它們能從數萬種蛋白質中,以高度的精準度,辨識並束縛住一個特定蛋白質。利用一個已知蛋白質的抗體,如果研究者能逮住一個自這碗湯液中釣出的東西,就可以順帶釣出這個蛋白質對應的未知基因。
這是一個漂亮的構想,而史密斯於 1985 年證實那是可行的,他製造出了一個噬菌體,其表面攜帶了一個蛋白質的部份胜肽,運用一個抗體,成功的將這一個他製造的噬菌體,由含有許多不同噬菌體的湯液中釣出。
透過這個實驗,史密斯建立了現在被稱為「噬菌體顯示法」的基石。此法的精彩處在於它的簡便,它的長處則是將噬菌體當成一個蛋白質與它的基因之連結。不過此法卻在基因複製的領域之外,取得其最主要的突破性進展;在另外一方面,於 1990 年左右,幾組研究人員開始運用噬菌體顯示法,來發展新的生物分子。其中一個採用此技術的人就是溫特(Gregory P. Winter)。感謝他的研究,使得噬菌體顯示法現在帶給人類更大的福祉,要瞭解其原因,我們需要對抗體進一步的認識。
抗體可遏阻疾病的進展 人類的淋巴系統能產生數十萬種不同抗體的細胞。在這一個發展完善的體系中,這些細胞通過檢驗,不會攻擊任何屬於身體之各種型態的分子,不過這龐大的種類能確保總是會有抗體,能附著在感染我們的病毒或細菌之上,一旦抗體附著在上面,就會傳送訊號給強悍的免疫細胞,趕來消滅入侵者。
因為抗體具有高度的選擇性,在數萬種分子中,只會附著在一個特定分子上,因此研究人員很早就希望設計抗體,能遏阻各種疾病在體內的進展,扮演藥物般的功能。最初為取得這些醫療用的抗體,是將各種藥物的標的物,例如癌細胞的蛋白質,注入老鼠體內。不過在 1980 年越來越清楚地知道此法是有侷限的;某些物質對老鼠是有毒的,但也有一些不會產生任何的抗體。更進一步發現這樣取得之抗體,會被病人的免疫系統視為異物,而被攻擊,導致這些老鼠抗體被破壞,為病人帶來副作用。
由於這個障礙,促使溫特開始研究史密斯的噬菌體顯示法可能具有的潛力。他想要避免使用老鼠,改成發展基於人類抗體的藥物,因為它們可以被我們的免疫系統所容忍。
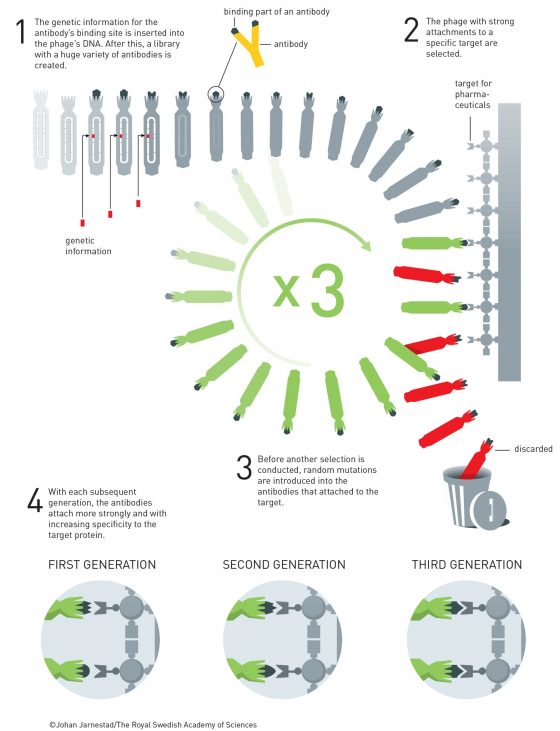
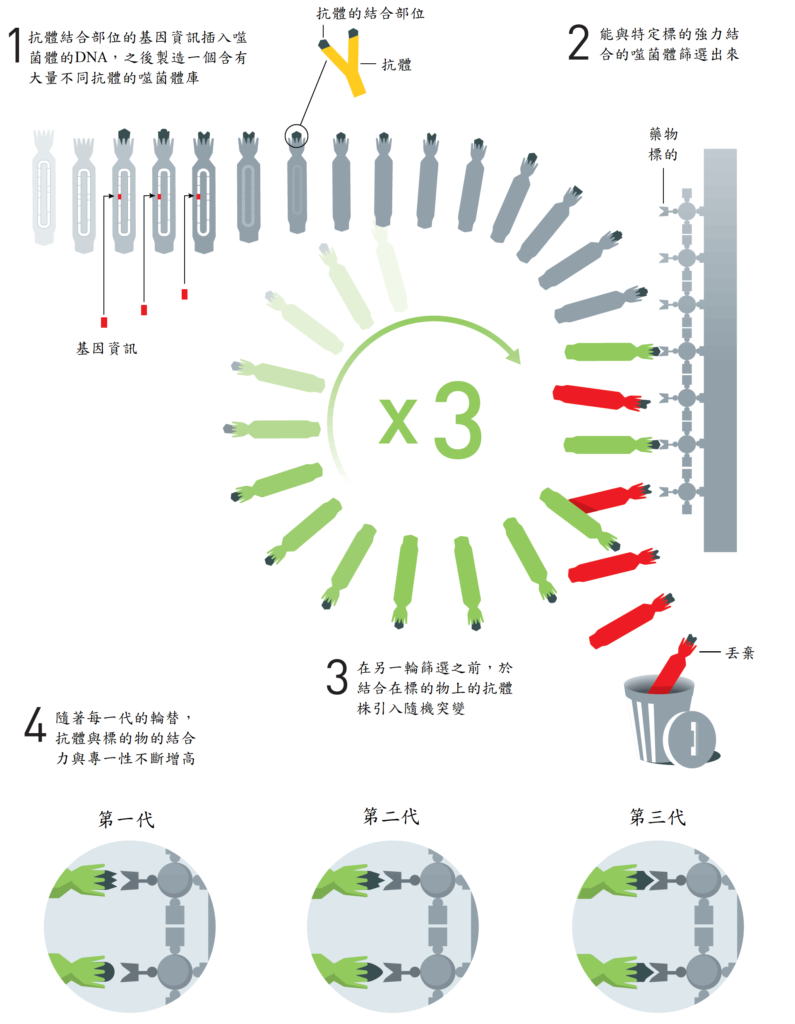
溫特將抗體置於噬菌體的表面 抗體是具有 Y 字形的分子;靠著每隻手臂的遠端附著在外來物質之上。溫特將此部分的基因訊息,與噬菌體鞘膜的一個蛋白質基因融合,於 1990 年他成功的證實此法,讓抗體的結合部位出現在噬菌體的表面。他所用的抗體是設計來與一個稱為 phOx 的小分子結合,當溫特用 phOx 作為一種分子釣魚鈎,他成功的從一含有四百萬個其它噬菌體的湯液中,釣出那個含有抗體在其表面的噬菌體。
在這之後,溫特展示了他能將噬菌體顯示法運用於抗體的定向演化。他製造了一個噬菌體庫,其內包括數十億不同的抗體表現在噬菌體的表面,從這個庫藏中,他釣出了一些可與不同蛋白質標的結合的抗體,接著他隨機突變這第一代的抗體菌株,進而創造出一個新的噬菌體庫,從中找到與標的物具有更強結合力的抗體。例如在 1994 年,他用此法發展出了一些抗體,能以非常高的專一性與癌細胞結合。
世界上第一個基於人類抗體的藥物 基於抗體的噬菌體顯示法,溫特與他的研究同仁創立了一家公司,在 1990 年代發展出一個完全基於人類抗體的藥物: adalimumab,此抗體能中和一個稱為 TNF-alpha 的蛋白質,該蛋白質驅動許多自體免疫疾病的發炎反應。於 2002 年此藥物被核准醫治風濕性關節炎,現在亦用於治療不同型態的牛皮癬和發炎性腸疾。
藥物 adalimumab 的成功,刺激了製藥業的重要發展,而噬菌體顯示法已被用來製造包括癌症在內的各種疾病抗體。其中有一個抗體能讓體內的殺手細胞釋出,以攻擊腫瘤細胞,使腫瘤生長遲緩下來。在某些例子中,那些產生轉移的癌症病患甚至也能被治癒,成為癌症醫療的歷史性突破。另一個抗體藥物被核准用於中和造成炭疽病的細菌毒物,另一種藥物能減緩稱為狼瘡的自體免疫疾病;還有更多的抗體現在正在進行臨床實驗,用來對抗阿茲海默症等疾病。
一個化學新時代的開始 由 2018 年的諾貝爾化學獎得主們所開發的方法,現在正以跨國際的方式發展,來提升一個更為永續的化學產業,產出新的材料,製造永續的生質燃料,減輕疾病挽回生命。酵素的定向演化和抗體的噬菌體顯示法,讓阿諾、史密斯和溫特帶給人類最大的福祉,並為化學的革命性變化立下基石。
延伸閱讀