癌症的治療從傳統的化療(chemotherapy)開始,近年來則因開發出標靶治療(target therapy)有很大的進步。
標靶治療的中心概念包括了找到腫瘤與正常細胞在遺傳組成上的不同點,設計出專門攻擊它的藥物;由於這藥物不會攻擊正常的細胞,因此對病人的健康狀況影響會比較小。由這個概念設計出來的標靶藥物,最有名的應該是針對肺癌的 Iressa 以及針對黑色素瘤(melanoma)的 Zelboraf。
像 Iressa(又名 Gefitinib)主要是抑制表皮生長因子受體(epidermal growth factor receptor,EGFR)[1],由於 EGFR 只在特定癌症(如肺癌與乳癌)中會過度表現,因此 Iressa 對這類的癌症相當有效。但近年發現,如 Iressa 這類的標靶藥物,往往在使用 1-2 年之後失去效用…為何會如此呢?
最近英國的科學家 Charles Swanton 以及 James Larkin 的發現 [2],或許可以解釋這個現象。
他們把病人的腫瘤取了九個不同位置的切片,同時也取了轉移位置的一些樣本(如圖);
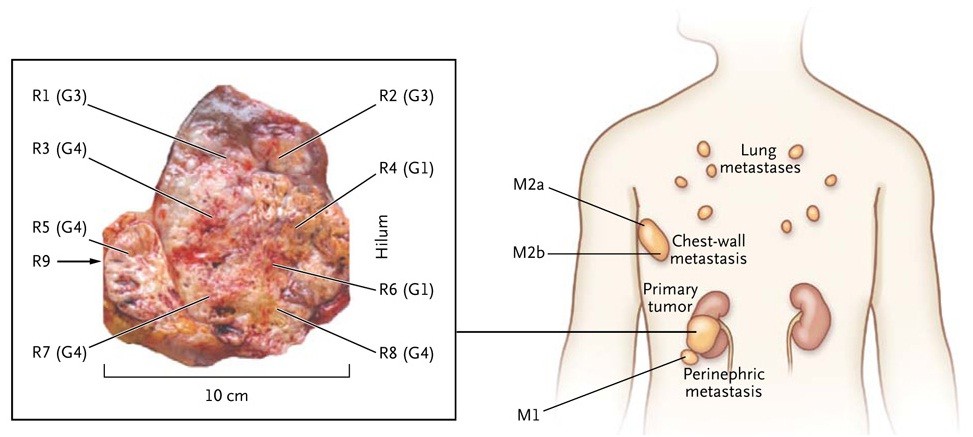
然後把這些切片拿去作一系列的遺傳測試,包含把所有的基因都定序出來。結果他們在所有的樣品中總共鑑定出 118 個突變,但其中只有 34% 的突變是存在於所有的樣品。而有些關鍵的癌症基因雖然在所有的樣品中都可以看到突變的發生,但是突變發生的位置也不相同。由於在治療上常以偵測「基因表現標記」(gene expression signature,也就是檢測哪些基因在腫瘤中有表現)作為預後(prognosis)的參考,既然腫瘤並非如過去所想的,由一個正常的細胞(clone)不斷突變累積形成腫瘤,而是由一群具有基因差異的細胞所組成的;如此一來就意味著以一次切片的結果來進行診斷,誤診的可能性很大。
當然這個研究成果,就如 UCSF 的 Carlo Maley 所說,測試的樣本數極小(只測試了 4 個病人,其中只有 2 個病人有仔細的測試);但是 Maley 也提到,這個實驗結果也提醒了我們,腫瘤並非如我們想像的是由相同的細胞組成,而這也解釋了為何標靶藥物在使用後 1-2 年內會漸漸失效的原因,可能不是腫瘤細胞產生抗藥性的突變,而是具有抗藥性突變的腫瘤細胞原來就存在於腫瘤中,標靶藥物消滅了不具有抗藥性的腫瘤細胞後,這些細胞得以增生並取而代之。
在現在許多藥廠都在致力於開發標靶藥物的時刻,他們的研究成果無異於投下一顆震撼彈。雖然說相比於傳統的化療,標靶治療減低了治療時的副作用,但是標靶藥物的價格昂貴,這也是一直為人所詬病的。如果終究是無法治療,那麼病人在診斷結果出爐且確定無法進行手術切除後,是否仍要接受標靶治療呢?筆者最近簽署了「預立選擇安寧緩和醫療意願書」,當時在與朋友討論時,也提到如果確診為癌症,且無法手術切除時,筆者打算放棄化療,但是標靶治療似乎是可以接受的;如今看來,似乎連標靶治療可能都不是好的選項(與其耗費龐大金錢治療,還不如將這些資金拿去救更多的人),當然每個人的想法不一樣,只是筆者常想到,在筆者上大學時(那已經是將近 30 年前的事了),曾讀到一些疾病無法治療,當時老師說:說不定過幾年就可以治療了。但是到現在,這些疾病也還是無法治療,甚至連我們一度以為已經克服的一些疾病(如結核病、瘧疾)都有捲土重來的樣子,究竟人與疾病的戰爭中,誰贏誰輸呢?
參考文獻:
[1] Wikipedia. Gefitinib. [31 March 2012]
[2] Cancer’s Many Faces of Resistance—ScienceNOW [7 March 2012]
本文發表於作者部落格