「醫生,我哥的手術成功率有多少?」
「零,所有做過這個手術的人,都死了」
兄弟,不夠的地方我給你
腎衰竭正折磨著一名23歲的年輕人。理查德(Richard J. Herrick)躺在床上,理當年少俊俏的臉龐,如今卻因高血壓和浮腫苦痛難當。他的孿生兄弟羅納德(Ronald Lee Herrick)正考慮著切下他身上一顆健康的腎臟,讓他的兄弟重獲新生。羅納德現在唯一的考量是,這個手術的存活率,是零。
但對波士頓的摩爾醫師外科團隊而言,要思考的事情太多了,手術失敗已不是特別的事(反正也沒成功過…),最壞就是病人死亡罷了。然而從活人身上切除一顆腎臟,確實是件有違道德的事。納粹利用活人進行實驗不過是9年前的事情而已,真的有必讓他的兄弟冒著失去生命的風險來換回一條人命嗎?但從學術的角度上來看,這對孿生兄弟,就是天生的複製人,是有機會突破免疫排斥高牆上僅有的缺口-「身體不會拒絕和自己長得一模一樣的器官!」。1954年12月23日,聖誕節的前夕,摩爾醫師等人,不顧外界的抨擊,決意讓病人上手術檯。手術團隊裡的穆雷醫師執起沉重的手術刀,劃開了兄弟倆的身體,同時也劃開了歷史… …[註1]

婚禮對新婚夫婦倆人來說是件意義非凡的大事,而這場婚禮對器官移植界來說更是別具意義。羅納德笑著看著他的兄弟,不久之前,他還躺在波士頓哈佛醫院的病床上,而今日,他的兄弟不僅帶著他分享的一顆腎臟,更牽著當初照顧他的護士小姐(今天的身分是新娘)步入禮堂,這種戲劇張力,恐怕連電影情節都不見得編的出來……
有別於理查德婚禮的溫馨,這個創下歷史新頁的移植團隊,在簡短的病例報告中寫著:「患者原先的高血壓完全消失,移植的腎臟已經在新的身體裡存活11個月…」這短短的幾頁病例報告,其代表的意義是器官移植的時代已經來臨。這對存活的兄弟為全球數以萬計的腎衰竭患者帶來希望,成千上萬的患者湧入波士頓,向摩爾醫師的外科團隊尋求一線生機,也讓當日執刀的穆雷醫師一戰成名,而奠定基石的休姆醫師,也被視為移植界的先鋒者!(36年後,穆雷醫師也因為他持續地在器官移植領域的貢獻,獲得諾貝爾醫學獎的肯定;遺憾的是,休姆醫師在1973年因飛機失事而離世,未能得見他一手打造的器官移植醫學大放異彩。)
儘管值得喜悅,但這對孿生兄弟的手術成功,也大辣辣地打了醫學界一巴掌!代表著先前的手術失敗,並不是因為技術不精良,僅僅就是因為免疫系統排斥新臟器的緣故,以往在手術台上遭受撒旦詛咒而死去的病人,其實最大的敵人就是自己體內的免疫巨人。於是,要繼續挑戰夢想中的器官移植,只需要追尋最後的聖杯-完美的抗排斥藥。
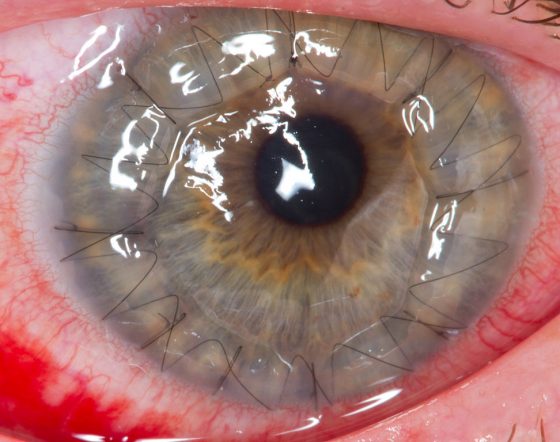
聖杯的追尋
首位碰觸到聖杯的是一對化學合成實驗室的搭檔,艾利昂女士(Gertrude B. Elion)和希青斯先生(George H. Hitchings)。他們在戰火不斷的40年代持續合成核酸(nucleic acids)衍生物,首先登場的是6-mp(6-Mercaptopurine),後來是出名的治療血癌用藥。而在1957年合成出的是azathioprine,則是造福了廣大風濕性關節炎患者。

在6-mp進入移植界之前,也有其他人試圖正面迎戰免疫細胞。首先是類固醇,英國免疫學者梅達瓦爵士(Sir Peter Brain Medawar)[註2]發現它能有效紓緩免疫系統。而在波士頓,身為穆雷醫生前輩的休姆醫師,則採用更激烈的手法:將狗照射X光以破壞全身的免疫系統,休姆醫師也同時進行6-mp化學藥物的實驗。可惜的是,不論他如何調整X光或藥物的劑量,狗不是死於器官排斥(X光或藥物劑量太小),就是被細菌感染而死(X光或藥物劑量太大)。在這座尋找聖杯的戰場上,越來越多的死亡案例及實驗報告指出,使用單一療法來對抗免疫排斥是有效的,但藥物安全劑量的範圍可能極為狹窄,這部份的瓶頸須要有新的思維才能有所突破。

舞台換回1960年大西洋彼岸。法國。古斯醫師(René Küss)改良了許多前輩失敗的案例,採用X光+類固醇+6-mp的雞尾酒療法,終於成功地移植了5例非雙胞胎的腎臟,代表著核酸藥物的初步勝利,也讓下一代核酸藥物azathioprine有了大展身手的舞台。此時接棒的人物是史達策(Thomas E. Starzl)醫師,同時也是前高雄長庚醫院院長陳肇隆醫生的恩師 [註3]。史達策改進雞尾酒混合藥物療法,在1966年發展出抗淋巴球抗體(anti-lymphocyte globulin, ALG)+類固醇+azathioprine的療程,有效提高腎臟移植患者的術後存活率。此時的歐美各國,腎臟移植技術漸漸普及到各地的醫院,而其他器官的移植,也開始有了新的曙光。
隔年,史達策醫師即將再次挑戰體內最大的臟器-肝臟移植。此時,是1967年,距離首例腎臟移植成功已跨過遙遠但卻意義非凡的13年。 [註4]
下一章:用器官拼圖的人
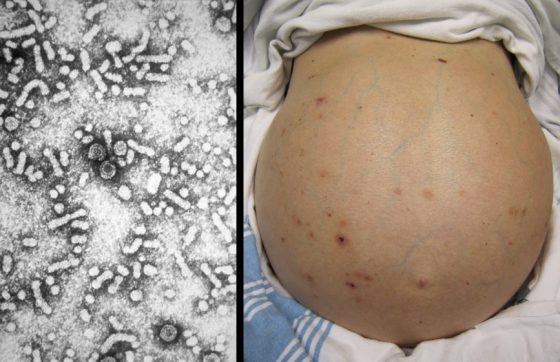
【科學簡史】雖死猶生的器官移植系列:
- 註1:為求書寫流利和情節起伏,本文所出現的對話皆為模擬情境
- 註2:梅達瓦爵士和弗蘭克·麥克法蘭·伯內特爵士(Sir Frank Macfarlane Burnet)因為對於免疫系統和移植物之間的交互作用,及胚胎早期的免疫耐受性的研究,而獲得1960年的諾貝爾醫學獎
- 註3:史達策醫生,全球首位肝臟移植成功的醫師。陳肇隆醫生,台灣首位,同時也是亞洲首位肝臟移植成功的醫師。
- 註4:當時有許多的醫師在各個臟器上都歷經了巨大的研究和失敗,其中的努力很難以寥寥數語表達,有興趣的讀者可閱讀「拼圖人:一個器官移植外科醫師的回憶錄」。