- 作者/吳明儒教授
- 本文轉載自 Care Online 照護線上《腎臟移植重點講解,醫師圖解說明》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔

我們的腎臟主要負責維持體內水分和電解質的平衡,並排除一些代謝廢物。當腎臟功能衰竭,患者就必須仰賴定期洗腎來維生。根據健保署統計,2019 年健保支出最多是疾病是「慢性腎臟疾病」,治療費用高達 533 億元,接受洗腎治療的患者超過 9.2 萬人。
臺中榮民總醫院內科部主任吳明儒教授指出,腎臟移植能幫助患者脫離洗腎的羈絆,生活品質大幅提升,也有助於降低醫療支出。
台灣的腎臟移植技術已相當成熟,接受腎臟移植五年後,患者存活率高達 93%,而且有超過 85% 的移植腎臟仍然具有功能。隨著免疫抑制劑的進步,有超過半數的移植腎可以存活 15 至 20 年以上。
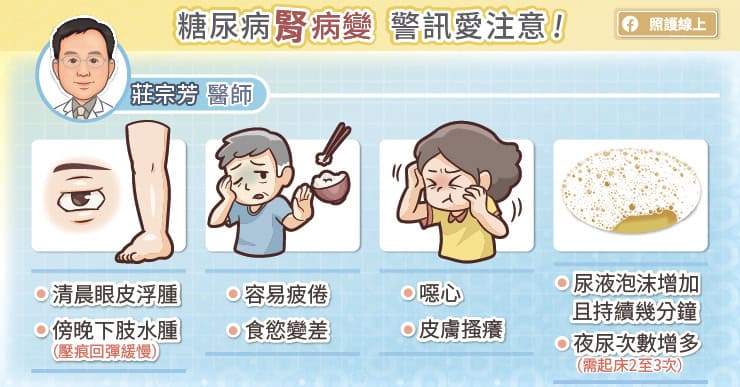
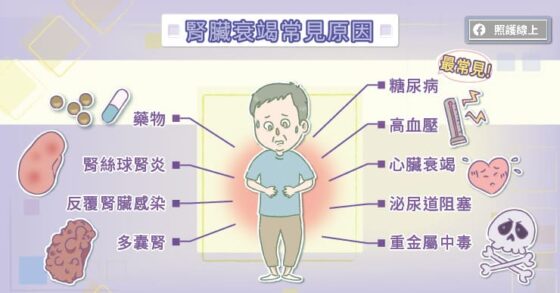
糖尿病、反覆感染、腎絲球腎炎——這些患者可能出現腎臟衰竭
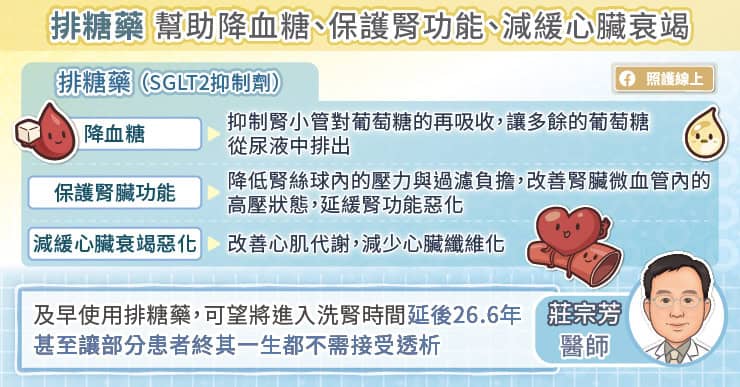
吳明儒教授表示,糖尿病是造成慢性腎臟病最常見的原因,超標的血糖會持續對腎臟造成傷害,進展到腎臟衰竭而需要洗腎的患者中約四成是因為糖尿病。另外還有許多原因可能導致慢性腎臟病,例如高血壓、腎絲球腎炎、反覆腎臟感染、泌尿道阻塞、心臟衰竭、具有腎毒性的藥物、重金屬中毒等。
當腎臟功能惡化到一定程度時,醫師便會建議患者開始為接下來的透析治療做準備,若要接受血液透析,就要建立動靜脈瘻管,若要接受腹膜透析,就要將腹膜透析導管植入腹腔。
另一方面,患者也可以考慮接受腎臟移植的評估,經過一系列完整的檢查,諸如人類白血球抗原測定(Human Leukocyte Antigen,HLA)、群組反應性抗體測定(Panel Reactive Antibody,PRA)、感染篩檢、心肺功能、手術風險等,便能夠登錄至器官捐贈移植登錄中心,列入等待名單。
如果狀況許可,早一點進行腎臟移植對患者愈有利,很多國家不鼓勵洗腎後再移植,他們希望可以在末期腎臟病第五期時就開始評估進行腎臟移植的可能性。這些患者預計會在一、兩年內開始洗腎,若能在洗腎前接受腎臟移植,對患者存活率有幫助。
腎臟剩一顆還可以生活嗎?移植如何進行?
吳明儒教授解釋,腎臟移植的器官來源有大愛捐贈和活體捐贈,大愛捐贈的腎臟數量很有限,每年僅有兩百餘人能獲得配對相符的腎臟。活體捐贈的腎臟能幫助縮短漫長的等待時間。
我們體內有兩顆腎臟,正常狀況下,一顆腎臟就能滿足生理所需,因此有機會進行活體移植。目前的規定必須是患者五等血親以內的親屬或結婚兩年以上的配偶,在經過詳細檢查,評估健康狀態、手術麻醉風險後,可以擔任活體捐腎者。
因為我們的免疫系統會攻擊外來的組織、器官,所以腎臟移植前都必須進行組織配對,以降低排斥反應發生的機會。
目前外科醫師大多會使用腹腔鏡微創手術來取下一顆腎臟,術後疼痛較少、恢復期也比較短。根據研究,活體捐腎者的長期存活率與同年齡層的族群相當,日後罹患末期腎臟病的機會也和一般人相當。隨著手術技術的成熟,活體捐腎者大概能在一個禮拜出院,死亡率約千分之一。
吳明儒教授說,我們很希望民眾能對活體腎臟移植有更多的了解,讓更多洗腎患者有機會接受腎臟移植。
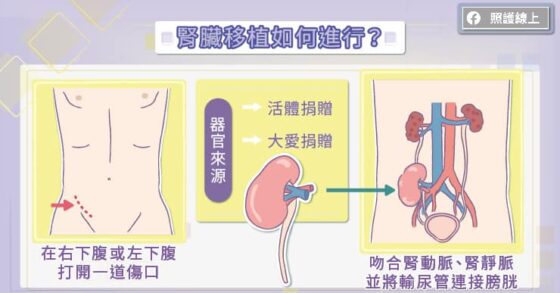
除非有特殊考量,否則在進行移植手術時,通常不會去切除原本失去功能的腎臟。外科醫師會在受贈者的右下腹或左下腹打開一道傷口,小心分離出外髂動脈(external iliac artery)、外髂靜脈(external iliac vein),然後將腎動脈與外髂動脈做吻合,腎靜脈與外髂靜脈做吻合。
完成腎動脈、腎靜脈的吻合後,便能將血流導入新腎臟,讓新腎臟漸漸恢復作用。腎臟移植手術時間大約需要四至六個小時,接受腎臟移植的患者大概會在兩個禮拜出院,出院前的腎功能幾乎能回到醫師可接受的範圍,約莫一個月後能達到穩定的腎功能。
減少排斥!腎臟移植後最重要的一件事——規律服用免疫抑制劑
吳明儒教授提醒,接受腎臟移植後,最重要的是規律服用免疫抑制劑,以減少排斥反應的機會,延長新器官的存活時間。
有些患者在經過幾年狀況都很穩定後,就漸漸沒有規律服藥,而開始出現排斥反應。一旦發生過排斥,身體的免疫系統被激活,往後就容易發作。吳明儒教授強調,規則服用免疫抑制劑非常重要。尤其台灣有不少人屬於快速代謝的基因型,只要忘記吃藥,免疫抑制劑的濃度就可能偏低,而出現問題。
因為服用免疫抑制劑,患者較容易受到各種病毒、細菌、黴菌的感染,例如巨細胞病毒(Cytomegalovirus)、單純疱疹病毒(Herpes Simplex Virus)、腺病毒(Adenovirus)、念珠菌(Candida)、肺結核等,尤其是移植術後前半年的感染風險較高,要留意發燒、咳嗽、腹瀉、頻尿等感染徵兆。請盡量避開人潮,減少感染的機會,飲食衛生也要特別留意。
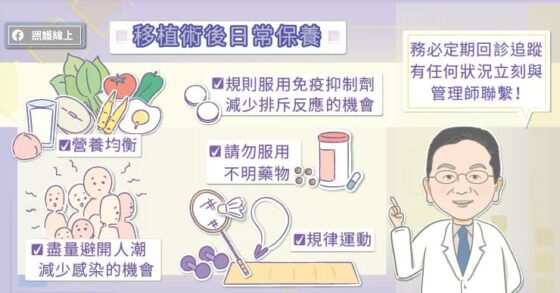
移植腎臟得來不易,務必好好愛惜,切勿服用不明藥物。若有糖尿病、高血壓、高血脂一定要好好控制,以免新腎臟又遭到這些慢性病的破壞。養成良好生活習慣、規律作息、適度運動、均衡營養皆有助於維持體能與整體的健康狀況。
患者必需定期回診追蹤,若發現移植腎有腫痛感、尿量突然減少、水腫、血尿、發燒、倦怠、焦慮不安等狀況,請立刻回醫院檢查和治療!
- 本文轉載自 Care Online 照護線上《腎臟移植重點講解,醫師圖解說明》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接!