熱死人的天氣,你卻身陷人潮中動彈不得。三公尺外的桌上有冰啤酒,你看得到卻拿不到。只能乾瞪眼嗎?那可不,因為你的一群朋友正好站在你和啤酒之間,只要叫他們一個接一個地傳過來就搞定了。有一隊自己人排成的人龍,可以快速把遠方的好東西傳遞到你手上,看你是要冰淇淋,熱狗還是搶贈品都沒問題。
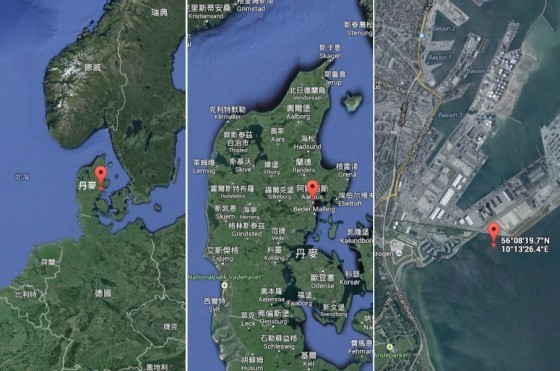
下一個場景我們來到海邊。有湛藍的海水,陽光,和大片燙腳的沙灘。偶爾你會想到找找砂裡的貝殼,或者注意到礁石上的石鼈還有藤壺的奇怪長相。喜歡生物的人大概很少會往海水裡找,更不會有人注意到沉積在大片海水下面的底泥。丹麥的 Lars Peter Nielsen 教授發現了不一樣的東西。他發現在 Aarhus 港的海洋底泥裡有電流在表層和底層間傳送。而且發現這是一個生物現象。為什麼會有生物會跟電流的產生有關係?
電是一種自然界可以取得的能量,不是只會從發電廠裡產生的。夏天常有雷陣雨,電從天上的雲跳到地面上來玩耍就是雷,放出的能量可以把人燒焦。如果我們能在對的時間把電纜掛上對的雲(呃,掛得住的話),或許導出來的電可以讓我們用好一陣子。有沒有生物也可以利用自然的電位差來生活呢?
學過生物學的朋友會知道所有生物細胞都有電子傳遞鏈這個機制,細胞從A分子拉出帶有能量的電子,放進傳遞鏈裡放出能量,再交給B分子帶走。這過程有點像你在超商買了電池,帶回家使用,等電用光了再把這電池送去回收站。這樣一來生物只要有個穩定的電子來源(賣電池的地方),跟一個接收電子的接受者(回收廢電池的地方),就可以持續得到能量,讓自己活下去。如果賣電池的地方和回收電池的地方不是同一個,中間間隔有捷運一站的距離,那為了得到穩定的電源供應,你或許還願意走個十五分鐘去了結這件事。如果這間隔是高鐵一站的距離呢?那大部份人可能就放棄了吧?
大部份的細菌碰到這種狀況也只能放棄。海洋底泥深處是沒有氧氣的厭氧環境,很多細菌活在這裡,利用硫化氫當做燃料來提供能量。Nielsen 教授在 2010 年時在海洋底泥裡發現有電流產生[1]。研究人員發現當底泥上海水裡的氧氣量充足時,數公分深的底泥裡積存的硫化氫會很快被用掉,顯示在數公分深的厭氧區裡生長的細菌,似乎可以用某種方式利用氧氣來接收從硫化氫抽出的電子,以產生能量。令人不解的就是這數公分的距離;這距離對細菌來說就好比我們走到下一個高鐵站的距離,細菌不可能持續來回穿梭數公分來完成這個反應,因為這可是細菌體長的好幾千倍的距離啊。
2012 年的後續研究報告終於揭露了驚人的答案[2]。這些屬於 Desulfobulbaceae 科的新種細菌,原來會自己排成一排,接成一條長龍來連接厭氧區和有氧區,讓在厭氧區的細菌可以抽取在硫化氫裡的電子,一路經過同伴傳送到遠方的有氧區交給氧氣。而在這條線路上合作的同伴個個都能分到好處,更鞏固了這樣的合作行為。如果你有一整隊的朋友排好幫你傳來無限量供應的啤酒,我想每個人在幫你工作的時候,自動地攔截一兩杯滿足自己的需求,應該是很合理的報酬。透過幾千隻同伴的合作,小細菌可以克服體型上的劣勢,能夠利用到環境裡分隔在兩地的資源,成為在資源不足的海洋棲地裡勝出的成功戰略。

今年,Nielsen 教授又追加了兩篇重量級的研究報告〔3, 4〕。他也應邀在今年八月底於韓國首爾舉行的第十五屆國際微生物生態學會年會(ISME15)裡,以電纜細菌(cable bacteria)為題介紹這群特殊的小生物。在今年發表的研究論文裡,他指出這些細菌不只能利用氧氣,在沒有氧氣的時候它們也能改用硝酸根離子來接收電子,讓電流持續產生。這就像你到了個附近沒咖啡廳的環境,只要有便利商店,你一樣可以買到咖啡來讓自己維持在清醒的工作狀態,這樣就擴張了你能繼續工作的空間範圍。他們在實驗室裡測試這些電纜細菌的生長狀況。在 10 天內就可以佈滿 1.5 公分厚的底泥層,21 天後這些”電纜”的總長度已經到達每平方公分裡有兩公里長的線路。他們觀察到這些電纜還會隨時間和深度來調整而逐步加粗。這些細菌真的是很厲害的小小佈線者。

演講中他還提到,自從發現這個有趣的機制後,團隊成員開始到處去尋找厭氧底泥區,看看像這樣的細菌合作關係是不是個普遍存在的自然現象。他們刻意帶了儀器到不同地區的海邊去測電流,連 Nielsen 教授自己家後院的水塘也不放過。他們發現這種有趣的合作關係果然在很多不同的環境都存在。我們人類又搞懂一種細菌在自然環境討生活的絶活了。

進階閱讀
- Nielsen LP, Risgaard-Petersen N, Fossing H, Christensen PB, Sayama M. Electric currents couple spatially separated biogeochemical processes in marine sediment. Nature. 2010 Feb 25;463(7284):1071-4.
- Pfeffer C, Larsen S, Song J, Dong M, Besenbacher F, Meyer RL, Kjeldsen KU, Schreiber L, Gorby YA, El-Naggar MY, Leung KM, Schramm A, Risgaard-Petersen N, Nielsen LP. Filamentous bacteria transport electrons over centimetre distances. Nature. 2012 Nov 8;491(7423):218-21.
- Marzocchi U, Trojan D, Larsen S, Meyer RL, Revsbech NP, Schramm A, Nielsen LP, Risgaard-Petersen N. Electric coupling between distant nitrate reduction and sulfide oxidation in marine sediment. ISME J. 2014 Aug;8(8):1682-90.
- Schauer R, Risgaard-Petersen N, Kjeldsen KU, Tataru Bjerg JJ, B Jørgensen B, Schramm A, Nielsen LP. Succession of cable bacteria and electric currents in marine sediment. ISME J. 2014 Jun;8(6):1314-22.