想像一下,如果有一天,救命的解藥不再僅僅來自大藥廠耗資數十億美元的無塵實驗室,而是出自你家客廳的一台筆記型電腦?這聽起來像極了科幻電影的瘋狂劇本,卻是一個為了挽救愛犬性命,真實上演的科學奇蹟。
這場「素人對抗癌症」的戰鬥,不只徹底打破了我們對醫療邊界的認知,更像一顆投入靜水中的巨石,激起的漣漪正迅速蔓延到整個人類醫學、長壽社會與個人健康責任的論述核心。今天,就讓我們來拆解這場傳奇救犬記背後的科學邏輯,看看「生物可程式化」的時代如何悄悄降臨。
一隻狗、一位工程師,與一個不肯認輸的決定
故事的主角是澳洲軟體工程師 Richard Sutherland。他領養了一隻曾有創傷歷史的柴犬 Kuma,Kuma 很快成了他生命中不可或缺的夥伴。然而在 2023 年,Kuma 被確診為高度惡性的「肥大細胞瘤」(Mast Cell Tumor, MCT),這是犬類中最常見也最兇猛的皮膚惡性腫瘤。獸醫遺憾地告知,即便進行手術與化療,Kuma 存活的時間恐怕也只剩幾個月。
面對死神的宣判,Sutherland 拒絕單純等待奇蹟。身為工程師,他本能地選擇了另一條路:定義問題,然後寫出解法。他動用了約 3,000 美元(約台幣十萬元)的個人積蓄,委託商業基因體公司對 Kuma 的腫瘤組織進行了「全外顯子組定序」(Whole Exome Sequencing, WES)。
這項技術專門聚焦於基因組中實際被轉譯成蛋白質的那 1-2% 編碼區域。相較於昂貴且龐雜的全基因組定序,WES 更適合用來尋找腫瘤的「體細胞突變」。但問題來了,取得幾十 GB 的原始定序數據後,一個沒有生物醫學背景的工程師,該如何在超過兩萬個基因的龐大變異資料中,揪出那幾顆真正驅動癌症的「子彈」?
科學的鑰匙:ChatGPT、AlphaFold 與 mRNA 的三重奏
這不是盲目的嘗試,而是一場精密的科學工程。Sutherland 其實正踏在目前全球頂尖生技公司(如 Moderna、BioNTech)積極推進的「個人化新抗原疫苗」(Personalized Neoantigen Vaccine)研發前線上。他靠著三件神器,完成了這項不可能的任務。
步驟一:用 ChatGPT 尋找「新抗原」
癌細胞突變會產生原本不存在於正常細胞的異常蛋白質片段,如果這些片段能呈現在細胞表面被免疫系統識別,就稱為「新抗原」(Neoantigen)。要成為有效的靶標,突變必須夠多、必須能與個體的 MHC(主要組織相容性複合體)緊密結合,還要能活化 T 細胞去毒殺癌細胞。
Sutherland 利用 ChatGPT 作為他的「智識介面」,協助撰寫 Python 腳本、整理與篩選突變資料。雖然 AI 本身不是生物資訊引擎,但它強大的代碼輔助與文本推理能力,大幅降低了門檻,讓他得以建構出原本需要博士級專家才能完成的分析管線。
步驟二:AlphaFold 的蛋白質立體建模
找出潛在的新抗原後,必須確認它的「形狀」真的和正常蛋白質不同。這時,DeepMind 劃時代的 AI 工具「AlphaFold 2」登場了。過去需要耗資百萬、耗時數年的蛋白質結構解析,現在只需要網路連線,幾分鐘內就能精準預測立體折疊結構。Sutherland 藉此確認了突變蛋白確實能作為疫苗的標靶。這證明了一件事:結構生物學被徹底民主化了。
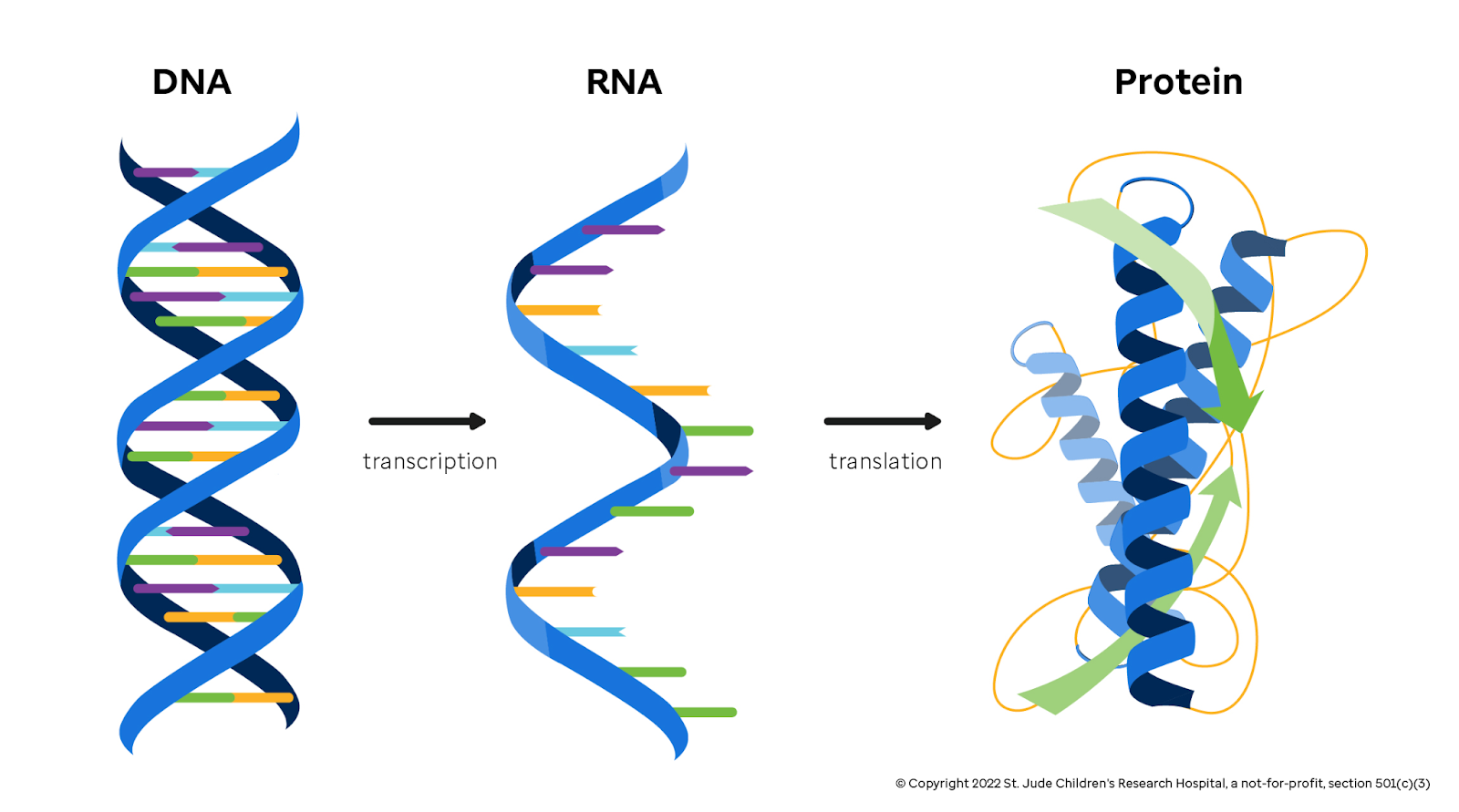
步驟三:客製化 mRNA 疫苗上陣
目標確認後,他設計了一段對應的 mRNA 序列。這段序列就像是一張發給免疫系統的「通緝令」,注射進體內後會教導細胞製造這些腫瘤特徵蛋白,啟動免疫系統追殺帶有相同特徵的癌細胞。在取得獸醫主管機關的「特殊人道同情豁免」許可後,這劑客製化疫苗被施打在 Kuma 身上。幾週後,奇蹟發生了:Kuma 的腫瘤開始縮小,活力也逐漸恢復。
醫療典範轉移:從「大數法則」到專屬於你的「N-of-1」
傳統藥物開發是建立在「統計多數」上的,尋找對「平均患者」有效的療法。但現實是,每個人、每顆腫瘤都是獨特的,這就是為何同一種化療對某些人有效,對另一些人卻毫無作用(即腫瘤異質性)。
Sutherland 的做法,展現了未來的「N-of-1 醫療」:臨床試驗的樣本數不是一萬人,而是「一個人」(或一隻狗)。隨著基因定序成本崩跌、AI 分析能力平民化,以及 mRNA 合成技術的成熟,這種「不找萬能藥,只為你打一把專屬鑰匙」的醫療模式,正逐漸從實驗室走向現實。
長壽社會的挑戰:成為自己身體的守護者
台灣即將在 2025 年邁入超高齡社會,活得長已是常態,但「活得好」才是考驗。當醫療技術逐漸軟體化,癌症或許將從「絕症」轉為可管理的「慢性病」。未來我們甚至能定期更新癌症疫苗,維持免疫系統對腫瘤的監控。
Kuma 的故事揭示了一種全新的主體性:我們不應再只是被動接受治療的患者。借助智慧穿戴裝置收集生理數據、了解自身的基因風險,並透過 AI 輔助整合健康資訊,每個人都可以成為自己健康的「共同決策者」。醫師的角色也將從「知識的壟斷者」轉變為「認知的橋接者」,協助我們辨識偽科學,共同制定健康策略。
技術民主化的光明與陰影
當然,我們不能忽視這場革命帶來的風險。Sutherland 的成功發生在法規相對彈性的獸醫領域,若在人體上進行,未經監管的「生物駭客」(Biohacking)行為將帶來極大的安全隱憂。此外,個人基因數據的隱私保護、以及高昂技術可能加劇的「健康貧富差距」,都是社會必須迫切面對的倫理挑戰。
Kuma 的故事不是終點,而是一個時代的預告。醫療的邊界正在被那些拒絕等待、選擇親手書寫解方的人們重新定義。活得長是科技的恩賜,但活得有尊嚴、有主體性,則需要我們每一個人的覺醒。或許未來的某一天,你的健康,就掌握在你親手敲下的那一行代碼裡。
參考資料
- Alexandrov, L.B., et al. (2013). Signatures of mutational processes in human cancer. Nature, 500, 415–421.
- Jumper, J., et al. (2021). Highly accurate protein structure prediction with AlphaFold. Nature, 596, 583–589.
- Reynisson, B., et al. (2020). NetMHCpan-4.1 and NetMHCIIpan-4.0: improved predictions of MHC antigen presentation by concurrent motif deconvolution and integration of MS MHC eluted ligand data. Nucleic Acids Research, 48(W1), W449–W454.
- Sahin, U., et al. (2017). Personalized RNA mutanome vaccines mobilize poly-specific therapeutic immunity against cancer. Nature, 547, 222–226.
- Marusyk, A., et al. (2012). Intra-tumour heterogeneity: a looking glass for cancer? Nature Reviews Cancer, 12, 323–334.
- Tie, J., et al. (2016). Circulating tumor DNA analysis detects minimal residual disease and predicts recurrence in patients with stage II colon cancer. Science Translational Medicine, 8(346).
- Karikó, K., & Weissman, D. (2005). Suppression of RNA recognition by Toll-like receptors: the impact of nucleoside modification and the evolutionary origin of RNA. Immunity, 23(2), 165–175.