- 作者/照護線上編輯部
- 本文轉載自 Care Online 照護線上《肝硬化讓肝癌風險暴增!B型肝炎的病程與治療,醫師圖文解說》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接

「20 年前,我們團隊開始到社區進行肝病篩檢,第一次把腹部超音波搬出醫院。」,高雄醫學大學附設中和紀念醫院肝膽胰內科余明隆教授回憶,「當時共出動 12 位醫師和 4 台超音波去梓官鄉,一天做了 1,000 個腹部超音波,就發現兩位肝癌患者,一位是 C 型肝炎帶原者,一位是 B 型肝炎帶原者。」
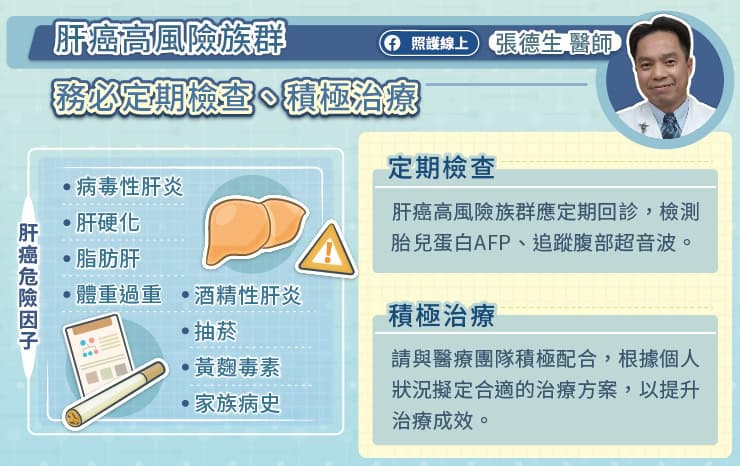
那位患者知道自己有 B 型肝炎帶原,但是從來沒有追蹤。當時只是打算順便做個檢查,結果意外發現罹患肝癌,非常震驚。余明隆醫師提醒,B 型肝炎帶原者一定要定期追蹤、治療,不能輕忽!
B 型肝炎傷肝又致癌
B 型肝炎有兩個主要傳染途徑,余明隆醫師指出,一個是媽媽傳給小孩子,母子垂直感染,另外一個是經由血液、體液感染,例如藥物毒癮者、不安全性行為等。
小時候得到 B 型肝炎病毒後,會有大概 20 年的「免疫耐受期」,在這 20 年當中,可以測到 B 型肝炎病毒,但是肝指數都正常,肝臟組織也沒有發炎。余明隆醫師解釋,隨著人體免疫系統的成熟,B 型肝炎就會開始發作,進入「免疫清除期」,我們的免疫系統會去攻擊遭到感染的肝細胞,造成肝臟反覆發炎,被稱為慢性 B 型肝炎。
在免疫清除期中,有些人比較幸運,免疫系統會漸漸抑制 B 型肝炎病毒,甚至可以把 B 型肝炎病毒全部清除掉,但是機會很低,每一百個人裡面,每一年只有一個人可以清除病毒,余明隆醫師說,大部分患者的肝臟會持續發炎,造成肝臟破壞,大概有五分之一的病人會變成肝硬化,一旦肝硬化形成以後,大概每一年就有 1% 至 4% 的機會會產生肝癌。終其一生,有大概五分之一肝硬化的病人會走進肝衰竭、末期肝病變。
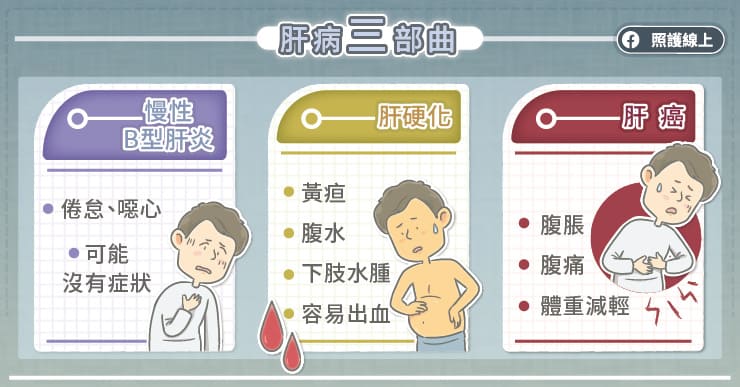
慢性肝炎、肝硬化、以及肝癌就是我們常說「肝病三部曲」。
「Child 氏肝臟殘存功能分類表」評估肝硬化
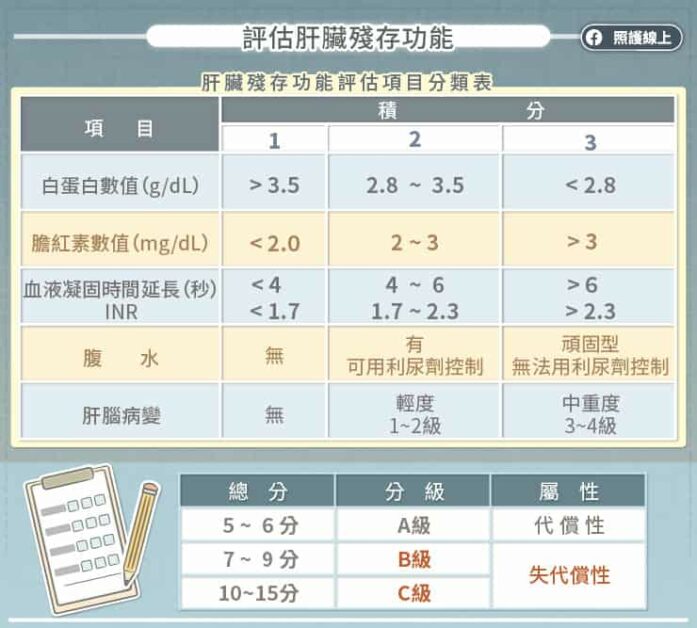
肝硬化的嚴重程度可根據「Child 氏肝臟殘存功能分類表」分為三期,主要評估 5 個項目,分別是血中的白蛋白、血中的膽紅素、血液的凝血機能、是否有腹水、是否有肝腦病變。
- 「白蛋白」由肝臟製造,肝臟功能越差,血液中的白蛋白就越低,分數也越高。
- 「膽紅素」主要由肝臟代謝,肝臟功能越差,血液中的膽紅素就越高,黃疸越嚴重,分數也越高。
- 「凝血機能」與肝臟製造的多種凝血因子有關,肝臟功能越差,凝血功能就越差,分數也越高。
- 「腹水」在肝功能惡化時會越來越多,腹水越多,分數越高。
- 「肝腦病變」與血液中的肝毒素有關,肝臟功能越差可能造成意識改變、中樞神經障礙,肝腦病變越嚴重,分數越高。
把各項分數加起來,總分 5~6 分為 Child 氏 A 級,屬於「代償性肝硬化」;總分 7~9 分為 Child 氏 B 級,開始有肝衰竭的現象;總分 10~15 分為 Child 氏 C 級就要考慮進行肝臟移植,B 級和 C 級都屬於「失代償性肝硬化」。
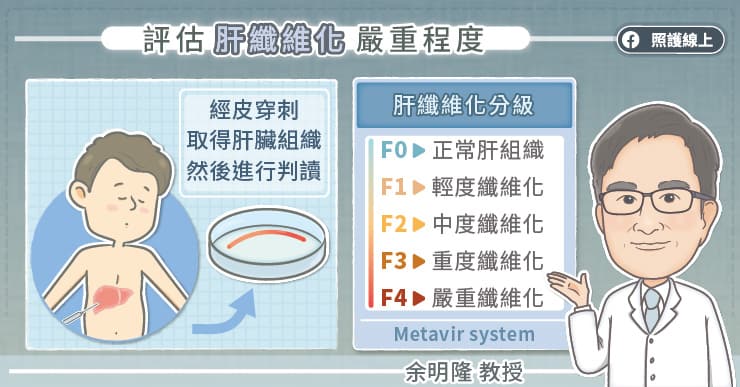
在 B 型肝炎的病程中,會從慢性肝炎進入肝硬化,余明隆醫師說,我們可以利用穿刺的方法取得少量肝臟組織,交由病理科醫師判斷肝臟纖維化的嚴重程度。肝臟纖維化的嚴重程度可分成 5 級,F0 是沒有肝纖維化、F1 是輕度纖維化、F2 是中度纖維化、F3 是重度纖維化、F4 是嚴重纖維化。
較簡易的方法是使用腹部超音波評估肝硬化的狀況,不過超音波僅能預估,余明隆醫師說,現在有肝纖維化掃描儀,利用震波能夠較具體的量化肝臟纖維化的程度。肝纖維化掃描儀屬於非侵入性檢查,便利性高、安全性高、也沒有疼痛感,是實用的檢查工具。
B 型肝炎的治療是非常重要的議題,余明隆醫師解釋,如果處在免疫耐受期,肝指數都正常,肝臟沒有遭到破壞時,患者不需要接受治療。因為接受治療的效果也不好,所以沒有必要接受治療。如果已經進入不活動期,病毒量很低、肝指數正常,也不建議接受治療。
接受治療的黃金時期就是在免疫清除期,余明隆醫師說,首先要評估肝臟纖維化程度、血中病毒量與肝指數。
如果肝臟纖維化程度是 F0 到 F2,會在血中 B 型肝炎病毒量達 2,000 IU/mL 以上,且肝指數達正常值上限 2 倍以上才需要治療。
如果肝臟纖維化程度是 F3,在血中 B 型肝炎病毒量達 2,000 IU/mL 以上,且肝指數異常便需要治療。
如果肝臟纖維化程度是 F4 至 F5,只要血中有 B 型肝炎病毒存在,都應該要馬上接受治療。
貼心小提醒
B 型肝炎帶原者可能沒有明顯症狀,但是會在不知不覺中進展為肝硬化,甚至產生肝癌,余明隆教授叮嚀,只要不清楚自己是否帶原,都建議要接受篩檢,若已有帶原,務必要定期追蹤,適時介入治療,降低肝硬化及肝癌的機會!
- 歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接