- 作者/愛姆斯的醫材藥品法規世界
協作及審閱/Jeff Hsu
Moderna 的 RNA 疫苗有什麼特別的地方?
今年 5 月中旬有一天,道瓊指數一日暴漲了 900 點,因為位在波士頓的 Moderna 公司開發新冠肺炎疫苗 (mRNA-1273) 的臨床 I 期數據表現亮眼1,Moderna 市值也瞬間衝上 290 億美金。然而媒體引用多位免疫學專家說法指出,該公司的說辭中實際缺乏關鍵資料,數據不足且不夠透明等等,又導致其股價連跌三天,且跌幅達到 20%。那通過了臨床 I 期的 Moderna 新冠肺炎疫苗能否繼續突圍,最快也將會在七月揭曉二期臨床數據。
為什麼一家新銳生技公司的疫苗可以撼動這個市場甚至是全世界?讓我們來一窺究竟。
傳統常見的疫苗區分為活性減毒或非活性
活性減毒疫苗:
利用培養技術製造出的活體微生物,在製程中利用添加化學藥劑、改變遺傳物質、重複繼代培養或是施以物理變化的方式,以得到有病原特徵卻無致病力的的病源品種。但因為是活性病源,還是有機率突變生成致病力,卡介苗和口服小兒麻痺疫苗等都屬於這個類別。
非活性疫苗:
透過熱或化學藥劑殺死、或破壞致病微生物的結構,去除病原的致病力,但因部分結構仍然完整,可誘起免疫反應,以達到疫苗接種之目的,日本腦炎疫苗和白百破疫苗皆在此列。
Moderna 所開發的疫苗則是新式疫苗,且屬於 RNA 疫苗。近年來RNA疫苗的開發主要是偏重在感染疾病和癌症,運用病原體特定部份組成對應的 RNA 片段,經過修飾後送入人體,在人體中轉譯成能使人產生免疫反應的抗原蛋白,免疫細胞學習過後,便能夠辨識並對抗侵入的特定病毒。
RNA 疫苗和傳統疫苗不同之處在於,它的製程更快、花費更便宜,而且 RNA疫苗其實更安全,因為它們組成物不具致病性。RNA疫苗可以標準化大量生產,因此可以在大規模疫情下,快速量產。近年來 RNA疫苗的開發主要是偏重在感染疾病和癌症上面。
有潛力、可快速量產、不曾正式上市的 RNA疫苗
Moderna 所開發的相關產品有 20 種左右,目前還沒有任何一種產品得到監管單位批准,進度最快的產品 (CMV) 也只進行到臨床二期。即便如此,RNA 疫苗仍被視為極具潛力的一種技術。2
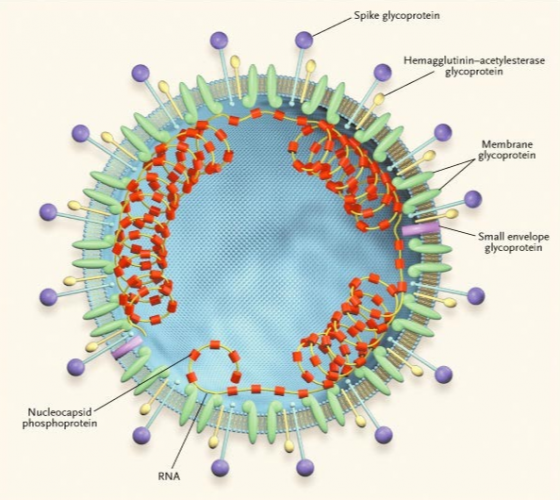
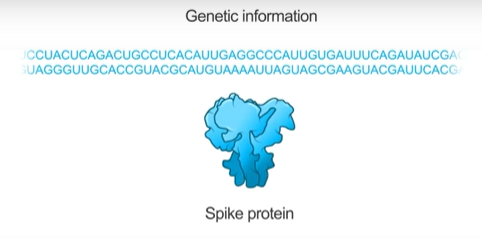
Moderna 的 mRNA-1273 疫苗便是利用新冠病毒外殼上的棘蛋白 (Spike glycoprotein; Spike protein),又稱 S 蛋白的RNA來製成疫苗。S 蛋白是病毒感染宿主細胞的關鍵結構,也因此成為藥物或疫苗開發的重要標靶位置。帶有 S 蛋白的 mRNA 進入人體細胞轉譯成 S 蛋白後,使經由免疫細胞辨識後產生中和性抗體,以避免將來可能的新冠病毒感染。3
Moderna 官網的新冠病毒疫苗原理介紹影片:3
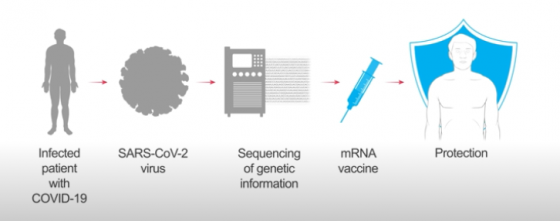
RNA疫苗的設計概要:
- Moderna 和 NIH 的科學家從公開的新冠病毒的基因體資料庫中,找出疫苗的關鍵候選物質 S 蛋白的基因序列
2. 利用該基因 DNA 序列做出對應 mRNA
3. 再將此mRNA做成疫苗注射進入人體
4. 免疫細胞對mRNA轉譯成的S蛋白進行辨識,產生免疫反應
完成第一期臨床,離上市還有多遠?
簡單來說疫苗的臨床試驗中,分成三期 (I、II、III)。5
- I 期臨床:20-100 位健康受試者,主要測試在測試疫苗是否安全、是否有副作用,以及副作用和劑量之間的關係。
- II 期臨床:受試者較 I 期多,約莫數百人。主要測試疫苗最常見的短暫副作用,以及受試者的免疫系統對疫苗的反應。
- III 期臨床:受試者受試者較 I、II 期多,會有幾百到幾千人。主要測試疫苗安全性和有效性,以及最常見的副作用。

Moderna 在 5 月所發表的實驗結果正是 I 期臨床的資料。
結果顯示受試者共 45 人在三個不同劑量組別中,兩個低劑量組別中的 8 人均檢測出中和性抗體,佔全體受試者的 17.8%,目前疫苗開發也已經順利進到第 II 期臨床試驗。
但自從 Moderna 公佈了 I 期臨床資訊後,就有學者出面質疑;媒體 STAT News 也指出單憑 Moderna 提供的資料並無法判斷疫苗真的有效與否6,股價又瘋狂的跌了三日。
所以是 Moderna 對還是 STAT 對?
兩者都沒有錯,因為 I 期臨床最重要的是在測試安全性而不是在有效性。
所以哈佛學者在STAT說不能單就這些新聞稿就認為這支疫苗是有用的,這質疑沒問題。Moderna說他們的 I 期實驗數據沒問題,已進入臨床 II 期了,這也是事實。
但如果說非常亮眼嘛,下個階段完成再來說也不遲。我們耐心等一下臨床 II 期資料出爐後就可以知道是怎麼回事了,因為雙方都不知道結果會是如何(Moderna可能知道的多一點或是少講了一些關鍵資訊)
從過去紀錄來看看,疫苗研發成功機率有多高?
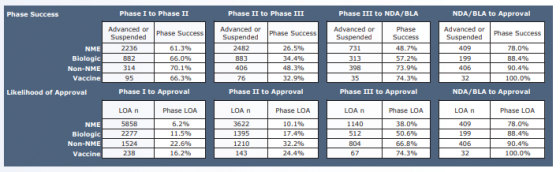
首先我們來看,疫苗臨床一期成功了,可以說明什麼呢?在這裡讓我們瞧瞧一些數字。這是根據世界最大的生技貿易組織,Biotechnology Innovation Organization, BIO)在2006年至2015年研究得到的資料。7
疫苗從臨床一期到最終拿下上市許可證的成功率:16.2%
那疫苗在臨床一期的成功率大約是多少呢?66.3%
也就是說 Moderna 疫苗公佈的 I 期臨床數據,其實本來就已經有三分之二的成功機會。
至少現在算是臨床二期了,那它的成功率是多少呢?
臨床二期到批准的成功率,聽起來好一點:24.4%
大約是四分之一的機會最終會成功。
而單單就臨床二期的成功率:32.9%
也就在二期時有三分之二的疫苗會栽在這裡。
以上的數據係由所有疫苗合併計算得出,但也許你會思考到,有些類型的疫苗(例如癌症疫苗)失敗率本就極高,合在一起看會失準。
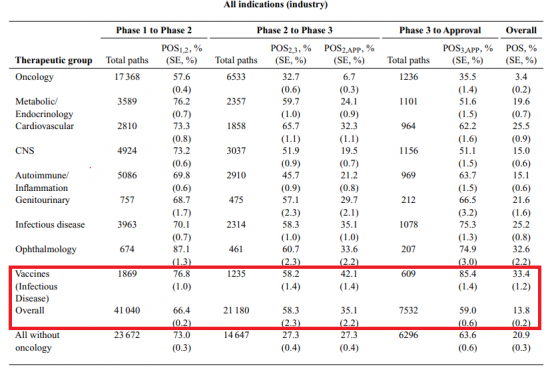
美國麻省理工學院 (MIT) 論文顯示,在 2000 年到 2015 年間,感染疾病疫苗在所有疫苗中成功率已屬最高,但臨床到最後批准的成功率也只有 33.4 %(至於癌症疫苗只有 3.4%)。
即使過了臨床 I 期,疫苗亦非穩操勝算,臨床 II 期是才是陣亡率最高的階段。
MIT 數據顯示,疫苗進入臨床 II 期後上市機率為 42.1%,雖不到五成,但和其他各種治療方式相較下,疫苗的最終核准成功率算是高的。其中傳染病疫苗 II 期成功率約莫落在 58.2% ,表示研發人員有超過一半的機會見到其成功。
II 期臨床之所以屬於三個階段中失敗率最高者,主要因為在臨床 II 期,受試者數量會提升到數百人,除了招募難度變高之外,隨著受試者增加,也可能出現更多的副作用和不良反應。此外,這個階段最重要需要觀察的面向在於,疫苗是否能使人體產生免疫反應,這是臨床 II 期最容易失敗之處。
Moderna 現在正式邁入最困難的臨床試驗階段,Moderna 能不能克服難關值得觀察下去。若順利,Moderna 最快很有可能在七月邁入三期臨床試驗。
無論如何,都希望 Moderna 的這支 RNA 疫苗能成功,除了可以改善疫情之外,這支疫苗的成功,也會開啟疫苗的新頁,代表著一種革命性的新技術應用在疫苗領域。
Moderna 7 月 14 日在新英格蘭醫學期刊上正式公佈了他們的 I 期臨床數據9
- 作者/愛姆斯的醫材藥品法規世界,愛姆斯有超過十年醫藥法規經驗,工作經驗遍及海內外生技藥品臨床醫材公司。
- 協作及審閱/Jeff Hsu,東海大學生科系學士,美國南加大 USC 微免所碩士,具多年美國生技藥廠及醫材的法規經驗。
參考文獻
- Moderna Announces Positive Interim Phase 1 Data for its mRNA Vaccine (mRNA-1273) Against Novel Coronavirus by Moderna
- Moderna’s Pipeline by Moderna
- Moderna’s Work on a COVID-19 Vaccine Candidate by Moderna
- 新英格蘭醫學期刊COVID-19結構圖
- 美國疾管局(CDC),介紹疫苗開發流程 by CDC
- HelenBranswell. Vaccine experts say Moderna didn’t produce data critical to assessing Covid-19 vaccine STAT (May.19, 2020)
- Clinical Development Success Rates 2006-2015 by BIO
- Estimation of clinical trial success rates and related parameters by MIT
- Moderna於新英格蘭醫學期刊公佈其臨床一期資料
- Moderna於官網公佈臨床II期結束,準備開始臨床III期試驗


 2. 利用該基因 DNA 序列做出對應 mRNA
2. 利用該基因 DNA 序列做出對應 mRNA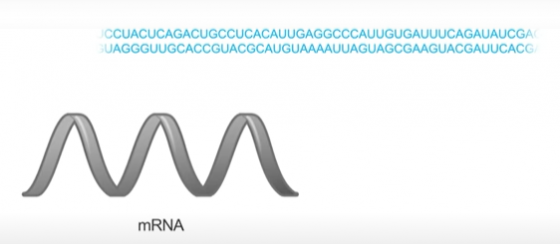 3. 再將此mRNA做成疫苗注射進入人體
3. 再將此mRNA做成疫苗注射進入人體 4. 免疫細胞對mRNA轉譯成的S蛋白進行辨識,產生免疫反應
4. 免疫細胞對mRNA轉譯成的S蛋白進行辨識,產生免疫反應