- 作者/照護線上編輯部
- 本文轉載自 Care Online 照護線上《癌症治療新頁 生物相似性藥》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔!

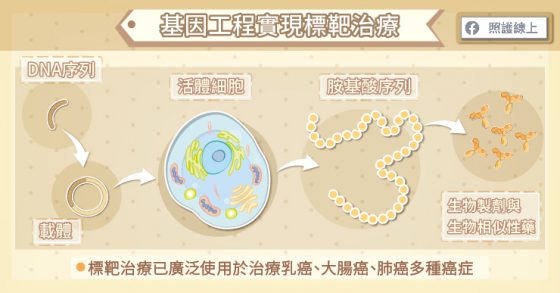
近年來,受惠於基因工程的進步,標靶治療已被廣泛使用於治療乳癌、大腸癌、肺癌、頭頸癌、多發性骨髓瘤等多種癌症,標靶治療藥物能與特定細胞標記結合以達到抑制癌細胞生長的目的,屬於較精準的治療機轉,因此稱為標靶治療,是現代精準醫療重要的一環。
羅東博愛醫院醫療副院長葉顯堂醫師指出,標靶治療藥物是由活體細胞所製造的生物藥物,與化學反應合成的藥物大不相同。需要先將一段特定的 DNA 序列透過載體植入活體細胞,活體細胞會根據 DNA 序列製造胺基酸序列,然後組成生物藥物,也稱之為單株抗體。
什麼是生物相似性藥?
葉顯堂醫師解釋,要了解什麼是生物相似性藥,需要從生物藥物解釋起。
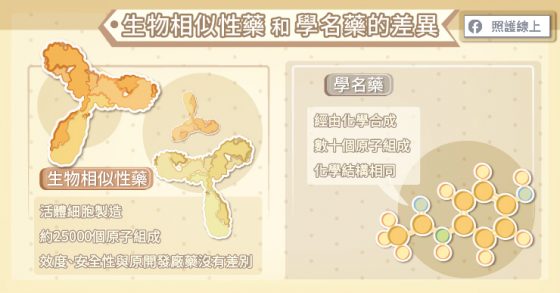
生物藥物是由一系列胺基酸所組成有 4D 結構,其分子量較大,可能高達 150,000 g/mol,是化學藥的一千倍,製造過程複雜度遠高於合成化學藥物,製作生物藥物牽涉到基因工程,藉由活體細胞株生產,每個生物藥會有不同的關鍵品質屬性(Critical Quality Attribute,CQA),關鍵品質屬性關係到這個生物藥的功能,功能不同,所產生的療效、安全性亦不相同。
當原開發廠所生產製造的生物藥上市一段時間後,專利期限也會隨之過期。此時,即可開放其他有生產生物藥能力的藥廠,自行研究製造相似的生物藥,稱為「生物相似性藥」。
台灣食品藥物管理署(TFDA)、美國食品藥物管理局(FDA)、歐洲藥物管理局(EMA)在核准生物相似性藥時都是基於一個原則:生物相似性藥的效度、純度、安全性,在臨床使用上與原開發廠生物藥物(或稱為:參考藥品)是沒有差別的。
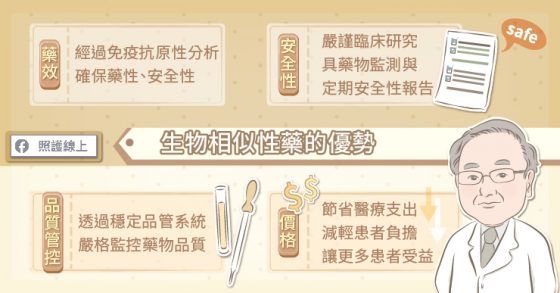
生物藥物是活體細胞的產物,即使是同一間藥廠,採用相同製程,每一批出廠的生物藥物都不見得完全相同,因此所有的生物藥物需要持續監控,以確保品質,不同藥廠生產的生物相似性藥亦是如此。生物相似性藥是經由分析多批原開發廠生物製劑以建立基準,藉由活體細胞經過複雜且精細的多重步驟程序,透過繁複的定性分析、臨床前試驗、臨床藥動學與第三期臨床試驗,以確保生物相似性藥臨床使用的療效、安全性及免抗原性,保障患者用藥選擇權。
生物相似性藥在世界各國的使用情況為何?
葉顯堂醫師表示,目前台灣食品藥物管理署核准的生物相似性藥有好幾類,包括治療多項癌症、類風濕性關節炎、乾癬等。
歐盟約在 2006 年開始有生物相似性藥進入臨床使用,目前已有 15 個生物藥物及數十個生物相似性藥,而每一種生物藥物可能都有好幾間藥廠在製造生物相似性藥。近年來,美國也有越來越多的生物相似性藥可供選擇,例如治療乳癌常用來對抗 HER2+的標靶藥物,也已有五項生物相似性藥被核准。
而台灣食品藥物管理署(TFDA)針對癌症標靶治療,目前也核可數個生物相似性藥,提供罹患 HER2+陽性乳癌、非小細胞肺癌、大腸直腸癌、胃癌、子宮頸癌、惡性神經膠質瘤會者在治療時的治療新選項。此外,目前癌症領域常用的國際治療指引中,也已將生物相似要列入患者治療的選項之一,在國外生物相似性藥,也已經有多年的使用經驗。
生物相似性藥的優點有哪些?
「與化學治療相比較,生物藥物有更高的專一性,能減少副作用的發生,而且可以提升治療成效。」葉顯堂醫師說明,「然而,生物藥物的製程複雜,所以價格較高。生物相似性藥累積多重的臨床試驗與臨床經驗,且藥價較低的優勢,有助減輕醫療費用的負擔,讓更多患者有機會接受標靶治療、有更好的預後,並減少復發的風險。」
生物相似性藥對台灣整個醫療環境也有相當的好處,當生物相似性藥被更多人使用,患者在治療疾病的同時,也為國家整體醫療省下一些經費,進一步用來幫助更多新的藥物納入給付,幫助更多的人。
目前生物相似性藥的核准條件是需要通過人體試驗,以證明其藥性、安全性與參考藥物相同。
了解生物相似性藥,讓更多患者受惠
葉顯堂醫師分享,世界衛生組織持續呼籲,各國應該加快腳步整合生物相似性藥上市的可能性,主要希望透過生物相似性藥的加入與廣泛採用,讓民眾能夠更加容易地獲得具相同療效、安全性的標準治療,同時節省醫療花費,對患者以及整體醫療環境都有幫助。
不過在使用生物相似性藥方面,仍需要讓患者有更多了解與認識,畢竟生物藥物是近年來發展出的藥物,大家對於生物相似性藥自然較為陌生,容易產生誤解。
葉顯堂醫師強調,生物相似性藥並非學名藥,必須通過相當嚴謹的監控及把關,以確認效果及安全性。擁有臨床使用經驗的醫師也應該多多與醫界分享,傳遞正確的醫學知識,讓患者、家屬能透過醫師更了解生物相似性藥的製造及核准流程,便能有更多的信心。
生物藥物是近代醫學的重大進展,讓許多疾病的治療成效顯著提升,期望生物相似性藥的問世也能讓更多的患者受惠!