本文轉載自中央研究院研之有物,泛科學為宣傳推廣執行單位
- 採訪編輯|林承勳、美術編輯|林洵安
從 1982 年開始,癌症一直是我國十大死因之首。根據衛生福利部統計資料顯示,2018 年將近五萬人死於癌症,高達總死亡人口百分之二十八。癌症如果早期發現,大多能夠有效治療、恢復,當癌症進入晚期、開始轉移之後,可就凶多吉少。
好消息是,中研院生物醫學科學研究所陶秘華研究員指出,近年來癌症免疫治療 (cancer immunotherapy) 的進步,可增加癌症晚期病患的治癒率,跟著「研之有物」 一起來了解!
癌症晚期為什麼棘手?
癌症 (Cancer) 或稱作惡性腫瘤 (Malignant tumor),源自身體某個部位開始有細胞不正常的增生。腫瘤形成之後,可能從原本部位向周圍組織擴張,藉由淋巴和血管,轉移到身體的其他部位。大量癌細胞沒有限制地瘋狂生長,破壞重要器官功能,也佔據身體大部分的營養,導致病患最終因器官衰竭、營養不良、併發症而死亡。
所幸,早期癌症只要被診斷出來,藉由手術切除、輔以局部放射治療,很有機會徹底消滅癌細胞。但如果癌細胞已經入侵淋巴結、血管並向外擴散,甚至轉移到身體其他部位,不論手術、化學療法、標靶治療,療效皆有限。
約有百分之九十癌症病人死於轉移癌,而非原位癌。
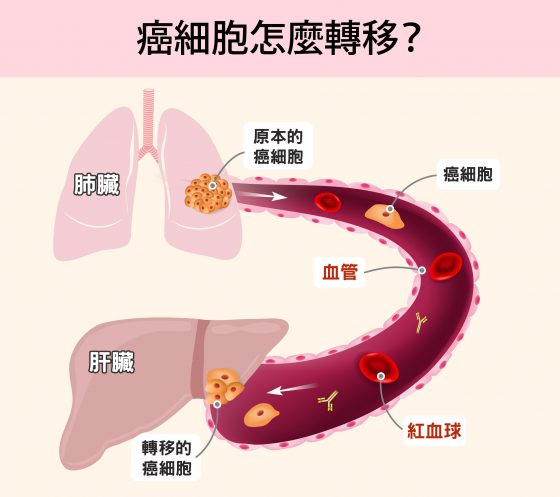
治療轉移癌的困難在於,即使手術切除了可見腫瘤,仍可能有少數癌細胞早已轉移到身體其他部位。根據臨床病例,肺跟肝是轉移癌常發生的區域,但每位病患情況不同,醫生難以判斷癌細胞往哪裡跑,只能用化學或是標靶治療,給予病患全身性的藥物,造成身體沉重的負擔。
更嚴重的是,即使當下控制住了,腫瘤仍具有很高的復發風險。因為癌細胞會突變,對化學治療和標靶治療的藥物產生抗藥性,導致藥物無法繼續控制。 陶秘華舉例:「像原本認為已經治癒的乳癌病患,甚至還有在 25 年後復發的例子。」
癌症免疫療法,正可彌補這些傳統療法的不足。免疫療法是訓練人體自己的免疫系統攻擊癌細胞,當癌細胞突變、變得與正常細胞不同,反而更容易被免疫系統偵測辨識,達到徹底殲滅癌細胞的目標。
事實上,免疫系統與癌細胞的戰役,每天都在你我身上開打!
人人身上都有癌細胞,卻不是人人都得癌症:關鍵在免疫系統
「每一個人」身上都會出現癌細胞。人體內細胞不斷複製增加,染色體複製的過程中,基因就可能發生突變,突變的累積會使正常細胞變成癌細胞;另外,人體外的幽門螺旋桿菌、B 型肝炎病毒、陽光中的紫外線、食物中的亞硝胺等,也都有機會促進細胞突變。
現代人壽命持續延長,根據內政部統計,國民平均壽命目前已達創新高的 80.4 歲(男性 77.3 歲,女性 83.7 歲),意味著人體細胞有更長時間接觸前述致癌因素,癌細胞出現機率更勝以往。
不過,每個人身上都有癌細胞,卻不是人人都會得癌症。
癌症發生的關鍵,在於人體的免疫系統!
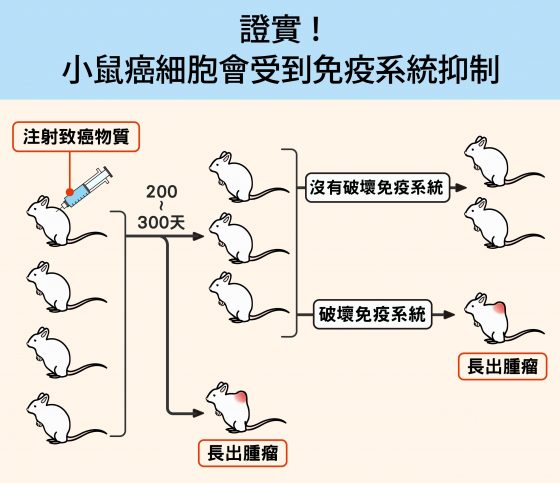
全球最具名望的科學期刊《自然》(Nature),在 2007 年刊載一篇研究論文,證實了健康生物體內的癌細胞會被免疫系統抑制。方法是:研究人員先對一群健康小鼠注射致癌物質,經過半年多,發現只有少數小鼠罹癌,大部分仍然很健康。
於是研究人員提問: 這些健康小鼠體內是否也有癌細胞? 如果有,為什麼不發病?是因為免疫系統提供的保護嗎?如果答案是肯定的,那麼破壞小鼠的免疫系統,是否會引發癌症呢?
他們破壞小鼠的細胞性免疫系統,尤其是 T 細胞免疫,結果約一半的小鼠長出了腫瘤。「這個實驗證實,接觸致癌物的小鼠體內確實出現癌細胞,只是被免疫系統控制住了。」陶秘華解釋。
原來當身體出現癌細胞,就會引發免疫系統發動攻擊!例如:有一種稱為殺手 T 細胞 (Cytotoxic T cell) 的免疫細胞,會辨識癌細胞或被病毒感染的細胞,再將含融解酶的顆粒注射到癌細胞,沒多久癌細胞表面出現破洞、逐漸凋亡。
不過,「物競天擇,適者生存」也適用癌細胞。雖然大多數癌細胞一出現即被殲滅,仍可能有少數躲過免疫細胞追殺、緩慢地增殖,經過數年、甚至十多年的漫長時間,演化出許多抵抗免疫系統的奇招,最終發展成免疫系統再也無法控制生長的腫瘤。「認真說起來,其實腫瘤的生長歷程也是很艱辛的。」陶秘華打趣的說。
簡言之,腫瘤能驅逐、消滅外圍的殺手 T 細胞,同時讓腫瘤內部的免疫細胞失去功能。
腫瘤可能分泌激素,讓周圍的殺手 T 細胞無法靠近;或是腫瘤特化的血管,除了向外竊取養分之外,還會誘導殺手 T 細胞凋亡。在腫瘤內部,也存在各種免疫細胞,只是大多數已經「轉性」,不具有攻擊性,有些甚至已「倒戈」,反而當起癌細胞的保鑣。
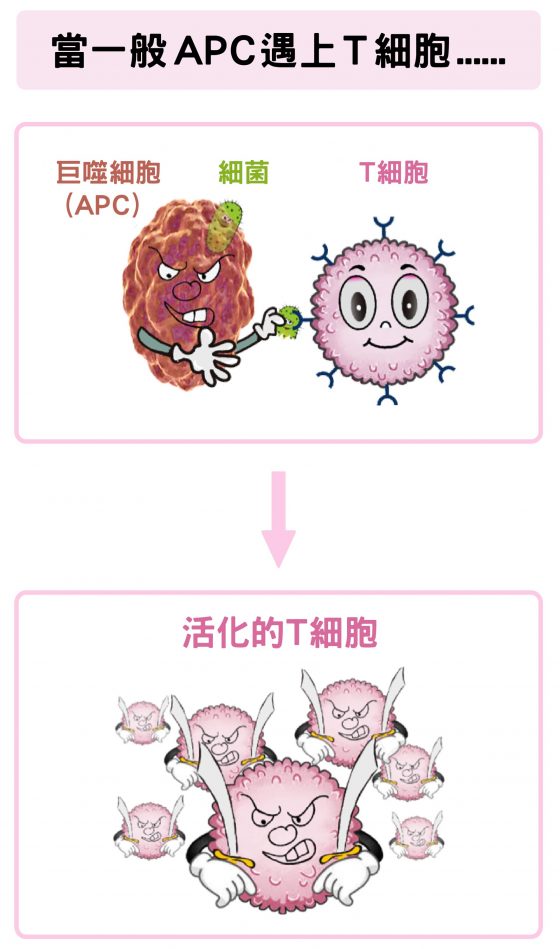
像免疫系統的巨噬細胞 (Macrophage) 原本負責活化殺手 T 細胞。當它吞噬病原體(如細菌或病毒)之後,會變成抗原呈現細胞 (Antigen-presenting cell,簡稱APC),會將病原體的殘骸當作可辨識的抗原 (Antigen),激活特定的殺手 T 細胞。而且下次再遭遇同種病原體,免疫系統就能夠快速反應、有效地處理,這是疫苗保護效果的主要原理。
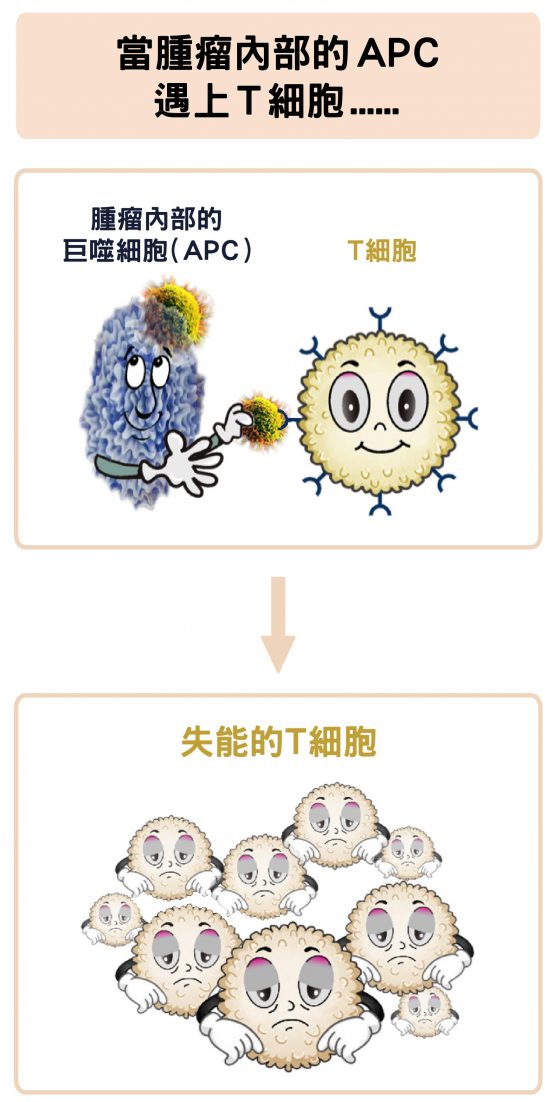
但在腫瘤內部的巨噬細胞,即使吞下癌細胞,不僅沒辦法活化殺手 T 細胞,反而會讓 T 細胞失去功能,甚至還會反過來守衛腫瘤,就像是被癌細胞招降一樣。
免疫療法即是破解癌細胞抑制免疫細胞的諸多「招術」後,想辦法讓免疫細胞恢復,繼續擊殺癌細胞!
免疫檢查點抑制劑:讓腫瘤內的殺手 T 細胞不再失能
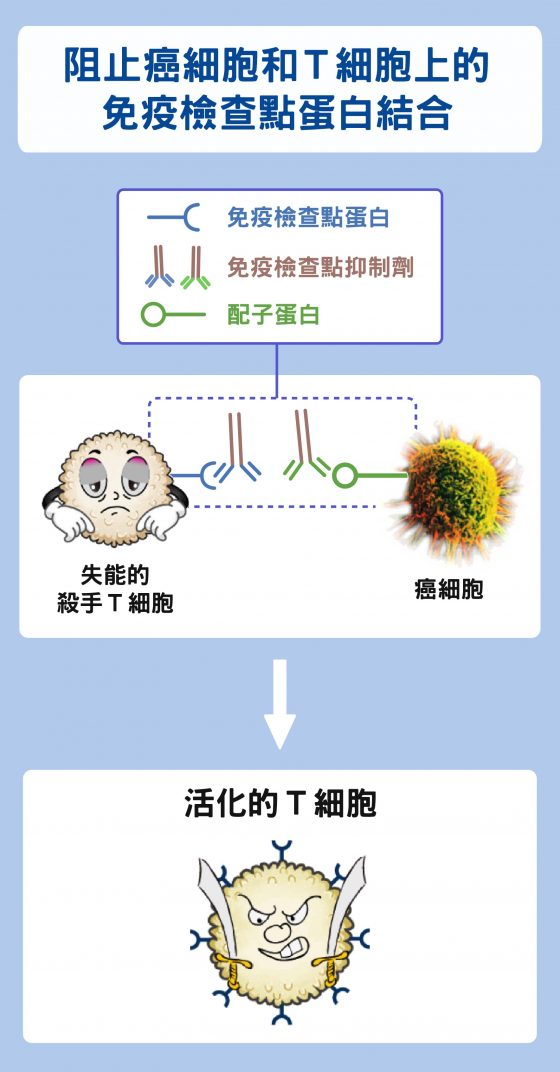
前面提到,腫瘤抑制免疫細胞其中一招,是讓殺手 T 細胞失去活性。說得更清楚一點,癌細胞或被癌細胞馴化的吞噬細胞,用特化的配子 (ligand) 蛋白與殺手 T 細胞表面的「免疫檢查點蛋白」結合,使其失能。
因此,只要投入分別能與之結合的抑制劑,就可以有效阻絕兩者互相接觸,保有殺手 T 細胞的攻擊性,這個方法稱為「免疫檢查點抑制劑」。
看來貌似簡單的概念,實際上卻是癌症醫學的重大突破。2018 年的諾貝爾醫學獎,就是頒給發現殺手 T 細胞抗原 4 (Cytotoxic T-lymphocyte-associated protein 4, CTLA-4) 與計畫性死亡蛋白質-1 (Programmed cell death protein 1, PD-1) 兩種免疫檢查點蛋白的學者。
CTLA-4 被發現、製造出抑制劑後,已於 2011 年獲歐美藥證,能夠有效治療黑色素瘤轉移癌。陶秘華強調,原本罹患這種癌症的病人很少能活過一年,但臨床上長期追蹤使用 CTLA-4 抑制劑的一千八百位病人,發現有百分之二十存活超過十年。
至於 PD-1/PD-L1 抑制劑對何杰金氏淋巴瘤具有百分之八十七的治療有效率,對於 DNA 修復蛋白發生突變、容易產生細胞突變的各種轉移癌患者,也有高達五成的治療效果;但對於肺癌、肝癌則是效果中等,只有五分之一。
陶秘華指出,PD-1/PD-L1 抑制劑治療效果的關鍵,包括腫瘤內殺手 T 細胞的數量不足、腫瘤細胞的突變點位太少、或腫瘤細胞不表現 PD-L1 配子等。目前尚無法確認為什麼有些腫瘤殺手 T 細胞數量多、有些比較少。
「不過,至少在治療前,可取病人上述生物指標量當作評估的參考,」陶秘華建議:「因為藥費可不便宜,如果不適合免疫抑制劑療法,建議採用其他療法,以免徒勞無功。」
免疫細胞治療:先在體外製造大量殺手T細胞,再送進病患體內
另一種免疫療法,並非由病患自己生產殺手 T 細胞,而是將身體原有的分離出來、大量增加後,再注射回病患體內去攻擊腫瘤,稱為「免疫細胞治療」。
目前的主要療法為 CAR-T 細胞。原理是從病人血液中分離出 T 細胞,再用基因工程將其改造,讓 T 細胞上面出現設計好的嵌合抗原受體(Chimeric antigen receptor , 簡稱 CAR),負責辨識癌細胞「表面抗原」的抗體,以及用來活化 T 細胞的訊息傳遞分子,皆能讓 T 細胞更有能力攻擊腫瘤。
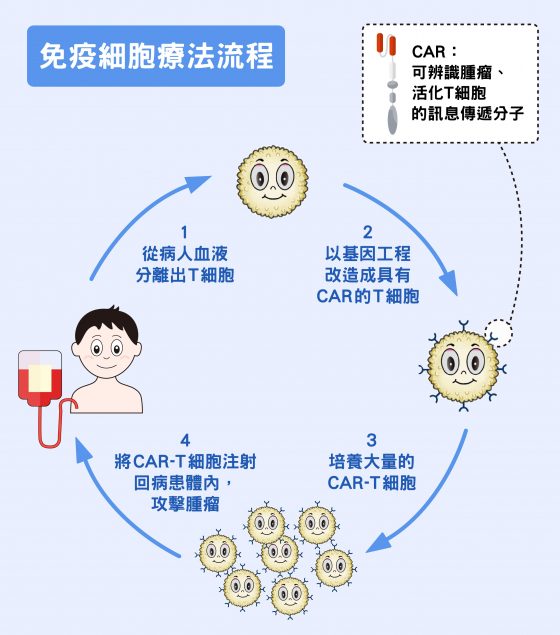
CAR-T 細胞在治療急性 B 淋巴細胞白血病(Acute lymphoblastic leukemia , 簡稱 ALL)時效果非常顯著,對晚期患者有效率達百分之九十以上。可惜的是,用在其他常見癌症,例如肺癌,碰到許多困難。
主要是 CAR 的專一性不夠,因為癌細胞與正常細胞只有些微差異,為數眾多且活力充沛的殺手 T 細胞,常會錯誤辨認、攻擊到正常細胞。臨床試驗上,曾出現正常肺細胞遭受攻擊,導致病人死亡的案例。CAR-T 細胞的「抗藥性、專一性與治療伴隨的副作用,都是未來要克服的難題。」陶秘華補充說。
奈米癌症疫苗:追擊潛藏的癌細胞,降低癌症復發機率
癌症發展到晚期,可能會轉移到身體任何部位,即使當下看似痊癒,復發的案例不在少數。藉由接種奈米癌症疫苗,有機會降低復發與轉移機率,甚至將癌細胞徹底殲滅。
作法是,將癌症病人切除的腫瘤一部分移植到小鼠身上,當作日後實驗樣本;一部份用來萃取 DNA 與 RNA,再經次世代基因定序與生物資訊演算法,找出癌細胞基因突變的片段與抗原性預測;再來用這些資訊合成不同的胜肽片段,製造奈米級粒子,製成疫苗以訓練該病患免疫細胞,追殺、掃清體內可能躲藏的癌細胞。(有關更多奈米疫苗的製造,請見「研之有物」另一篇好文〈奈米級的 Cosplay:假扮病毒的 MERS 奈米疫苗〉)
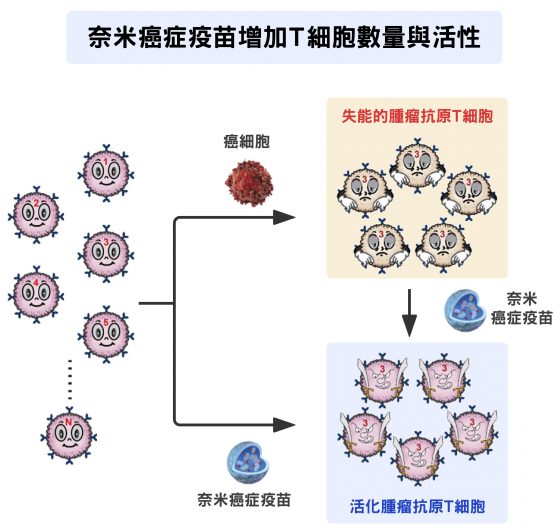
值得注意的是,奈米癌症疫苗跟一般疫苗不一樣,不是預防疾病,而是防止「復發」,所以無法製造大眾通用的疫苗。以 B 型肝炎疫苗為例,每個人接觸的病毒都一樣,所以疫苗成分也一樣;但以癌症來說,每個人癌細胞的基因突變不一樣,奈米癌症疫苗必須等到病患發病後,再為病患量身打造。
前期傳統治療、後期免疫療法
拜免疫治療進步所賜,原本傳統療法很難處理、存活率很差的癌症晚期病患,如今有機會大幅度降低癌症復發、轉移。但由於個人體質差異,不論是哪一種免疫治療,仍無法保證一定有治療效果,還要考慮龐大醫藥費以及可能的副作用。
因此盡早發現、立即處理,才是對抗癌症最好、最有效的方式。
陶秘華指出,免疫療法是提供晚期癌症的新選擇,但晚期補救遠遠不及早期發現、治療有效。因此定期健康檢查、腫瘤偵測依然不可少。「以目前能偵測到的最小腫瘤來說,也已經是數億甚至更多的癌細胞,千萬不可拖延、輕視。」陶秘華提醒。
最後,還要建議民眾,在看完中研院癌症相關研究後,有任何關於個人的問題,不論是診斷或是治療,還是必須向醫院請求協助。「畢竟中研院沒辦法治療癌症,醫院才行。」陶秘華小心提醒。
延伸閱讀:
本文轉載自中央研究院研之有物,原文為癌症晚期可以治癒嗎?!一篇弄懂癌症免疫治療,泛科學為宣傳推廣執行單位