Nature 150 歲生日的汙點
大家都認識的 Nature 期刊,第一期於 1869 年 11 月 4 日出版,因此今年 2019 年 11 月 7 日這一期,就是 Nature 期刊第 150 歲的大日子。何其諷刺,如此值得紀念的這一期中刊出的〈Human origins in a southern African palaeo-wetland and first migrations〉,這篇論文竟然引發罕見的劣評潮。1
閱讀論文以前,我先從新聞稿〈The homeland of modern humans〉讀到這個研究,讀完大感不妙,再讀論文後真的是深受震撼,Nature 竟然讓這種東西刊登?隨後幾天搜尋新聞與社群媒體,有遺傳學、古人類學、考古學等領域的許多專家表達疑慮,或是指責 Nature,具名講話的學者們幾乎一面倒批評。2
志大才疏的「跨領域」團隊
這篇論文的作者宣稱:根據粒線體DNA 和氣候模型,發現人類的原鄉位於南非南部某處。即使不涉及仍然高度爭議的討論方向,這麼直接的論點也很明顯是錯誤的,由一些訪問來看,論文作者們或許是由於所知太少,而過於自信,他們的知識水平無能駕馭這麼複雜的議題。
論文一共有 12 位作者,主導研究的頭牌是 Vanessa Hayes,她是資深的人類遺傳學家,長期研究非洲南部的桑族,之前有研究上過 Nature 卻也起過爭議。3, 4
第一作者 Eva Chan 根據記錄,她的專業是生物資訊,缺乏古人類、考古,以及演化的經驗(看訪問是一竅不通)。另一位作者 Axel Timmermann 專業在於古氣候模型,相對之下比較正常一點。志大才疏的這群人跨領域合作,造就一場研究上的大災難。

20萬年前誕生,停滯7萬年,然後動得很厲害
非洲南部的桑族,是與其他人分家最久的群體之一,研究人類演化的學者絕對不會忽略他們。有很多小群體被歸類為桑族,各有科學界的合作對象,而 Vanessa Hayes 長期與某些地方的桑族人交好,因此能取得他們的樣本。最新研究中,Vanessa Hayes 獲得 198 位桑族人的粒線體DNA。
人的染色體位於細胞核,繼承自父母雙方,承載大部分遺傳訊息;但是粒線體中有自己一套獨立的DNA,是母系遺傳,只由媽媽傳給女兒與兒子。DNA有時候會突變,沒什麼危害的話會保留下來,繼續一代一代傳承。
根據不同的人的粒線體DNA彼此的差異,能判斷突變們產生的先後次序;依此可以定義出不同「單倍群(haplogroup)」和更細的「單倍型(haplotype)」,方便描述彼此的關係。智人粒線體最早分家成兩大群,一群是 L1 到 L6,另一群是 L0, L0 就是這次論文著重的對象。
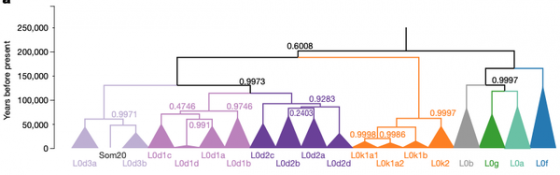
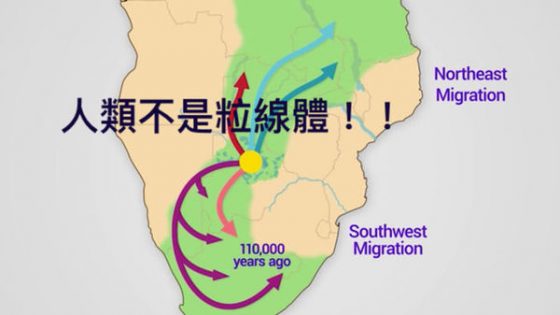
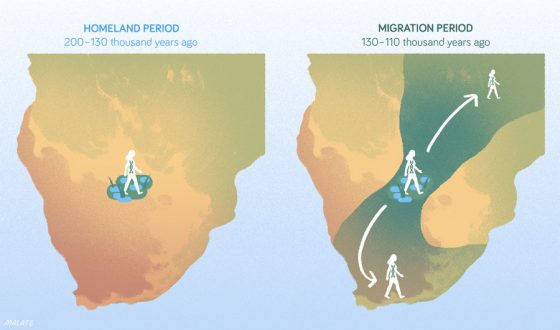
綜合新取得和之前的資料,Vanessa Hayes 與 Eva Chan 組成的遺傳學團隊估計 L0 單倍群大概在 20 萬年前誕生,接下來 7 萬年都缺乏變化,接著距今 13 萬年之後,衍生出 L0d、L0k、L0f 等等後續變異。
她們認為這些型號,現代的地理分佈位置會與古代一樣,所以主張 L0 起源自非洲南部的波札那(Botswana) Makgadikgadi–Okavango 地帶。此地現在氣候乾燥,20 萬年前卻是湖泊與溼地。
再加上古氣候條件模擬,恰好非洲南部距今 13 到 20 萬年前之間,7 萬年來都沒有太大變化,而氣候開始改變的時刻,剛好也是 L0 衍生型號陸續誕生的年代,遺傳、地理、氣候如此完美的對應,怎麼可能是巧合呢?
「太巧合了,你知道,太巧合了(It’s just too coincidental to be, you know, coincidence)」,Eva Chan 受訪時如是說。5
一些遺傳學家該知道的事
莫非人類史上的大秘密就這麼容易被揭露嗎?當然不是,必須無視近幾年許多重大發現,還要不知道好些基本常識,才能像 Eva Chan 如此天真。

以一位人類遺傳學家而言,最基本該有的知識是:粒線體只是一個人一小部分的遺傳訊息,而一個人基因組上不同部分的來歷可以不一樣。粒線體不等於人體。我非常好奇,Vanessa Hayes 和 Eva Chan 難道不知道最早分家的人類 Y染色體,現在位於西非嗎?
至少能夠確定,有些如今智人的粒線體,可以追溯到 20 萬年前。但是也該知道的常識是:人類會移動。缺乏其他佐證之下,L0 現在分佈於某處,不等於 20 萬年前一定也在該處。
還有一條進階一點的知識:粒線體是不會經歷遺傳重組的單一遺傳標記,也容易被遺傳交流後的另一群型號取代。族群中的粒線體假如被取代就是被取代了,事後很可能毫無跡象,若是沒有古代DNA,沒有人知道成千上萬年前發生過什麼事。
目前知道的案例是,西班牙的胡瑟裂谷 43 萬年前的人類,化石形態看起來像是初期尼安德塔人,細胞核基因組 DNA 也接近尼安德塔人,但是粒線體 DNA 卻比較偏向丹尼索瓦人。目前仍不清楚為什麼細胞核與粒線體的遺傳史不一致,但是可以肯定牽涉到混血與取代。6
用單純的粒線體變化,等同於整個人類的演化,風險非常大。有些學者建議,如 Y染色體、粒線體、特定基因變異這類單一遺傳標記,不適合用於追溯經歷時間比較久,牽涉多層次混血的複雜遺傳史,我覺得很值得參考。
只選中意的證據,還搞錯定義!
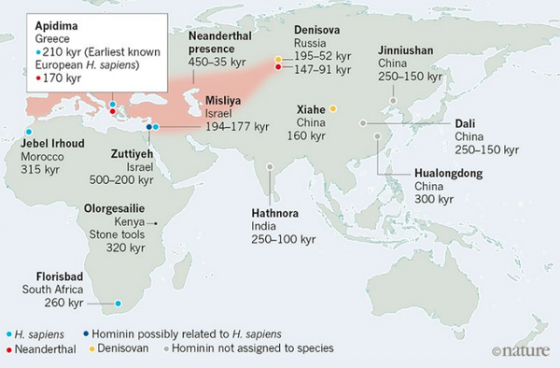
一些專家也指出,近年不少新的各領域發現,都告訴我們智人的演化之路,比之前認為的更早也更廣。例如已知具備智人特徵的化石,最早於 30 多萬年前的北非摩洛哥出土,還有 26 萬年前的南非、21 萬年前的希臘、20 萬年前的東非、18 萬年前的以色列等等,廣義上他們都屬於「解剖學意義上的現代人(anatomically modern human,簡稱 AMH)」,比此論文聲稱,智人開始動的很厲害的 13 萬年前更早。7, 8, 9
神奇的是,這篇論文其實誤用了 AMH 的定義。綜合論文敘述與 Vanessa Hayes 受訪的講法,她認知中的 AMH 就是「Homo sapiens sapiens」,意思是智人中的智人亞種,或者不是尼安德塔人的非洲智人。然而,AMH 其實是以化石型態特徵定義,與粒線體DNA 等遺傳特徵無關,可以兩個人遺傳上很不一樣,卻都是 AMH。
論文的敘述中,似乎直接把 20 萬年前的 AMH 描述為具備 L0 粒線體單倍群,又直接等同於今日智人的祖先。但是這點毫無證據,也或許所謂的 AMH 型態特徵,大部分是在其他智人族群中演化出來,後來再和有 L0 的女生合體,才形成現在的狀況。
遺傳與形態的改變時常沒有一致,另一項遺傳演化學家該有的常識。
看 Vanessa Hayes 講話充滿驚喜。有專家批評 Vanessa Hayes 主導的研究沒有考慮化石和古代DNA,面對質疑時她表示,北非、希臘、以色列那些更早的「智人」並沒有留下後裔,與今日的智人無關,所以無需理會他們(但是即使是女生也不該無視 Y染色體吧?)。可是這也表明,她沒有跟上她長年投入的桑族研究最新進度。10
長時間多地交流?智人起源的新思考
由基因組估計,某些桑族人確實和其他人分家最久,而且至少有 26 萬年,比 Vanessa Hayes 用粒線體計算的 20 萬年更早。事實上,26 到 30 多萬年此一年代,有經過古代DNA 的修正;因為桑族人的祖先,數千年前曾經與其他人混血,使得混血過後的桑族人,配備更多與其他族群相同的遺傳變異,而拉低遺傳差異,使得估計的分家年代縮短。11, 12
更不要提,最近分析非洲族群的基因組發現,有好幾個族群彼此分家數萬或數十萬年,和這篇論文主張智人起源於南非再跑到各地,狀況非常非常不一樣。
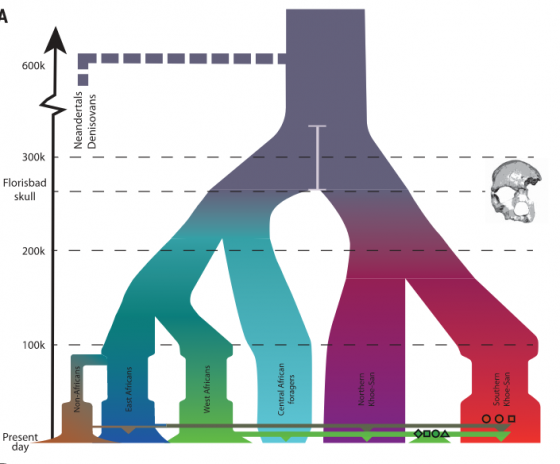
有關智人起源,一度相當流行的論點是,智人最初誕生於 20 萬年前的東非某處,7 萬年前經歷一次瓶頸,只剩下少數人口,後來全人類都能追溯至此。不過最近愈來愈多人認識到,此一推論是由於當年資訊有限,加上忽視非洲內部的多樣性所致,智人演化的狀況實際上更加複雜許多。
根據最近的遺傳、化石、考古等跨領域證據,一批學者在 2018 年提出「非洲多地起源論(African multiregionalism)」,主張智人並非源自特定地區的單一族群,而是在 20 到 50 萬年前,於非洲各地(有時候也包括中東),長期交流所形成。13
非洲多地起源論仍存在不少漏洞,必需持續修正,但是根本上反對智人起源自某一時刻的單一地點,也難怪跳出來批評「南非某地 20 萬年前是智人原鄉」的學者中,如 Eleanor Scerri 和 Huw Groucutt 等人,就是非洲多地起源論的支持者。
參與這篇論文問世的人,都該受到譴責
不過對於這篇論文,學術界並非一面倒批評,也有人認為有值得稱道之處,其中一位是 1980 年代提出「粒線體夏娃」,證實智人源自非洲的 Rebecca Cann;然而,她剛好也是這篇論文的審查者。14, 15
透過經營交情,這項研究取得一批難得的人類材料,但是對於人類起源和演化的了解,說實話並沒有增加多少,更何況一番狀況外的推論有夠驚世駭俗。即使 Rebecca Cann 認為這篇論文可以促進討論與後續研究,也不是放行的理由。Nature 與這篇論文的審查者,都應該受到嚴厲的譴責。16, 17
我覺得,讓這種品質的論文過關,Nature 期刊的編輯與找來的審查者都該負起責任,他們聯手造就了這篇論點很糟糕,也許還將帶來某些負面影響的論文。
延伸閱讀
- 南非人類原鄉?落伍遺傳學,粒線體不能這樣用
- 丹尼索瓦人(上):尼安德塔人的神秘近親
- 尼安德塔人的粒線體變化,古DNA 揭露未知混血秘辛
- 改寫智人物種起源:時間從30萬年前起、地點涵蓋整個非洲
- 非洲之外的最早智人,以色列18萬年前
- 非洲之外的最早智人,希臘超過21萬年前
- 人類對自身起源的百年追尋
參考文獻
- Chan, E. K., Timmermann, A., Baldi, B. F., Moore, A. E., Lyons, R. J., Lee, S. S., … & Bornman, M. R. (2019). Human origins in a southern African palaeo-wetland and first migrations. Nature, 1-5.
- The homeland of modern humans
- Has Humanity’s Homeland Been Found?
- Schuster, S. C., Miller, W., Ratan, A., Tomsho, L. P., Giardine, B., Kasson, L. R., … & Alkan, C. (2010). Complete Khoisan and Bantu genomes from southern Africa. Nature, 463(7283), 943.
- Experts Skeptical of New Study Pinpointing the Birthplace of Humanity
- Meyer, M., Arsuaga, J. L., de Filippo, C., Nagel, S., Aximu-Petri, A., Nickel, B., … & Viola, B. (2016). Nuclear DNA sequences from the Middle Pleistocene Sima de los Huesos hominins. Nature, 531(7595), 504.
- Hublin, J. J., Ben-Ncer, A., Bailey, S. E., Freidline, S. E., Neubauer, S., Skinner, M. M., … & Gunz, P. (2017). New fossils from Jebel Irhoud (Morocco) and the Pan-African origin of Homo sapiens. Nature.
- Hershkovitz, I., Weber, G. W., Quam, R., Duval, M., Grün, R., Kinsley, L., … & Arsuaga, J. L. (2018). The earliest modern humans outside Africa. Science, 359(6374), 456-459.
- Harvati, K., Röding, C., Bosman, A. M., Karakostis, F. A., Grün, R., Stringer, C., … & Gorgoulis, V. G. (2019). Apidima Cave fossils provide earliest evidence of Homo sapiens in Eurasia. Nature, 571(7766), 500-504.
- Experts question study claiming to pinpoint birthplace of all humans
- Skoglund, P., Thompson, J. C., Prendergast, M. E., Mittnik, A., Sirak, K., Hajdinjak, M., … & Heinze, A. (2017). Reconstructing prehistoric African population structure. Cell, 171(1), 59-71.
- Schlebusch, C. M., Malmström, H., Günther, T., Sjödin, P., Coutinho, A., Edlund, H., … & Lombard, M. (2017). Southern African ancient genomes estimate modern human divergence to 350,000 to 260,000 years ago. Science, 358(6363), 652-655.
- Scerri, E. M., Thomas, M. G., Manica, A., Gunz, P., Stock, J. T., Stringer, C., … & d’Errico, F. (2018). Did our species evolve in subdivided populations across Africa, and why does it matter?. Trends in ecology & evolution.
- Controversial new study pinpoints where all modern humans arose
- Humans’ maternal ancestors may have arisen 200,000 years ago in southern Africa
- No, a genetic study didn’t pinpoint the ancestral homeland of all humans
- The diversity of human origins in content and practice: A response to Chan et al (2019)
本文亦刊載於作者部落格《盲眼的尼安德塔石匠》暨其 facebook 同名專頁。