從安潔莉娜裘莉 (Angelina Jolie) 進行預防性乳房切除術談起
文 / 曾文宏(大林慈濟醫院家庭醫學科,住院醫師)
前言
安女士,37歲
有過二段婚姻,目前有一個穩定交往的男友
育有三個親生兒女,也領養三個兒女
母親56歲時,於2007年因卵巢癌過世
自費測BRCA 1是陽性
別的醫師說我有87%的會得到乳癌,50%會得到卵巢癌
我該做預防性的乳房切除和卵巢切除嗎?
我們假設這是裘莉姐在做最後決定前所有的全部資訊,這情況也可能發生在妳或你姊妹妻女媽媽阿姨身上,想必你應該對其中的一些名詞感到困惑,也覺得裘莉姐做這個決定雖然很有勇氣,但真的值得嗎?
本文即是以科學的角度匯集最新的資料來回答這些問題。
問題目錄:
- 乳癌和卵巢癌發生率和死亡率有多高?
- BRCA是什麼?
- 有BRCA基因異常的人,得乳癌或卵巢癌的機會較大嗎?
- 我有需要做BRCA檢測嗎?
- 如何知道自己罹患乳癌的風險?
- 什麼時候該上醫院尋求乳癌或卵巢癌遺傳諮詢?
- 我BRCA為陽性,怎麼辦?
- 我的BRCA1或BRCA2異常,我不想每年都擔心乳癌或卵巢癌發生,有沒有減少風險或一勞永逸的方法?
- 誰可考慮預防性乳房切除?
- 預防性乳房切除真的有預防效果嗎?
- 預防性乳房切除缺點是什麼?
- 治療乳癌的方法日益進步,得乳癌一定會很快步入死亡嗎?
- 預防性雙側卵巢摘除真的有預防效果嗎?
- 預防乳癌不開刀的方法
Q1: 乳癌和卵巢癌發生率和死亡率有多高?
依人種不同有很大差異。
乳癌:
台灣發生率約63.2,死亡率11.6 (每十萬人口);
美國白人發生率約125,死亡率24(每十萬人口)。
卵巢癌:
台灣發生率約5.4,死亡率1.72(每十萬人口);
美國白人發生率13.3,死亡率8.9(每十萬人口)。
點評
- 乳癌發生率高卵巢癌十倍,但得卵巢癌死亡率較高
- 台灣人得到或死於乳癌、卵巢癌的機會,比美國白人低一半以上
詳解
一、乳癌
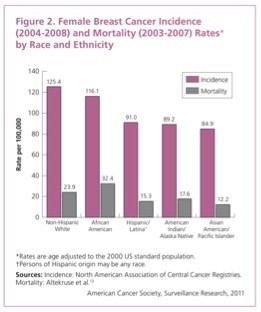
這是美國乳癌發生率(incidence, 紅色)和死亡率(mortality, 灰黑色)的統計製表,最左邊是非西班牙裔白人,最右邊是亞洲裔。白人乳癌的發生率和死亡率都比亞裔高不少。
附帶一提,根據Dynamed資料庫,美國女性終其一生得到乳癌的機會是12.15%,亦即每八位美國女性就有一位會得到乳癌。
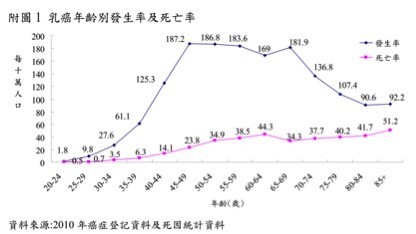
這是台灣國民健康局(簡稱國健局)的資料。
資料顯示台灣女性標準化乳癌發生率為63.2;標準化死亡率: 11.6 (每十萬人口)。值得一提的是,和美國的數據比較,台灣乳癌發生率和死亡率都比美國亞裔還低。
我們可以看出45歲至69歲是乳癌發生的高峰,因此國健局在這段年齡層的婦女提供免費的每二年一次的乳房攝影檢查。
二、卵巢癌
在美國,根據Dynamed資料庫。整體平均:發生率12.9,死亡率8.6 (每十萬人口);若只算亞裔:發生率9.2,死亡率4.9 (每十萬人口);若單算白人:發生率13.3,死亡率8.9 (每十萬人口)。
在台灣,根據1998年資料,年齡標準化發生率 5.44/100,000,年齡標準化死亡率 1.72/100,000。
同樣台灣卵巢癌的發生率和死亡率都比美國亞裔還低。另外,雖然卵巢癌發生率少於乳癌十分之一,但得到卵巢癌死亡率較高。
同場加映:2011國內十大癌症死因
| 全國 | 男性 | 女性 | ||||
| 排名 | 癌症死因 | 死亡人數 | 癌症死因 | 死亡人數 | 癌症死因 | 死亡人數 |
| 1 | 肺癌 | 8541 | 肺癌 | 5740 | 肺癌 | 2801 |
| 2 | 肝癌 | 8022 | 肝癌 | 5633 | 肝癌 | 2389 |
| 3 | 大腸癌 | 4921 | 大腸癌 | 2875 | 大腸癌 | 2046 |
| 4 | 女性乳房癌 | 1852 | 口腔癌 | 2308 | 女性乳房癌 | 1852 |
| 5 | 口腔癌 | 2463 | 胃癌 | 1482 | 胃癌 | 806 |
| 6 | 胃癌 | 2288 | 食道癌 | 1415 | 胰臟癌 | 700 |
| 7 | 攝護腺癌 | 1096 | 攝護腺癌 | 1096 | 子宮頸癌 | 681 |
| 8 | 胰臟癌 | 1607 | 胰臟癌 | 907 | 卵巢癌 | 445 |
| 9 | 食道癌 | 1507 | 淋巴瘤癌 | 613 | 淋巴瘤癌 | 358 |
| 10 | 子宮頸癌 | 681 | 鼻咽癌 | 570 | 白血病 | 338 |
| 總計 | 32978 | 22639 | 12416 | |||
Q2: BRCA是什麼?
BRCA1和BRCA2是1990年代發現和乳癌、卵巢癌相關的癌症抑制基因,若異常可能會引發癌症。一般人基因異常機率小於1%,在乳癌或卵巢癌的族群也僅約10%此基因異常。亞裔族群帶有這基因的機會更低。BRCA1或BRCA2異常的人的確有較高可能得到乳癌(57%~85%)或卵巢癌(18%~40%),但數據僅供參考且可能過於誇大。
點評
台灣人和此基因的相關性並不高,所以毋須過度緊張、人人皆跑去篩檢。但若有高危險家族史,此基因檢測確實可提供罹患乳癌或卵巢癌的可能性參考;若已罹患乳癌卻治療效果不彰,也可能是此基因作怪。
詳解
歷史:
1990年,第一個發現和乳癌相關的基因,位於第17對染色體,顯性遺傳,稱作乳癌一號(breast cancer 1,簡稱BRCA1)。
1994年,第二個發現的基因,位於第13對染色體,顯性遺傳,稱作乳癌二號(breast cancer 2,簡稱BRCA2)。
簡言之,這基因是癌症抑制基因,專控制細胞生與死,若失調就會引發癌症。
註:乳癌一號和二號翻譯是筆者自己翻的,我也覺得很俗…
(Reference: Standford Cancer Institute, http://cancer.stanford.edu/information/geneticsAndCancer/types/herbocs.html)
盛行率:
- 在美國一般人裡,BRCA1或BRCA2異常的人約0.2到0.33%。(Reference: Ann Intern Med 2005 Sep 6;143(5):362)
- 其中美國白人有乳癌的女性,約5%到10%有BRCA1或BRCA2異常;有卵巢癌的女性約10%到15%有基因異常。(Reference: Hum Genet 2008 Aug;124(1):31)
- 若是從種族分析,已得到乳癌的病人中,美國德裔猶太人帶有BRCA1的機會最高 (8.3%),非西班牙裔的白人第二 (3.5%),亞裔最低 (0.5%)。(Reference: JAMA 2007 Dec 26;298(24):2869)
國健局的遺傳疾病諮詢窗口網站也有相關描述,節錄如下:
- 大部分的乳癌和卵巢癌是偶發的,不清楚其致病原因,大部分罹患乳癌或卵巢癌的婦女也不屬於遺傳性乳癌與卵巢癌。
- 目前估計在一般族群中找到BRCA1與BRCA2基因突變的機會是小於1%,而罹患乳癌的婦女約有10%至15%具有此基因突變。
- 若家族內有四人或以上在60歲以前罹患乳癌,則有八成的機會該家族具有此基因突變,相對地,若家族內只有一人在五十歲前診斷出乳癌,則找到基因突變的機會約只有10%。
- 根據台大醫院基因醫學部的統計,具有乳癌家族史的台灣患者,亦約有10%可以找到基因突變。
(Reference: http://gene.bhp.doh.gov.tw/index.php?mo=DiseasePaper&action=paper1_show&cate=Set1&csn=66&sn=434)
根據大林慈濟醫院血液腫瘤科蘇裕傑主任表示:國健局提到「目前估計在一般族群中找到BRCA1與BRCA2基因突變的機會是小於1%,而罹患乳癌的婦女約有10%至15%具有此基因突變」-是國外的說法,在台灣則約4~5%乳癌病患帶有BRCA1基因。
乳癌或卵巢癌病人有BRCA基因異常的機會比一般人高,那可以反推有BRCA基因異常的人,得乳癌或卵巢癌的機會較大嗎?
- 到70歲前,BRCA1基因突變有57%的機會得到乳癌,40%的機會得到卵巢癌;BRCA2基因突變有49%的機會得到乳癌,18%的機會得到卵巢癌。(Reference: J Clin Oncol 2007 Apr 10;25(11):1329)
- 另外一篇研究指出,帶有BRCA1或BRCA2基因突變,終身得到乳癌的機會達到85%,得到卵巢癌的機會達到26%。(Reference: Ann Intern Med 2005 Sep 6;143(5):362)
- 但也有研究指出,這些數據可能過於誇大BRCA基因異常得到乳癌或卵巢癌的機會。(Reference: J Natl Cancer Inst 2002 Aug 21;94(16):1221)
以我們台灣人或亞裔人種來說,和BRCA1或BRCA2的關聯性並不強,因此一般人毋須過度擔心。
但乳癌患者,若有BRCA1或BRCA2基因異常,可能對荷爾蒙反應差,只能用化療;HER2/neu也是陰性的,標靶藥物也無效;細胞分化往往也比較惡性。因此這對乳癌患者來說是有預後指標參考價值的。(Reference: http://www.breastcancer.org/symptoms/testing/genetic/pos_results)
Q3: 我有需要做BRCA檢測嗎?
一般人不建議做BRCA檢測 (除非錢太多),有高危險家族史才需要。高危險家族史的定義,美國較重視親等,歐洲較重視罹患癌症的年紀。只要自己的家族史有二位以上卵巢癌或乳癌,若任一親戚有雙側乳癌、男性乳癌、年輕乳癌,都應保持警覺、尋求醫師諮詢。
詳解
美國疾病預防署的建議(United States Preventive Services Task Force [USPSTF] recommendations):
- 若是德裔猶太人:只要有一位第一親等的親戚有乳癌或卵巢癌;或二位第二親等的親戚有乳癌或卵巢癌,就建議做BRCA基因檢查。
- 若是其他族群符合以下條件,也建議做BRCA檢查:
- 第一親等親戚,有2位以上罹患乳癌
- 第一加第二親等親戚,有3位以上罹患乳癌
- 第一或第二親等親戚,任1位有乳癌合併卵巢癌
- 任1位第一親等親戚,有雙側乳癌
- 第一加第二親等親戚,有2位以上罹患卵巢癌
- 有男性親戚罹患乳癌
歐洲癌症協會建議(European Society for Medical Oncology [ESMO] recommendations):
以下族群建議做BRCA檢查。
- 3位親戚以上有乳癌或卵巢癌,其中1位小於50歲
- 2位親戚小於40歲即得到乳癌
- 有1位男性親戚罹患乳癌,外加有女性親戚得到乳癌或卵巢癌
- 德裔猶太人,小於60歲得到乳癌
- 年輕且雙側乳癌患者
- 同時罹患乳癌和卵巢癌
BRCA檢測花費
- 美國:根據裘莉姐在美國的投書,約3000美元 (約九萬新台幣)
- 台灣:根據蘇怡寧醫師的說法,約三萬新台幣
(Reference: ~ 聯合報 台灣乳癌患者 僅5%與基因突變有關)
根據大林慈濟醫院血液腫瘤科蘇裕傑主任補充:目前BRCA1基因檢查,應該要考慮到親友兒女知道你有這個基因後,他們的心理狀況。以安小姐而言,她的女兒也許因為這樣從小就有因為基因不正常而受到歧視的風險,這些都是要驗BRCA1的無症狀人士應該要思考的。所以除了上述的guideline之外,要驗之前,建議還是要做遺傳專家或是醫學倫理咨詢。(不過,台灣目前好像沒有此類專門醫師)
Q4: 如何知道自己罹患乳癌的風險?
可以對一下自己有哪些危險因子-
A. 高危險群(致癌相對機率大於4倍):
- 一側乳房得過乳癌
- 特殊家族史(停經前得過兩側乳癌)
- 乳房切片有不正常細胞增生現象
B. 次高危險群(致癌相對機率大於2~4倍):
- 母親或姊妹得過乳癌
- 卵巢及大腸癌患者
C. 略高危險群(致癌相對機率大於1.1~1.9倍):
- 第一胎生育在三十歲之後
- 未曾生育者
- 停經後肥胖
- 近親有二位以上罹患乳癌,感覺像顯性遺傳
- 小於45歲就罹患乳癌
- 家族史有人有得到卵巢癌(Reference: Dynamed資料庫)
考科藍研究顯示,癌症基因諮詢,可顯著地減少有乳癌家族史的病人,對罹患癌症的焦慮和壓力。(Reerence: Cochrane Database Syst Rev 2012 Feb 15;(2):CD003721)
Q5: 我BRCA為陽性,怎麼辦?
- 每個月自我檢查乳房。
- 每6個月給醫師檢查乳房。
- 每年做乳房攝影和乳房核磁共振。
- 但國健局僅給付45至69歲女性每二年一次的乳房攝影檢查;健保局對於預防性的篩檢是不給付的。
詳解:
歐洲癌症協會建議(European Society for Medical Oncology [ESMO] recommendations):
從25歲開始-
- 每個月自我檢查乳房
- 每6個月給醫師檢查乳房
- 每年做乳房攝影和乳房核磁共振
美國癌症協會(American Cancer Society [ACS])建議:
本身有BRCA基因異常、或第一親等親戚有BRCA異常,30歲開始,每年做乳房攝影和乳房核磁共振。(Reference: CA Cancer J Clin 2007 Mar-Apr;57(2):75-89 full-text)
台灣國健局建議:
對女性家庭成員而言—
- 從十八歲起,每月應進行自我乳房檢查。
- 自二十五歲起,每兩年由醫師進行乳房檢查。
- 美國癌症學會建議每年具有BRCA1 或BRCA2基因突變者進行乳房X光攝影以及乳房核磁共振。
-乳房超音波和乳房攝影適合年輕女性。
-有些醫師建議乳房攝影搭配核磁共振。 - 自二十五歲起,每年或每兩年進行骨盆檢查。
- 自二十五歲起,每年或每兩年進行陰道超音波檢查。
- 自二十五歲起,每年抽血檢驗腫瘤指數CA-125。
對男性家族成員而言—
- 自三十歲起,每月進行自我乳房檢查。
- 自三十歲起,每年由醫師進行乳房檢查。
- 自四十歲起,每年進行前列腺癌篩檢。
(Reference: http://gene.bhp.doh.gov.tw/index.php?mo=DiseasePaper&action=paper1_show&cate=Set1&csn=66&sn=434)
乳房檢查怎麼做?
中華民國乳癌病友協會的真人自我檢查示範講解得非常詳細且用心!
Q6: 我的BRCA1或BRCA2異常,我不想每年都擔心乳癌或卵巢癌發生,有沒有減少風險或一勞永逸的方法?
對BRCA1或BRCA2基因異常的人來說,預防性雙側乳房切除和預防性雙側卵巢摘除確實可以減少乳癌或卵巢癌的發生率。優缺點孰多孰少恐怕要看個人權衡。在台灣,預防性雙側卵巢摘除可能比較容易被接受。
詳解
一、預防性乳房切除-
- 一邊乳房已有乳癌
- 有高危險乳癌家族史
- BRCA1或BRCA2異常
- 乳房硬化或是遍布鈣化點
- 30歲前即接受胸部的放射治療
(Reference: http://www.cancer.gov/cancertopics/factsheet/Therapy/preventive-mastectomy)
考科藍的系統性回顧指出,預防性雙側乳房切除確實顯著降低了有BRCA1或BRCA2基因異常的人,罹患乳癌的機率。並且顯著降低了這些人對罹患癌症的焦慮和壓力。(Reference: Cochrane Database Syst Rev 2010 Nov 10;(11):CD002748)
一篇前瞻性世代研究,追蹤了1619位有BRCA1或BRCA2異常的歐洲或北美女性,其中約15%進行了預防性雙側乳房切除術,追蹤3年後沒有人得到乳癌,但其他人有7%得到乳癌。(Reference: JAMA 2010 Sep 1;304(9):967)
- 切了就再也回不來了..
- 對女性自我身體印象的衝擊
- 失去正常乳房的功能 (如哺乳)
- 乳房會失去感覺,進而影響到性生活
- 手術可能有併發症,流血或感染
- 儘管有以上種種犧牲,卻無法保證自己從此不得乳癌
註:如果對此手術無法想像,可以看一位23歲時,接受預防性雙側乳房切,把整個過程公開的部落格 (Reference: http://www.cancer.gov/cancertopics/factsheet/Therapy/preventive-mastectomy; http://www.breastcancer.org/treatment/surgery/prophylactic_mast)
附上乳癌五年存活率
| 階段 | 5年內的存活率 |
| 0 | 93% |
| 1 | 88% |
| IIA | 81% |
| IIB | 74% |
| IIIA | 67% |
| IIIB | 41% |
| IIIC | 49% |
| IV | 15% |
(Reference: http://www.cancer.org/cancer/breastcancer/overviewguide/breast-cancer-overview-survival-rates)
二、預防性雙側卵巢摘除-
一篇收錄2482位歐洲或北美,有BRCA1或BRCA2異常的女性,進行的前瞻性世代研究顯示:40%選擇預防性雙側卵巢摘除,整體死亡率、死於卵巢癌或死於乳癌的機會都顯著降低。對於只有BRCA1異常且沒得乳癌的女性而言,可減少乳癌或卵巢癌的發生率,但卻不會減少死於這些癌症的機會。(Reference: JAMA 2010 Sep 1;304(9):967)
歐美的建議:
這是35歲到50歲女性,帶有BRCA1或BRCA2異常的癌症高危險族群,最具投資報酬率的預防策略。(Reference: Ann Intern Med 2006 Mar 21;144(6):397)
歐洲癌症協會(ESMO)則建議在35歲以後、已確認小孩養育決定後再施行。術後可給予短暫的荷爾蒙替代療法,此療法不會削減乳癌預防的效益。
三、不開刀的方法-
- 賀爾蒙療法 (Tajmoxifen):對帶有BRCA陽性的一般人預防乳癌的效果仍不明確;但若已有一邊的乳癌,預防另一邊乳癌的發生是有效果的。(Reference: Dynamed)
- 生活方式調整:
- 多運動
- 避免太晚生育
- 少攝取高脂肪食物
- 心情放輕鬆,減低工作壓力
- 定期乳房檢查習慣
(Reference: 乳癌防治基金會網站)
總結
- 乳癌發生率高卵巢癌十倍,但得卵巢癌死亡率較高
- 台灣人得到或死於乳癌、卵巢癌的機會,比美國白人低一半以上
- 台灣人和BRCA基因的相關性並不高,所以毋須過度緊張、人人皆跑去篩檢。但若有高危險家族史,此基因檢測確實可提供罹患乳癌或卵巢癌的可能性參考;若已罹患乳癌卻治療效果不彰,也可能是此基因作怪。
- 但若自己的家族史有二位以上卵巢癌或乳癌,或任一親戚有雙側乳癌、男性乳癌、年輕乳癌,都應保持警覺、尋求醫師諮詢。
- 若檢測BRCA陽性,建議接受密集的追蹤
- 對BRCA1或BRCA2基因異常的人來說,預防性雙側乳房切除和預防性雙側卵巢摘除確實可以減少乳癌或卵巢癌的發生率。優缺點孰多孰少恐怕要看個人權衡。在台灣,預防性雙側卵巢摘除可能比較容易被接受。
特別收錄-國內新聞投書摘要
- 國外統計顯示,即便有BRCA基因突變且適合做預防性乳房切除的婦女,也只有20至25%接受預防性乳房切除。安潔莉娜裘莉做什麼選擇,雖然是熱門話題,但不是重點。重點是在此過程。安潔莉娜裘莉利用醫學新技術得知其罹病風險,在充分諮詢後,自主性地決定處理方式。這是良好的醫病關係,值得我們學習。
-聯合報╱曾嶔元/國泰醫院病檢部主任
- 預防性切除房,可立即進行重建,不像罹癌婦女需等化療等治療結束三個月後才能進行。鄭明輝說,現在利用果凍矽膠重現雙峰,國內單側約10萬元左右,預防性切除乳房和重建,都必須自費。
- 禾馨婦產科執行長蘇怡寧也說,國內乳癌患者約只有5%跟基因突變有關,因此不建議婦女做基因檢測….由於國內婦女罹患乳癌的年齡約比國外年輕10歲,林口長庚副院長鄭明輝建議,與其做基因檢測不如及早進行乳房超音波、乳房攝影篩檢。目前衛生署給付45至69歲婦女、40至44歲二等親曾罹患乳癌婦女,每兩年一次免費乳房X光攝影。他建議一般婦女可於40歲開始篩檢、有家族史民眾則提前於30歲開始,每年一次檢查。
~聯合報 〈台灣乳癌患者 僅5%與基因突變有關〉
- 家族曾有乳癌、卵巢癌病人,其他成員有一半機會會帶有此突變基因。蘇怡寧曾發現有一家四姊妹、另一家三代六口,都帶有BRCA1的基因變異,且其中一人是男性。
- 這一家三代成員中,一開始是媽媽得到乳癌,二女及三女相繼罹患乳癌,四女、么弟及大姊女兒,全都帶有致癌基因,四女選擇預防性卵巢切除,么弟雖是男性,醫師認為他是乳癌及大腸癌高危險族群,建議他每半年追蹤一次。
- 中山醫學大學附設醫院副院長曾志仁表示,相較預防性乳房切除,國人對預防性卵巢切除的接受度較高,主要是切除乳房會影響外觀,但切除卵巢則無此顧慮,因此若檢驗有基因變異、生過小孩且接近更年期者,可考慮切除卵巢。
~聯合報 〈有癌症基因 在台灣切卵巢比切乳多〉