- 作者/照護線上編輯部
- 本文轉載自 Care Online 照護線上《HER2 陽性乳癌惡性度高、容易復發!新一代口服小分子標靶藥物強化輔助治療,顯著降低復發風險,專科醫師圖文解說》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接

一位 60 多歲的 HER2 陽性乳癌患者,已接受過手術並完成術後輔助治療。經過幾年後,患者覺得有肢體無力的狀況,於是回診檢查。義大癌治療醫院院長洪朝明教授表示,進一步檢查發現,患者腦部出現轉移的腫瘤。
HER2 陽性乳癌容易復發轉移,而腦部轉移對患者的影響很大,常會嚴重影響生活品質,預後會比骨頭轉移、內臟轉移更差。洪朝明教授說,為了降低復發風險,針對 HER2 陽性乳癌的治療越來越積極,除了術後輔助治療外,高風險患者還可考慮使用新一代口服小分子標靶藥物進行強化輔助治療,幫助降低復發的機會。
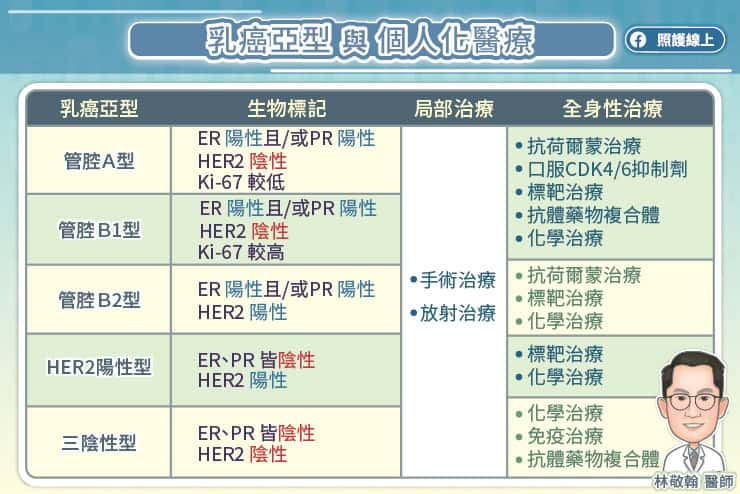
「發現乳癌後,必須了解癌細胞的特性,包括雌激素受體(ER)、黃體激素受體(PR)、第二型人類表皮生長因子受體(HER2)、癌症生長指數(Ki-67)等。」洪朝明教授指出,根據乳癌的特性,可以將乳癌區分成幾個亞型,例如荷爾蒙受體陽性型、HER2 陽性型、三陰性型等。
在台灣,HER2 陽性乳癌約占所有乳癌的 20%。洪朝明教授說,癌細胞的 HER2 基因過度表現,導致癌細胞快速分裂,屬於惡性度較高的乳癌。HER2 陽性乳癌的進展速度較快,復發風險較高,容易轉移到淋巴、腦部、骨骼等處,而且較常出現抗藥性,預後較差。
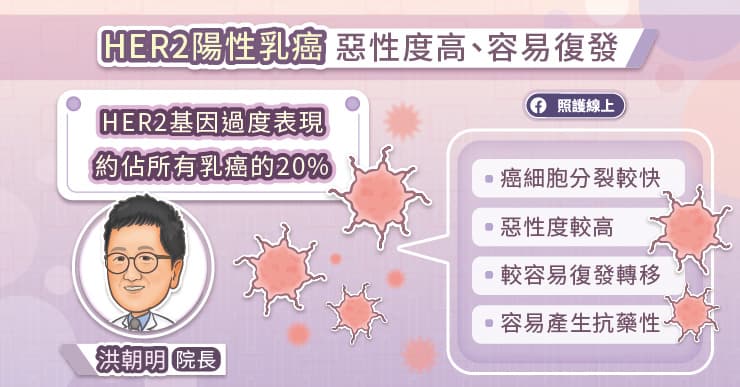
洪朝明教授說,根據統計,HER2 陽性乳癌患者接受治療後,在 8 年內復發的機會仍達 10% 至 20%,所以針對 HER2 陽性乳癌的治療會越來越積極,希望盡量降低復發風險。
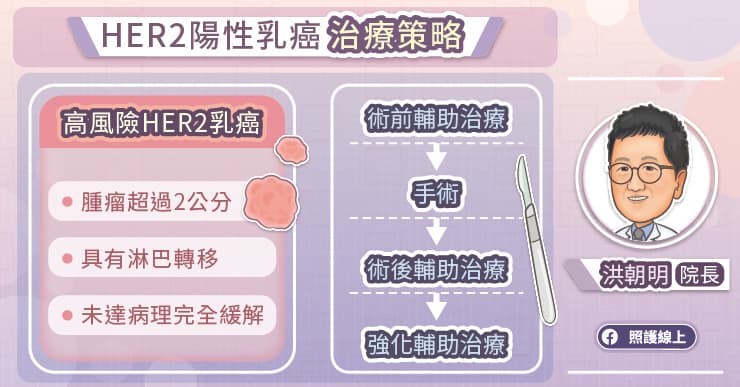
「一般而言,我們會建議 HER2 陽性乳癌患者,在術前接受輔助治療,做完一個完整的療程後再考慮開刀。」洪朝明教授說,手術治療後,接續進行術後輔助治療,目前可能採用標靶治療或雙標靶治療。
如果腫瘤大於 2 公分、有淋巴結轉移、沒有達到病理完全緩解,就屬於高復發風險之 HER2 陽性乳癌。洪朝明教授解釋,接受術前輔助治療後,腫瘤可能會縮小,甚至完全消失。如果在檢體中完全找不到癌細胞,稱為「病理完全緩解」,術後復發風險較低;如果在檢體中依然存在癌細胞,稱做「病理未完全緩解」,術後復發風險較高,容易轉移到肝臟、肺臟、腦部、骨頭等遠端器官。
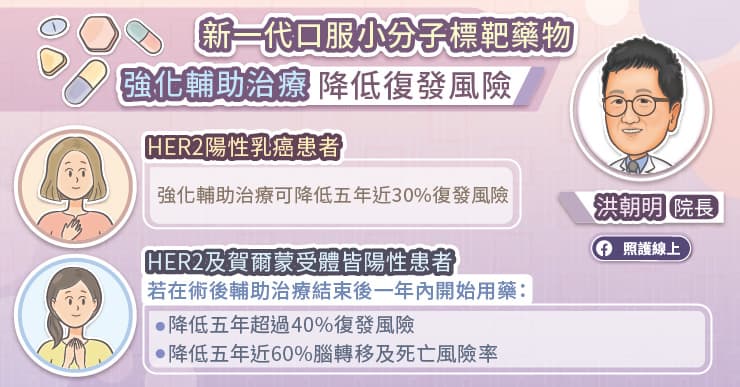
針對高復發風險之 HER2 陽性乳癌患者,在完成一年術後輔助治療後,現在還可以考慮接受強化輔助治療。洪朝明教授說,強化輔助治療是使用新一代口服小分子標靶藥物,小分子標靶藥物能透過不同的機轉抑制癌細胞,根據研究,使用小分子標靶藥物進行強化輔助治療,可降低 HER2 陽性乳癌五年近 30% 復發風險。
若 HER2 陽性與賀爾蒙受體同為陽性於術後輔助治療結束後一年內開始強化輔助治療,可降低五年超過 40% 復發風險。另外,由於小分子標靶藥物具有能夠穿過血腦屏障的特性,有助於預防及治療腦轉移,可降低五年近 60% 腦轉移及死亡風險。若是未達完全病理緩解者的高風險患者效益更顯著,可降低八年 53% 死亡風險。
乳癌的治療持續進步,運用不同的藥物從術前輔助治療、術後輔助治療、到強化輔助治療,能夠幫助患者提升治療成效、降低復發風險。洪朝明院長提醒,請與醫師密切配合,一起努力,對抗乳癌!
筆記重點整理
- HER2 陽性乳癌屬於惡性度較高的乳癌,進展速度較快,復發風險較高,容易轉移到淋巴、腦部、骨骼等處,而且較常出現抗藥性,預後較差。
- 一般會建議 HER2 陽性乳癌患者,在術前接受輔助治療後再開刀,接著接續術後輔助治療。如果腫瘤大於 2 公分、有淋巴結轉移、沒有達到病理完全緩解,屬於高復發風險之 HER2 陽性乳癌,需要更積極治療。
- 這些高風險患者可服用新一代口服小分子標靶藥物進行強化輔助治療,幫助降低復發的機會。
- 新一代口服小分子標靶藥物能夠穿過血腦屏障的特性,有助於預防及治療腦轉移,降低腦轉移及死亡風險。
- 本文轉載自 Care Online 照護線上《HER2陽性乳癌惡性度高、容易復發!新一代口服小分子標靶藥物強化輔助治療,顯著降低復發風險,專科醫師圖文解說》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接