
「下流老人」是近幾年日本出現的最新名詞,指的是那些沒有子女(或子女沒辦法供養父母),沒錢進安養院、也請不起看護來照顧自己的獨居老人,又老又窮又孤獨。你或許無法想像自己老了之後會是這般光景,「老了」也許離現在的你還有一段距離,但在台灣即將邁入高齡社會的此刻,我們對「老化」這件事有多少認知?
根據內政部 102 年底的人口資料推估,台灣 200 多萬的老人當中,有 217,855 人罹患失智症,佔老年人口的 8.09%。這個好發率隨著年齡增加而提高的疾病,目前還沒有根治的方法。沒辦法事後補救,有沒有辦法事前預防?「大家現在的想法是,不要等到疾病發生再來處理,而是要在還沒發生之前,先找出來哪些人未來有可能發病」,她是獲得今年(2016)吳健雄傑出女科學家新秀獎的台大心理系助理教授張玉玲,國內臨床神經心理學少數從事老年臨床研究的老師,主要針對未來極有可能罹患失智症的高風險群,例如輕度知能障礙(Mild Cognitive Impairment, MCI)做研究。
「我想念心理系的想法很單純,就是對人很有興趣,但真的進到心理系後發現,心理系比我想像的廣泛很多」,原先和大家一樣,以為念心理就是在念情緒的張玉玲,在台大心理系的第三年遇見花茂棽老師,就此結下她和神經心理學的不解之緣。
「大腦本身其實是讓我更著迷的,它影響到我們整個人如何行為思考。」台灣研究臨床神經心理學的人本來就不多,像張玉玲這樣年輕的就更少,但看看主計處的統計資料上頭寫著,台灣社會將在 2018 年邁入老年人口比例超過 14% 以上的高齡社會,2025 年就達到 20% 以上的超高齡社會。在社會面臨轉型的同時,對高齡長者醫療需求的相對性研究,能否跟上民眾老化速度,前景其實值得憂慮。

輕度認知障礙 罹患失智症的前哨站
老了其實不是問題,而是可能伴隨老化出現的種種疾病、照護所需要的醫療協助,社會福利有沒有能力即時銜接,才是老年人口日益增加的台灣面臨的最大隱憂。台灣目前有 18.74% 的人屬於輕微認知障礙(簡稱 MCI,約五萬多人),這個階段是介於正常老化到罹患失智症間的過渡地帶,可能會出現記憶力衰退、情緒反應遲緩等狀況,最後有 10~15% 比例的人會發展成失智症。為了能更早預防,張玉玲說:「很多時候我是在研究目前看起來還健康的人」。
這樣的研究方法,來自張玉玲在美國念書的經驗。她到社區中招募受測者,針對有可能罹患輕度智能障礙的長者進行簡單的心智功能診斷,企圖找出影響罹患失智症的關鍵因子。然而,這些資料蒐集都需要受訪者高度配合,畢竟要承認自己「失智」都不是那麼容易(看看電影《我想念我自己》女主角的故事),更何況是承認自己「有可能失智」,光想就覺得很有心理障礙。(延伸閱讀:認識早發性阿茲海默症)。「台灣老人跟國外不太一樣,大多時候還停留在『我沒生病,為什麼要看病』的思維裡」,挫折沒有讓張玉玲退縮,她反而因此明白自己研究的存在價值。
失智症知多少?
你對失智症了解多少?其實它不是單一的疾病,而是一群病症的組合,大致可分為因為腦神經細胞退化或病變引起的原發性失智症(約佔 70~80%)、與心血管疾病導致的續發性失智症(約 10~20%),症狀也不只是記憶力衰退,還包含語言能力、判斷力、注意力等全面性的心智功能減退,它是一種不正常的老化,嚴重到影響日常生活。對於為什麼會發生這些疾病,目前學界還沒有定論。
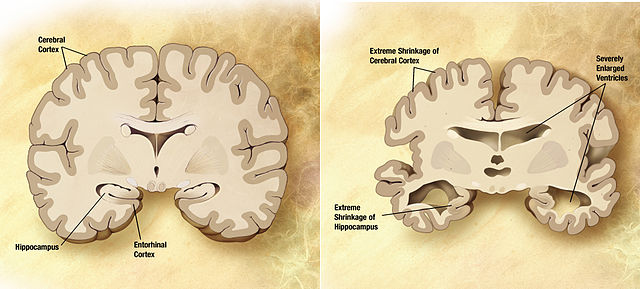
多數人對於失智症的診斷印象,大多停留在腦部影像或抽血,不過阿茲海默症的診斷是無法單用腦影像或是抽血檢查來判斷的,抽血主要是要排除因為其他生理疾病所造成的認知功能改變,例如維他命缺乏、甲狀腺功能低下等。阿茲海默症的診斷最終還是要依靠心智功能的評估來做診斷主要依據,透過一些臨床上標準化的神經心理測驗工具,來測量病人心智功能的表現,是不是明顯超過因為正常老化而造成的功能改變程度。不過其實這些只是用來排除「非」失智症的可能因素。
這件事說來簡單,但試想,失智影響的是大腦心智能力(認知、記憶、語言、思考),在還沒嚴重到影響生活時,你如何能夠判定自己/他人可能有失智傾向?
找出可能罹患 MCI 的高危險群
在醫療系統中,要篩選失智症很容易,但若想在社區中篩選可能發展成失智症的高風險群,就相對困難許多,主要是受限於測量工具的敏感度、使用上的方便性或成本考量。「這是為什麼我想去發展一些新的工具,根據我們對大腦以及認知歷程的了解,這些新工具可以在社區進行檢測」。未來若是工具完成,透過簡便的認知測驗在社區中就可以初步篩檢出未來可能罹患輕度知能障礙 MCI 的高風險群。
同時張玉玲也提到,心血管疾病、年齡、ApoE4 基因變異,都是罹患失智症的風險因子,「基因變異讓你的大腦比較沒有本錢抵抗老年失智」。由於失智症是一種持續進行的疾病,臨床經驗顯示,從 MCI 發展成失智症只需要幾年時間,但 MCI 之前的病程怎麼進行,就不是很清楚,提前找出潛在的 MCI 病患或是失智症的高風險個體,變成科學家們和時間賽跑的關鍵因素。
如何界定失智與正常?

由於正常老化過程當中也會造成功能上的改變,因此界定是失智還是正常老化的標準就變得很重要,多數時候科學家透過蒐集同年齡、性別、教育程度人的資料,找出一個標準化常模(意指一群人在測驗上的普遍水平或分布狀況),藉此判定病人的病況。張玉玲強調,常模有它的限制,對於功能已經不好的病人來說很適用,但是對於功能原本就很好的人未必是敏感的一套「標準」,因此必須建立更適合或是不同的參照標準、研發新的測量工具,讓結果的判讀上,能更敏感地反映出功能上細微且是與病理有關的改變,才能達到早期偵測的目的。
即使現在離目標還有段距離,但張玉玲樂觀的說,「我知道我們已經越來越近」。
我有沒有可能罹患失智症?
有時候,最簡單卻最重要的問題,最難回答。
對於這個進行中、不可逆的疾病,當前醫學恐怕只能提供這個問題最終答案的暫時版本。回台工作五年多,張玉玲頗多感觸,她希望最終能開發出簡單低成本的失智症初步篩檢工具,讓預防能落實在家庭或社區中,而不是一定得千里迢迢跑到大醫院做檢查,最後發現已經為時已晚。
有天我們都會變老,我想起自己家中的外公,時不時會看著我卻叫出別人的名字,是不是那也是自己未來的模樣?如果有天,我們能提早預見失智症的發生風險、及早治療,這一切或許可以變得不太一樣。


































