- 作者 / 照護線上編輯部
- 本文轉載自 Care Online 照護線上《失智症治療重點、照護資源,醫師圖文解說》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔

「醫生,我先生都會一直問同樣的問題,才剛講過的話,馬上就忘記。他從前愛看電視,現在卻連遙控器都不會用,而且常搞不清楚白天、黑夜。」老太太一臉擔憂地說,「前幾天出門去散步,結果竟然在公園迷路,走不回來。怎麼會這樣啊?」
員林基督教醫院神經醫學中心林君襄主任指出,失智症的症狀以記憶力退化為主,患者會反覆詢問相同問題,才剛講過一回頭又會再問,有些患者則會反覆購買同樣的東西,讓家屬相當困擾。
另外,患者的判斷力、計算能力、語言能力都會受到影響,整體的認知能力越來越差。失智症還會出現一些精神症狀,例如妄想、幻覺、憂鬱等,可能會誣賴別人偷他的錢、或是配偶有外遇的狀況。
「該如何區分老化健忘?還是失智症呢?」林君襄醫師舉例說明,「如果上週五帶長輩去看花展,長輩可能會忘記看過哪些花,但是失智症患者可能會記錯交通工具,嚴重的話甚至完全忘記去過花展。正常老化的健忘,可以透過寫筆記提醒自己;若是失智症患者,可能連寫筆記也沒有辦法提醒自己,而且失智症患者沒有病識感,會覺得自己一切正常。」
懷疑失智症該怎麼辦?
林君襄醫師解釋,失智症是一個總稱,它包含非常多種失智症,其中大概 6、7 成是阿茲海默症,另外還有血管型失智症、額顳葉型失智症、巴金森氏症失智症、路易氏體失智症、或是包含兩種以上失智症的混合型。

若懷疑家人有失智的狀況,要儘快至神經內科就診,醫師會透過較完整的檢查來診斷失智症。
抽血檢查是為了排除一些可以治療的疾病,例如甲狀腺低下、或長期吃素可能導致維生素 B12 缺乏等。影像檢查是為了排除腦瘤、外傷、水腦等問題。
臨床上,大多會使用「臨床失智症評估量表(Clinical Dementia Rating Scale,簡稱 CDR)」、「簡易智能測試(Mini-Mental State Examination,簡稱MMSE)」來進行評估。MMSE 會依照教育程度跟年紀去校正,分數越低代表越嚴重。CDR 會分成 0.5、1、2、3,代表疑似或極輕度、輕度、中度、重度失智症。
及早治療失智症,才能延緩病程
失智症的嚴重度不同,所需要的治療與照護也不相同,林君襄醫師強調,早期介入相當重要,倘若放任不理,患者的認知功能、生活功能將迅速衰退。
目前已有失智症的藥物能夠延緩病程,如果能夠提早警覺到失智症,並早期開始治療,患者的認知能力與生活能力可以被改善且延緩。
針對阿茲海默症造成的失智症,可考慮使用乙醯膽鹼酶抑制劑(Acetyl- cholinesterase inhibitor)或 NMDA 受體拮抗劑(NMDA antagonist)。乙醯膽鹼酶抑制劑可以減少神經傳導物質乙醯膽鹼的分解,改善認知功能;NMDA 受體拮抗劑可抑制 NMDA 受體的過度活化,延緩失智症惡化的速度。醫師會根據病情及健保給付條件來用藥,若能在失智症早期開始治療、按時服藥,有助於減緩病程。
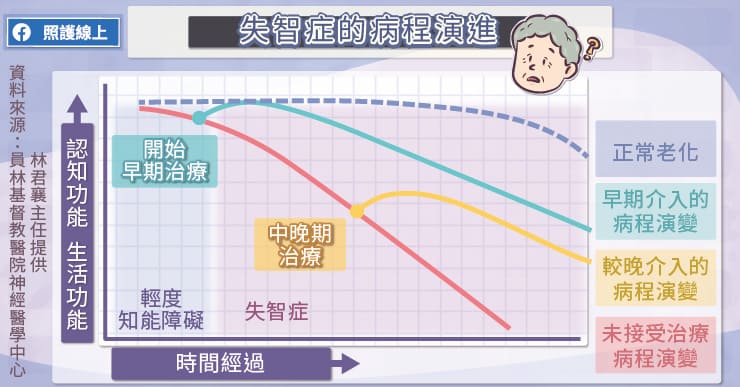
「假使到了失智症中晚期才開始治療,患者可保存的功能就會有些差距,也就是有無照顧自己的能力」林君襄醫師說,「早期介入治療就有機會可保存較多的認知與生活功能。」早期治療會有大概半年的時間,患者生活功能會變得更好,甚至接近正常老化的曲線。
由於失智症患者容易忘記吃藥或忘記吃過藥,有時還會一次吃掉好幾天份的藥物,建議可使用分裝藥盒或由照顧者餵藥,以確保用藥安全。
善用失智症照護資源
除了藥物之外,不同程度的失智症也需要不同的照護,林君襄醫師說明,目前有多種社會資源可以運用,包括「喘息服務」、「居家服務」、「家庭托顧」、「營養餐飲服務」、「安養服務」、「巷弄長照站」、「失智症團體家屋」等,提供給患者及照顧者各方面的協助。
「疑似或極輕度失智」患者若未接受治療,一年內進展到輕度以上失智症的機會達 15%,建議利用長照服務地圖尋找巷弄長照站、失智據點參加認知促進活動,有助維持認知功能。在患者仍有判斷力時,要把握機會討論相關法律問題,例如預立醫療決定、預立遺囑、遺產處置等。因為患者判斷力變差,較容易受騙,財務保管須更為謹慎。
「輕度失智」患者可透過巷弄長照站、失智據點獲取相關資訊,也能考慮參加日照機構。患者白天可至日照機構參加各種活動,維持社交功能。部分機構亦提供夜間臨時住宿,讓家屬或照顧者能獲得短暫天數的休息。由於失智症患者相當容易走失,務必事先準備,倘若走失48至72小時沒有得到救援,死亡率會提高三至四成。可以使用安心手鍊、智慧手環,讓患者穿著鮮豔、顯眼、容易辨識的衣服,並至警察局捺印指紋。
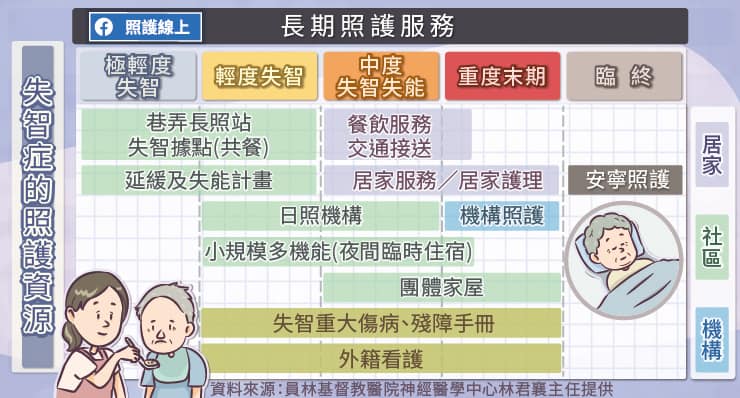
「中度失智」患者可能出現嚴重的行為問題或大小便失禁,可以考慮居家服務或機構收住。生活環境要預防跌倒,可安裝扶手、止滑條、減少障礙物、充足照明,減少意外發生的機會。
「重度失智」患者已經無法思考、表達,需要完全仰賴他人照顧,可能有吞嚥障礙、需要長期臥床,最後可能因為反覆感染而逝世。
「失智症照護牽涉生理、心理、家庭、社區等很多層面,」林君襄醫師說,「我們的失智症團隊有個案管理師、心理師,收案後個管師會每個月進行電訪,並依照失智家庭的狀況去規劃合適的長照資源。當家屬的壓力過大時,也有心理師可以諮詢、協助。」
貼心小叮嚀
林君襄醫師提醒,失智症並非單純的老化或健忘,如果發現家人出現重複發問、迷路、性格改變、判斷力變差、混淆時間地點、無法勝任原本熟悉的事物等狀況,務必盡快至神經科或精神科做進一步評估。
目前已有藥物能夠延緩失智症的病程,應及早接受治療,才有機會保存較多的認知能力與生活能力。同時,也建議家屬多善用各地區共照中心的資源,起初可協助疑似失智患者的就醫服務,再透過社區長照資源的輔助,延緩患者病程進展,並提供最適切的照顧建議。
- 本文轉載自 Care Online 照護線上《失智症治療重點、照護資源,醫師圖文解說》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接



































