本文接續上一篇:不只能夠「以毒攻毒」,當細菌從攻癌武器變成交通工具!細菌療法的今生(上)
在上一篇文章中,科學家透過梭菌屬 (Clostridium) 、沙門氏菌屬 (Salmonella) 研究了細菌治療癌症的效果,其中,雖然沙門氏菌沒有明顯的治療效果,但是卻啟發了科學家將細菌當作「運輸抗癌藥物的載體」的想法。
李斯特菌:偷偷藏到吞噬細胞裡面!
在日常生活中,若我們感染李斯特菌 (Listeria monocytogenes, L. monocytogenes) ,將會出現腸胃道症狀,嚴重者會引發如敗血症、腦膜炎等症狀,是最致命的食源性病原體之一,主要以食物為傳染媒介,其致死率甚至高過沙門氏菌及肉毒桿菌。
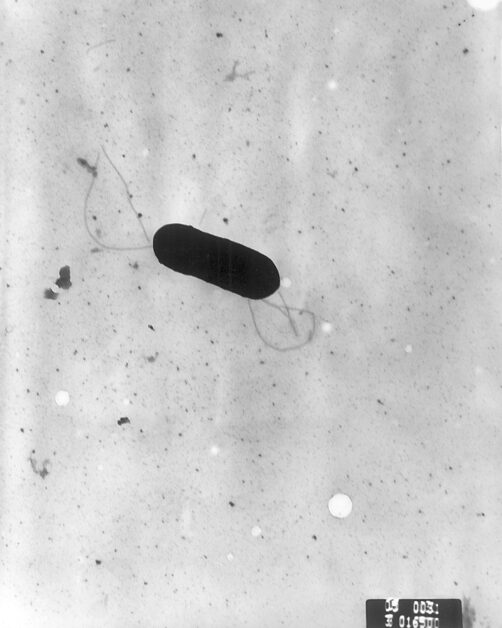
李斯特菌與沙門氏菌一樣,是兼性厭氧細菌,無論在缺氧、有氧的條件下均能夠生存,因此在細菌療法的考量下,科學家不用擔心當腫瘤失去微環境時,李斯特菌會失去治療的效果。
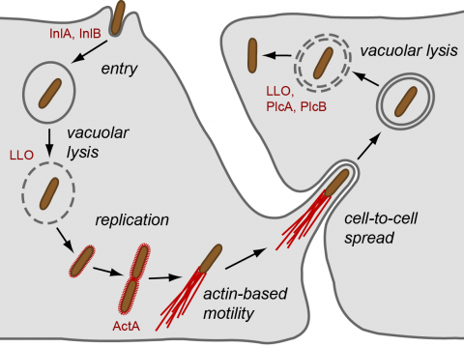
特別的是,李斯特菌也是兼性胞內寄生菌註1,可在吞噬細胞中生長,也可以在細胞外存活!
李斯特菌被吞噬細胞吞噬後,會分泌 listeriolysin O (LLO) 這個溶胞素註2破壞細胞膜,進而入侵到吞噬細胞的細胞質內,並在吞噬細胞的細胞質內繼續生長。這項讓免疫系統頭痛的特點,卻也成為科學家相中牠的原因。
負責撰寫「死亡筆記本」的吞噬細胞
人體的免疫系統由先天和後天組成,其中兩者的主要差異在於「專一性」。
先天免疫系統沒有專一性,只要辨識到非人體的病原體,就會啟動殺敵系統,當病原體感染人體後,受損的細胞會產生發炎反應。
而先天免疫系統的發炎反應會活化諸多細胞激素,吸引吞噬細胞和自然殺手細胞 (Natural Killer Cell,後稱 NK 細胞) ,前者會將被感染的細胞吞噬消化,後者則分泌毒素直接殺死被感染的細胞。
吞噬細胞還有另一個稱呼:抗原呈現細胞 (Antigen Presenting Cell, APC),APC 會把病原體的抗原放在自己的細胞膜上,就像是後天免疫系統的死亡筆記本一樣,藉此來提供訊息給後天免疫系統。
後天免疫系統具備高度專一性,一旦接受到 APC 提供的死亡筆記本,便會開始「量身訂製」殺敵策略。
執行後天免疫系統的主角,主要為兩類淋巴細胞: B 細胞和 T 細胞。B 細胞會分泌專一性的抗體,可與病原體的抗原結合,使其失活;T 細胞則會訓練一批殺手,專門獵殺帶有抗原的病原體或細胞。
後天免疫系統還有「記憶性」,當人體再被同樣的病原體感染後,後天免疫系統會徵招曾經參戰的 B 細胞和 T 細胞,達到更快速的制敵效率,而這個記憶特性,也是疫苗背後的基本原理。
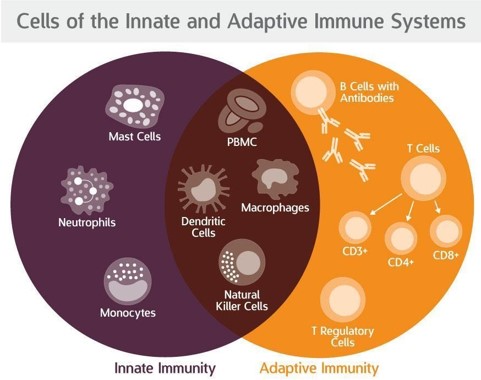
先天和後天免疫系統並非各自為政,而是相輔相成。其中可看出,APC 是連結兩者的重要橋梁。
癌細胞會分泌抑制免疫細胞的細胞激素,讓 NK 細胞和吞噬細胞無法作用。NK 細胞不作用,就無法毒殺癌細胞;吞噬細胞不作用,腫瘤的抗體資訊就無法傳遞給後天免疫系統,身體就無法針對癌細胞產生專一的殺滅作用。
看到這兒你可能會想,這些和李斯特菌的兼性胞內寄生有什麼關係?關係可大了!
逼迫細菌把腫瘤送入「死亡筆記本」!
正常來說,雖然李斯特菌會引起先天免疫系統的反應,但因李斯特菌可以靠 LLO 逃避吞噬細胞的消化,使得吞噬細胞無法紀錄牠的抗原訊息,也無法將抗原訊息提供給後天免疫系統。
科學家:嘿嘿,那我就改造你!
當李斯特菌跑到吞噬細胞體內後,科學家強迫李斯特菌不斷生產抗原,而且這些抗原還會跑到吞噬細胞表面,讓本來不能呈現抗原的吞噬細胞,瘋狂表現腫瘤抗原,並藉此活化後天免疫系統。
在動物實驗中,即使是沒有被改造完全、不會生產腫瘤抗原的李斯特菌,本來就具有腫瘤組織專一性,也和活化先天免疫系統的能力,確實能讓腫瘤消退9。
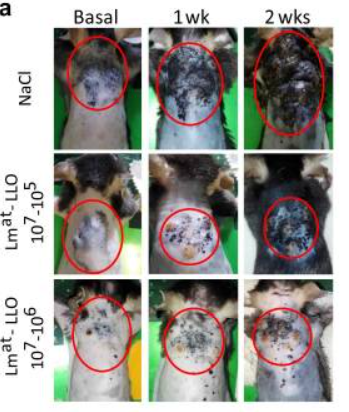
當科學家改造李斯特菌之後,實驗結果顯示,李斯特菌除了保持「腫瘤專一性」和「活化先天免疫系統」的兩個能力,科學家也確實觀察到後天免疫系統被活化了1。也就是說,腫瘤抗原真的成功被李斯特菌帶入吞噬細胞,而且被記上死亡筆記本、送給後天免疫系統了!
動物實驗的結果讓科學家們相當振奮,他們認為,這代表「將李斯特菌當成表達腫瘤抗原的載體,並活化後天免疫系統」的想法,確實可行!
讓人沮喪的臨床試驗結果
雖然動物實驗的結果不錯,但李斯特菌,在臨床試驗的結果可謂差強人意。
在最新的臨床試驗中,科學家對 15 位有侵犯性子宮頸癌的病患,施打了帶有腫瘤抗原的李斯特菌。所有的病患在施打後,都有很強烈免疫反應,但只有 6 位病患的腫瘤有消退(其中一位雖有消退,但腫瘤很快又長回);7 位病患的腫瘤沒有改變;2 位病患因強烈的免疫反應死亡2!
從李斯特菌的臨床試驗來看,這種作法確實能活化後天免疫系統,也有消滅腫瘤的效果,但牠的「安全性」卻是非常嚴重的問題。
雖然用於治療的李斯特菌已減毒,但這種減毒李斯特菌的感染,仍會引起人體過度強烈的免疫反應,何況李斯特菌還會逃到吞噬細胞內,讓免疫細胞難以消滅,因此如何平衡毒性和治療性,是科學家們接下來的研究重點。
瘋狂的細菌療法,仍未到此為止
本文所簡介的梭菌、沙門氏菌、李斯特菌,是目前學術上最多人研究的 3 種細菌療法,除了這 3 種細菌療法外,還有更多我們並不清楚也並不瞭解的做法,永遠不要小看科學家們的腦洞,他們將各種奇思妙想融合到細菌療法中,造就許多遠比上面更瘋狂的方法3。
透過本文,大家也可以發現細菌療法仍有不少侷限,例如動物實驗和臨床試驗的結果之間的巨大鴻溝、治療性與安全性的平衡等等問題,都是科學家們必須正視的難題。
未來細菌療法究竟該往何處走,又有哪些難解的挑戰需要被克服?下期,也是細菌療法的最終章,將帶大家一起看看細菌療法的挑戰與展望。
註釋
- 兼性胞內寄生菌:可以在寄生於細胞內,在細胞外也可以存活。
- 溶胞素:一類由微生物、植物或動物分泌,對特定細胞有毒性的物質。溶胞素會因對某一類細胞具有特異性而獲得相應的名稱。例如專門裂解紅血球,並使其釋放出的胞內血紅蛋白的溶胞素,就被命名爲溶血素。
參考資料
- Jahangir A, Chandra D, Quispe-Tintaya W, Singh M, Selvanesan BC, Gravekamp C. Immunotherapy with Listeria reduces metastatic breast cancer in young and old mice through different mechanisms. Oncoimmunology. 2017 Jul 5;6(9):e1342025
- Maciag PC, Radulovic S, Rothman J. The first clinical use of a live-attenuated Listeria monocytogenes vaccine: a Phase I safety study of Lm-LLO-E7 in patients with advanced carcinoma of the cervix. Vaccine. 2009 Jun 19;27(30):3975-83. doi: 10.1016/j.vaccine.2009.04.041. Epub 2009 May 3
- Torres W, Lameda V, Olivar LC, Navarro C, Fuenmayor J, Pérez A, Mindiola A, Rojas M, Martínez MS, Velasco M, Rojas J, Bermudez V. Bacteria in cancer therapy: beyond immunostimulation. J Cancer Metastasis Treat 2018;4:4.
- Pizarro-Cerdá, J., Kühbacher, A., & Cossart, P. (2012). Entry of Listeria monocytogenes in mammalian epithelial cells: an updated view. Cold Spring Harbor perspectives in medicine, 2(11), a010009.
- Lindahl, G. (2019). The effects of flaxseed and tamoxifen on the inflammatory microenvironment in normal breast tissue and in breast cancer (Vol. 1714). Linköping University Electronic Press.
- Vitiello, M., Evangelista, M., Di Lascio, N., Kusmic, C., Massa, A., Orso, F., … & Poliseno, L. (2019). Antitumoral effects of attenuated Listeria monocytogenes in a genetically engineered mouse model of melanoma. Oncogene, 38(19), 3756-3762.
細菌療法系列文章
- 太瘋狂了!注射細菌,竟然能夠「以毒攻毒」打敗癌細胞?細菌療法的前世(上)
- 太瘋狂了!注射細菌,竟然能夠「以毒攻毒」打敗癌細胞?細菌療法的前世(下)
- 不只能夠「以毒攻毒」,當細菌從攻癌武器變成交通工具!細菌療法的今生(上)
- 不只能夠「以毒攻毒」,當細菌從攻癌武器變成交通工具!細菌療法的今生(下)