- 作者/郭孝齡醫師
- 本文轉載自 Care Online 照護線上《這種痠痛不單純!早上起床關節僵硬緊繃,自體免疫性關節炎醫師圖解》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔

工作忙碌一整天,大家或多或少都曾有腰痠背痛的經驗,多數的腰痠背痛與搬重物、姿勢不良有關,通常稍作休息後可逐漸緩解。然而,有些關節炎可不單純,症狀會一直持續,千萬不能輕忽。
恩主公醫院過敏免疫風濕科主任郭孝齡醫師指出,當體內的免疫系統錯亂時,持續產生抗體及細胞激素侵犯組織器官,使身體持續發炎,就可能是所謂的自體免疫性關節炎。
常見症狀為關節紅腫熱痛或晨僵,若延遲就醫,嚴重恐導致不可逆關節變形與相關共病,如虹彩炎、乾癬、發炎性腸道疾病、心血管疾病等。目前臨床上常用藥物如非類固醇消炎止痛藥(NSAIDs)、類固醇、免疫調節劑、生物製劑。
醫師會依患者病況搭配不同的藥物組合。隨著醫學技術進步,近年已發展出多款治療自體免疫關節炎且獲健保給付的生物製劑,及早使用除可緩解關節症狀,亦可同步預防相關共病產生。
晨間僵硬、緊繃要提高警覺
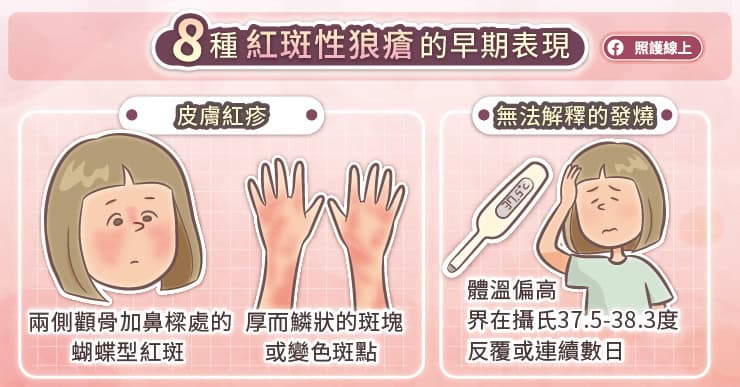
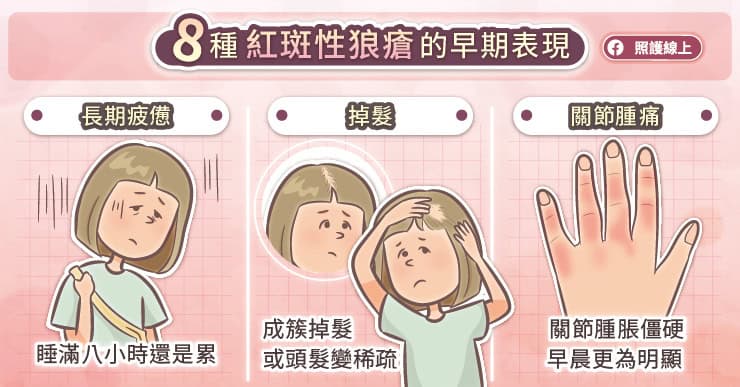
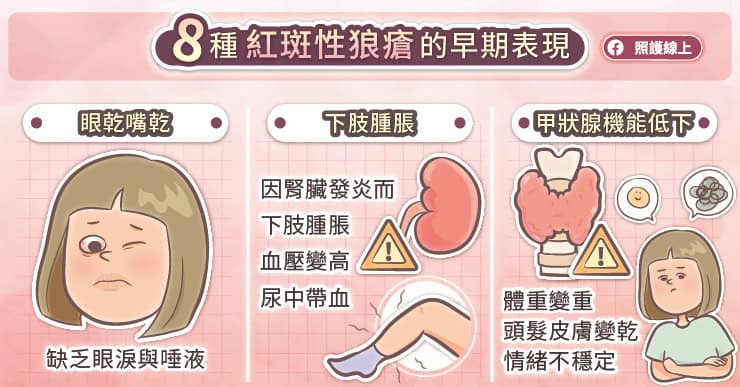
郭孝齡主任解釋,常見的自體性免疫性關節炎包含類風濕性關節炎、乾癬性關節炎、僵直性脊椎炎、紅斑性狼瘡等。
類風濕性關節炎好發於 50 歲以上中年婦女,早期症狀包含早上起床時手腳小關節僵硬、腫脹發痛、痠痛無力及轉成慢性關節發炎等,嚴重可能破壞關節軟骨和骨頭。
僵直性脊椎炎則好發於 20~30 歲年輕成年男性,初期症狀不明顯較難立刻察覺,症狀通常有晨起後下背疼痛、背部晨僵超過半小時,但隨著身體開始活動後可稍獲緩解。
乾癬性關節炎常好發於 40 歲左右之乾癬患者,皮膚病灶主要於頭部及四肢軀幹外側,是乾癬最主要的併發症,據統計約有 3 成乾癬患者會併發乾癬性關節炎,常見症狀如關節紅腫熱痛、腳後跟疼痛、指甲小凹洞指甲下黃色油滴狀等。
一般關節痠痛通常休息後可改善,但自體免疫性關節炎則是休息後也不見得改善。郭孝齡主任指出,患者每天早上起床時會感到關節僵硬、緊繃、腫脹,甚至活動度受限,平時能夠做到的動作,可能難以達成,甚至沒辦法握緊牙刷、擰毛巾穿內衣套襪子等,對日常生活造成很大困擾。
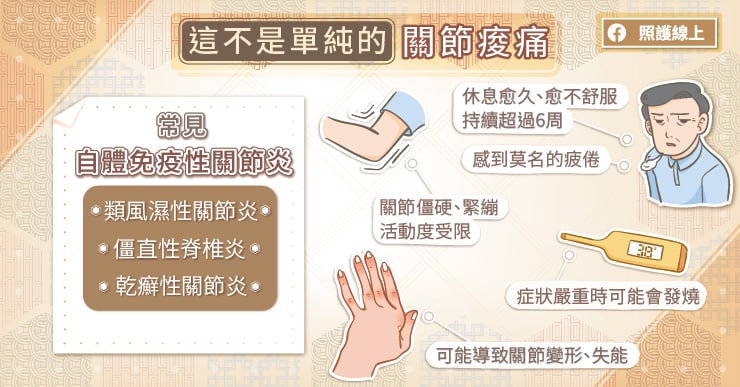
「因為身體處於慢性發炎的狀態,患者會感到莫名其妙的疲倦、吃不下飯、精神不濟,睡眠又不好。病情較嚴重的時候,也可能會發燒。」郭孝齡主任表示,「如果有持續六週以上的關節不適,最好要就醫檢查。」
郭孝齡主任提醒,若患者放任關節處持續發炎,關節可能遭到侵蝕,而逐漸變形、甚至失去功能。及早發現、及早治療,才能避免關節遭不可逆的破壞。
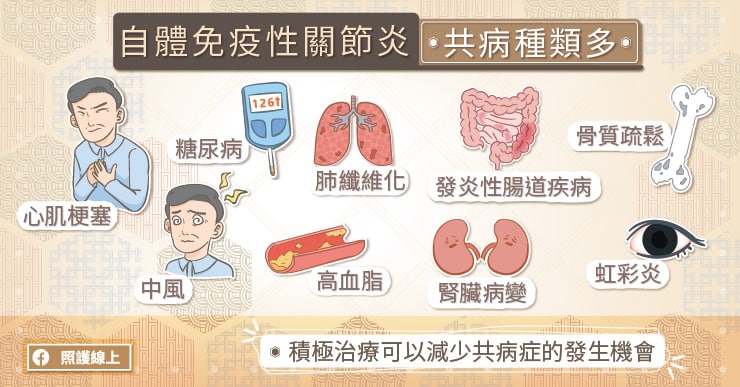
共病種類多,早期積極治療
郭孝齡主任提到,自體免疫性關節炎源於體內免疫系統失調,除造成關節炎症狀,還會影響其他器官,引起多種共病。常見共病包括心肌梗塞、中風、糖尿病、高血脂、骨質疏鬆、肺纖維化、虹彩炎、鞏膜炎、貧血及發炎性腸道疾病等。
罹病時間愈長、愈晚接受治療,就有愈高的機會出現共病。因此自體免疫性關節炎患者不僅應及早治療關節炎症狀,同時也要注意關節外症狀,以降低共病症對日常生活的影響。
發炎性關節炎治療、保養重點
郭孝齡主任說:「台灣很多患者會尋求民俗療法,因而延誤就醫的最佳時機,患者缺乏適當的治療,就會增加出現共病的機會,故及早正確至過敏風濕免疫科就診很重要。」
郭孝齡主任分析,自體免疫性關節炎的治療目標除減輕症狀,也要調節體內免疫功能、緩解發炎。常用的治療藥物包括非類固醇消炎止痛藥(NSAIDs)、類固醇、免疫調節劑以及生物製劑。醫師會根據患者病情嚴重程度,搭配不同的藥物組合。近年來隨著醫學技術進步,已發展出多款用於治療自體免疫關節炎的生物製劑,可說是革命性的治療,利用更精準的治療機轉,提供患者更好的治療成效。
郭孝齡主任補充,雖然治療「武器」多樣,但仍需配合醫師治療才能發揮較佳的效果,其中,治療的時機點是關鍵,早期發現、早期介入、持續治療,才能降低出現共病、失能的機會;此外患者日常生活的配合也很重要,倘若繼續抽菸喝酒、體重過重,治療成效也都會打折。
郭孝齡主任分享,「多年前門診有位類風濕性關節炎的女性患者,起初醫師先安排她服用三個月的藥,但成效不佳,經與醫師討論,改自費使用當時尚未獲健保給付之生物製劑治療。除了生物製劑的優秀成效,該患者也很注重自己的健康,相當積極配合醫師治療,至今已穩定追蹤了二十年,病情控制得很穩定,平時可享受與一般人無異的生活。」
目前健保對於這類生物製劑採有條件給付,若患者病情符合給付標準,醫師即可協助申請使用,及早搭配使用生物製劑,除可緩解自體免疫性關節炎造成的發炎,保護關節,亦可提早預防相關共病產生。
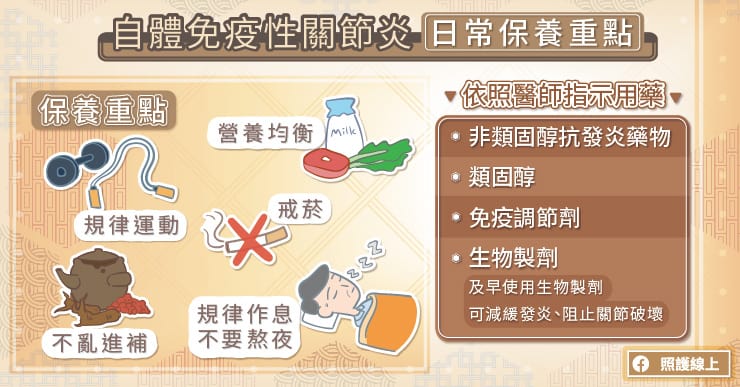
因自體免疫性關節炎屬於自體免疫疾病一環,建議患者平時最好維持規律作息、避免熬夜。規律運動有助維持關節活動度,建議每天至少三十分鐘,郭孝齡主任說,「通常會建議患者找到自己喜歡的運動,才會比較持久」。
飲食方面應以營養均衡為原則,盡量減少糖份及重口味飲食、加工食品的攝取,此外也應避免隨意進補,這些補品中可能含有讓關節發炎加劇之食材,建議食用前可先與醫師討論,以免治療成效功虧一簣。
- 本文轉載自 Care Online 照護線上《這種痠痛不單純!早上起床關節僵硬緊繃,自體免疫性關節炎醫師圖解》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接