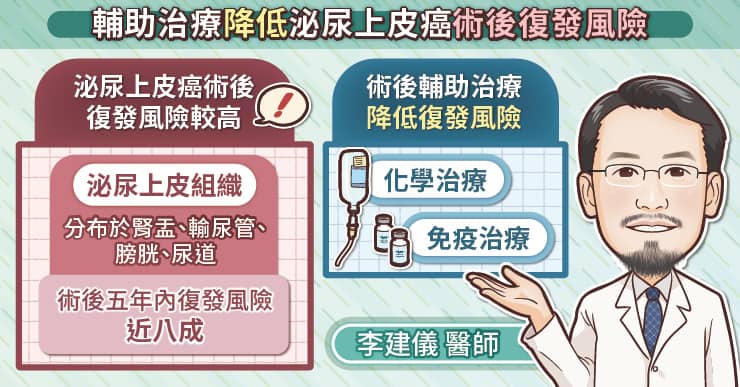
簡單理解什麼是癌症免疫療法
2018 年的諾貝爾生理醫學獎,讓屬於腫瘤免疫學 (immuno-Oncology, IO) 領域的「癌症免疫療法」成了眾所矚目的議題。
獲獎的詹姆斯.艾利森 (James Allison) 博士和本庶佑 (Tasuku Honjo) 博士,他們所研究的是一種可用來治療癌症的藥物,稱為「免疫檢查點抑制劑 (immune checkpoint inhibitor)」。
癌症的治療是近幾年醫學研究的一大重點,究竟什麼是「癌症免疫療法」?什麼又是「免疫檢查點抑制劑」?這樣的方法又有什麼特別,讓其被視為癌症治療近幾年的一大突破呢?
癌症免疫療法其實是一個統稱,從廣義層面來看,只要藥物作用位置不是針對癌細胞本身,而是通過「強化人體免疫系統去擊殺癌細胞」來達到治療效果,都可算是癌症免疫療法。
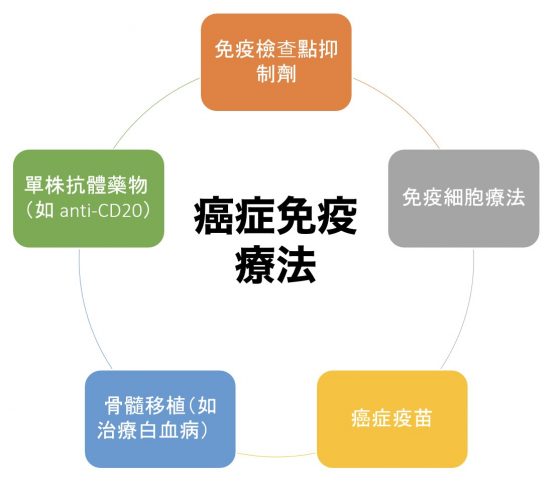
如下圖所示,免疫檢查點抑制劑就屬於癌症免疫療法的其中一種,其他還包括 2018 年台灣剛開放的細胞治療,還有骨髓移植(如治療白血病)、癌症疫苗、或是單株抗體藥物(如 anti-CD20) 等。由於近幾年免疫檢查點抑制劑在癌症治療上有了重大突破,也使得一談到癌症免疫療法,往往常是意指免疫檢查點抑制劑。
免疫檢查點抑制劑如何治療癌症?
免疫檢查點抑制劑的治療原理是基於「免疫監測 (immunosurveillance) 」這項假說,意思是指人體免疫系統能夠利用像是警察巡邏的機制,來辨識並消滅腫瘤細胞;但是腫瘤細胞也會透過一種稱為「免疫編輯 (immunoediting) 」的策略,來躲避免疫系統的攻擊。
延伸閱讀:如果想要更詳細了解免疫監測假說,可參考「腫瘤微環境不只是你追我跑」。本文這裡簡單帶過,讓我們把重心放在治療原理。
腫瘤細胞這個體內罪犯,為了不想輕易被當警察的免疫系統抓到,發展出了一種躲避策略,就像是罪犯在身上帶著很多張良民證或好人卡,在警察路邊臨檢時以之輕易地瞞混過關。
轉換為科學術語來說,腫瘤細胞上會表現很多可抑制免疫 T 細胞活性的分子,就能通過免疫 T 細胞的檢查哨,腫瘤細胞表現的這些分子也等於是通知免疫系統無需攻擊的訊號。

而此一免疫系統控制的樞紐機制就被稱為「免疫檢查點」。已知有相當多種分子類型都有這樣的功能,其中一類也成功作為治療標的,分別是表現在腫瘤細胞的「程序性細胞死亡蛋白配體-1 (programmed death-ligand 1, PD-L1) 」,以及相對應在免疫細胞上的「程序性細胞死亡蛋白受體-1 (programmed cell death protein 1, PD-1) 」。
PD-L1 與 PD-1 之間,我們也可以想像成是門禁卡與讀卡機的關係,腫瘤細胞若是刷卡沒過關就會啟動警衛免疫系統。因此,醫學上開發出阻斷 PD-L1 或是 PD-1 的抑制劑,就能讓免疫系統活化,進而達到消滅腫瘤的效果。
免疫檢查點抑制劑的特色與優點
過去的 19 世紀癌症治療僅關注於腫瘤細胞本身,並發展出如化學藥物的毒殺性治療方法。然而化療的副作用極大,令人聞之色變,就像是先傷己後傷敵的武功七傷拳,往往是傷了癌症一千,卻自損八百。
因為化療的專一性不高,後續又發展出標靶藥物,能夠專一的作用在腫瘤細胞,可惜的是標靶治療只能一定程度延長患者的生命,視癌症種類經過一段時間很容易出現抗藥性。
直到 20 世紀癌症免疫療法出現,將焦點轉移到人體最強的防禦武器「免疫系統」,這也帶來治癒癌症與長期存活的希望。縱觀癌症治療的發展史,就如同把武功從自傷傷敵的七傷拳,轉換成能克敵弱點的一陽指。
目前免疫療法已成為很多晚期癌症患者心目中最後一根救命稻草,理由是晚期患者的體能可能無法負荷化療帶來之副作用;標靶藥物雖然有效,不過在用藥一段期間後,終究會出現抗藥性;而免疫檢查點抑制劑卻有機會讓癌症獲得長期的控制。
由於免疫檢查點抑制劑是借著免疫系統的刀來殺死腫瘤,所以有著毒性較低並且治療耐受性較佳的優勢。對免疫檢查點抑制劑有治療反應的患者,也能獲得比起化療更長的存活期,以及較好的生活品質。
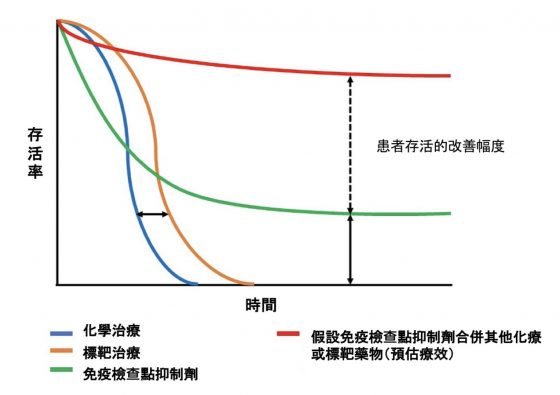
以致死率極高的晚期惡性黑色素瘤為例,在免疫檢查點抑制劑治療後,患者的 2 年整體存活率 (overall survival rate) 還可高達 45~60% 7,存活曲線如下圖所示,患者更能獲得長期存活的機會(綠線),假如合併其他化療或標靶藥物則預估療效能再有所提升(紅線)。
根據一篇分析 19 項第三期臨床試驗(共 11,640 名患者)的研究8,存活時間超過存活期中位數 (median overall survival) 2 倍的患者比率是免疫檢查點抑制劑高於化療 (30% vs 23%),而能達到持續有效 (durable response) 的比率更高出了 2.3 倍 (25% vs 11%)。由於擁有這些優點,免疫檢查點抑制劑已逐漸讓癌症成為一種可以控制的慢性病。
免疫檢查點抑制劑難道沒有缺點嗎?
第一項缺點就是藥費昂貴,健保署資料顯示每人每年所需費用高達 200~400 萬元,所以如果要自費使用,免不了要確認是否有足以支付療程費用的財源,不過 2019 年 4 月起健保已提供限額、限定資格申請的給付(延伸參考:癌症免疫檢查點抑制劑藥品給付規定)。
除了口袋深度的問題,免疫檢查點抑制劑也並非完全沒有副作用,用藥後可能會使得免疫系統過度活化而誘發「自體免疫疾病」,從輕微到嚴重的副作用都有可能出現,較為常見症狀包括疲倦、搔癢症、皮疹、噁心、腹瀉及食慾下降。
此外,單獨使用免疫檢查點抑制劑的治療反應率僅在某些特定的癌別較高,而某些情況如跨癌別的情況下大約只有偏低的 20~30%反應率。換句話說,在這種情況下將近有七至八成的機率是沒效的,而且治療反應又比較慢,必須等 2 至 3 個月才能看出效果。
再加上免疫檢查點抑制劑發展至今的時間還不夠久,對於有效的患者,無法確定何時才是停藥的最佳安全時機,不會因此而復發,患者也不可能持續負擔高昂的醫藥費。
綜合上述的優缺點,將免疫檢查點抑制劑與其他癌症療法的特性比較於下圖(癌症治療十分複雜,此處僅是簡略概觀)。
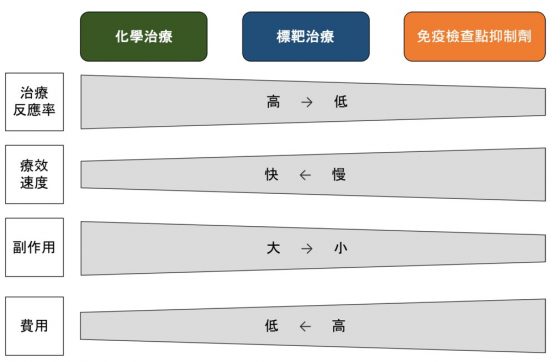
免疫檢查點抑制劑的未來發展
未來除了發展其他免疫治療新靶點,最要緊的為先解決現有痛點,其中最被詬病的就是治療反應率不夠高,所以有不少的臨床研究,開始著手將免疫檢查點抑制劑合併化療或標靶藥物,或是甚至合併兩種不同免疫檢查點抑制劑,現有研究已證實這些聯合療法已經能將原本 20~30% 的反應率,大幅提升至 50~70%,但是相對的副作用也會跟著加乘上去。
不過,相信隨著世界各地臨床研究的努力,一定能夠針對不同癌症找出最適合的聯合療法,並且達到療效與副作用風險之間的平衡點。
在講求精準醫療的時代,免疫檢查點抑制劑對哪些患者族群最有效?這也是有待決解的重要問題。現階段在臨床上主要已在運用的生物標記(biomarker)是檢測腫瘤上的 PD-L1 表現量,理論上越高的治療反應會越好。
但在實際狀況中,在某些癌別的預測準確度仍不夠好。所以其他相關生物標記也正在開發與追求檢測方法標準化,例如檢測腫瘤突變量,或是檢測免疫調節基因是否有突變等方法。未來應該藉由掌握多種生物標記指標,才能協助醫師更完整地評估免疫檢查點抑制劑的療效。
每種癌症的特性不同,治療方式也不同,現今免疫檢查點抑制劑展現出極佳的治療潛力,但並非適用於每種癌症或每個患者。像是腫瘤很大或症狀危急的患者就不適合等待免疫檢查點抑制劑慢慢發揮效果,須採用可快速控制病情的化療或標靶治療。
癌症治療仍持續在進展中,現行沒有方法是萬靈丹,面對新出現的免疫檢查點抑制劑治療法,應視為癌症治療的其中一種選項,依循醫生建議的情況使用,而不是唯一的方法。
參考資料:
- 全民健康基金會,好健康第 47 期,免疫療法擬納健保關鍵問答了解抗癌新療法
- Jaffer Yang,泛科學,「細胞治療」在台正式開放,但你對它又了解了多少?
- 楊朝傑,CASE 報科學,腫瘤微環境不只是你追我跑
- 李岳倫,泛科學,顛覆癌症治療的革命──免疫治療的前世、今生與未來
- Schirrmacher V. Int J Oncol. 2019;54:407-419. From chemotherapy to biological therapy: A review of novel concepts to reduce the side effects of systemic cancer treatment (Review).
- Ardolino L, et al. Aust Prescr. 2019;42:62-67. Immune checkpoint inhibitors in malignancy.
- Ryu Lab of Hackensack Meridian Health. Kaplan-Meier survival curves of currently available therapies for melanoma.
- Pons-Tostivint E, et al. JCO Precision Oncology. Feb 6, 2019. Comparative Analysis of Durable Responses on Immune Checkpoint Inhibitors Versus Other Systemic Therapies: A Pooled Analysis of Phase III Trials.
- 衛生福利部中央健康保險署,癌症免疫新藥專區
- Schmidt EV. Semin Immunopathol. 2019;41:21-30. Developing combination strategies using PD-1 checkpoint inhibitors to treat cancer.
- Havel JJ, et al. Nat Rev Cancer. 2019;19:133-150. The evolving landscape of biomarkers for checkpoint inhibitor immunotherapy.