暨之前引發軒然大波的新聞發表後,賀建奎今日 (2018/11/28) 出席了在香港大學舉辦的第二屆國際人類基因組編輯峰會。主辦方在演講前聲明對於賀的發表事情並不知情,而他提交給會議的簡報檔中也沒有提到關於雙胞胎的資訊。但是基於言論自由以及各方考量,他們最終決定讓賀如期上台發表,並且給予了他獨立的發表和提問環節。

前期實驗在動物身上修改 CCR5 蛋白
在發表前,賀首先向自己任教的南方科技大學致謝,但他表示校方對其研究內容事先並不知情。而研究資料已投稿期刊,等待審查。賀所發表的部分橫跨了動物實驗,而後到人類胚胎,首先使用了老鼠、猴子,最後則是如今舉世聞名的雙胞胎。
賀建奎表示,HIV 病毒造成了嚴重的問題,尤其在南非地區感染率極高,嬰兒在出生後的幾個月感染機會高,往後也會有歧視等問題,這是他想要解決的部分。賀所採用的作法是使用 CRISPR/Cas9 技術去修改人類胚胎的 CCR5 (C-C chemokine receptor type 5) 蛋白,以避免其感染 HIV 病毒。
- 註:有另一類型的 HIV 病毒,是利用輔助受體 CXCR4 來感染 T 細胞,換言之,即便編輯了 CCR5 基因,嬰兒仍可能被感染。
研究首先以老鼠進行實驗,編輯十分有效,被破壞 CCR5 基因的小鼠到了第三代時,其心、肝、肺、胃等部位的組織切片與行為都與一般未經編輯的小鼠沒有差別,並沒有出現健康問題。其後,賀的團隊利用了猴子進行實驗。
- 脫靶效應 (off-target):CRISPR 為相對新穎的技術,使用時有機率會意外修改到其他基因,而這類基因突變的影響可大可小、難以預測。
基因編輯雙胞胎,似乎有點兒小差錯
賀建奎的團隊利用了 HIV/AIDS 的自助團體尋找自願受試者,而後共有 8 對伴侶報名,1 對中途退出。參與研究的 7 對伴侶都是父親為 HIV 陽性、母親為 HIV 陰性(未感染)。根據現場的問答,賀表示共有 30 個受精卵細胞成長到胚胎階段,其中 70% 經過編輯。
現在已經平安出生的雙胞胎是露露和娜娜,她們的母親是首先懷孕的。
- 註:另有一對目前正處於化學性懷孕階段 (chemical pregnancy),意即早期受孕但未確定著床成功。
為了要確認整個成效,研究團隊在整個過程中進行了各種檢測(對真的是測了又測、測了還測),讓我們看看他們究竟測了些啥:
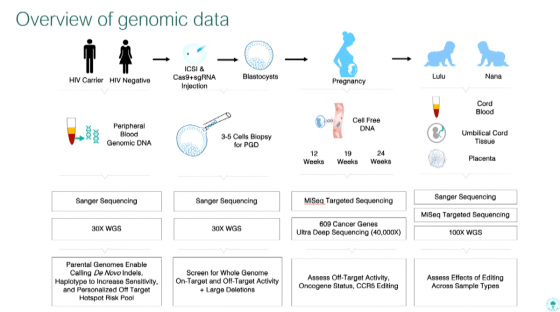
當露露和娜娜的受精卵經過修改、發育成囊胚 (blastocyst) 時, 團隊取 3-5 個細胞出來定序,這是 PGD(Preimplantation genetic diagnosis,胚胎著床前基因診斷)。而後將囊胚植入母親子宮,懷孕期間持續以胎兒的游離 DNA 檢測。等到小孩出生後,再取臍帶血、胎盤等組織進行基因檢測。
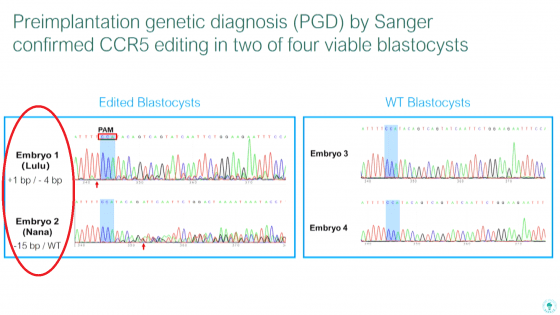
PGD 檢測結果顯示,露露兩條 DNA 的 CCR5 基因皆有被編輯,其中一條多了一個鹼基對,另一條少了四個鹼基對,成功使兩套基因都無法製造出 CCR5 蛋白。但娜娜就不一樣了,其中一條少了十五個鹼基對,會製造出結構較不穩定的 CCR5 蛋白(只是病毒較難結合上去),另一條沒有編輯成功,還是原本的序列,也就是說,娜娜仍然可以製造功能完全正常的 CCR5 蛋白,不能免疫於 HIV 病毒。
編按:此段為 11/29 新增
雖然露露的兩套基因都編輯成功,但露露似乎出現了脫靶造成的突變狀況,團隊判斷突變的位置是非編碼 DNA,附近也無轉錄因子,因此「可能」不會造成重大的影響。賀建奎宣稱父母充分了解兩個胚胎的狀況後,仍然同意懷下露露和娜娜。
- 註解(11/29新增):兩個胚胎皆在植入母體前就已知曉各有問題,尤其是娜娜不僅未達成實驗目的,還要承擔基因編輯的風險。賀建奎可以選擇中止實驗,但他仍然繼續實驗讓他們出生在世界上,動機令人費解。
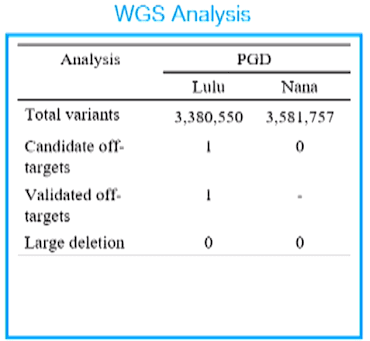
不過,在出生後的定序,賀建奎則表示並沒有出現任何問題。
- 註解:這個薛丁格般的脫靶是怎麼回事?其實,這的確有可能發生,畢竟 PGD 檢測的階段樣本數較少,有誤測的可能。但在沒有確切看到論文之前,我們無法妄下定論。
賀建奎說,團隊在未來 18 年,都會持續進行追蹤,直到雙胞胎成年。
發表結束後,眾多疑問仍未平息
針對實驗本身,賀建奎選擇修改 CCR5 基因,然而科學界對於 CCR5 的功能真的充分了解嗎?破壞它既有的功能,會不會造成其他問題,譬如說更容易得到流感?而且實驗的受試者為父親帶原 HIV 病毒,母親沒有帶原,原本人工授精的流程中就已經進行精子洗滌,可以安全生出未感染病毒的嬰兒,那麼修改胚胎基因實在是非必要而多餘的舉動,此實驗的正當性令人質疑。
對此,賀建奎再次強調愛滋病的問題,表示他實驗的目的並不只針對本案而已,而是為了全球數百萬個有感染風險的孩童。然而針對修改 CCR5 基因本身引發的風險則沒有做正面回覆。
另外,也有許多關於研究倫理的問題。會場多次有人提出質疑,認為賀的研究並未通過適當的倫理審查。在問答中,賀亦並未明確回應研究內容經歷哪些單位的倫理審核。
- 註解:他只說實驗前跟很多人討論過內容,這實在難以被判定為經歷完善的討論審查。

而針對事前告知方面的質疑,賀則表示研究共經過兩輪的告知:首先,團隊成員先與自願者會談了兩個小時,而在一個月後,自願者到達深圳,並由賀建奎與另外兩名觀察員與他們會談了 1 個多小時。他宣稱自願者都是高知識份子,非常理解這個研究的可能發展和風險。在第二次會談時,賀進行了知情同意 (Informed Consent)。但他的團隊是否有受過相關訓練呢?對此,他僅說自己在起草同意書前有讀過指導方針。
最後,大家都很想知道更多關於這對雙胞胎及其父母的資訊。賀建奎說中國的法律禁止揭露愛滋病帶原者的資訊,其他研究資料現已公開。他表示並不想干涉孩子的未來,他尊重兩個孩子。最後,他回答主持人的提問,說如果是自己的孩子,他也會願意進行同樣的嘗試。
- 賀建奎所在研究室的相關資料:http://www.sustc-genome.org.cn/research.html(編按:中國網站,可能會被下架)
目前階段,賀建奎實際研究資料尚未正式發表,而他對於會議上許多疑問亦含糊以對。第二屆國際人類基因組編輯峰會的主辦方在賀演講之前即表明,對相關事件於明日大會將有正式聲明發表。





































《運動基因》立體封面72dpi.jpg)




