- 本文轉載自諾貝爾化學獎專題系列,原文為《【2020諾貝爾化學獎】基因剪刀:一個改寫生命密碼的工具》
- 譯者 / 蔡蘊明|國立臺灣大學化學系名譽教授
基因剪刀:一個改寫生命密碼的工具
艾曼紐爾.夏本提爾(Emmanuelle Charpentier)與珍妮佛.道納(Jennifer Doudna)榮獲了 2020 年諾貝爾化學獎的桂冠,主要是因為她們發現了基因技術中最強大的工具之一:CRISPR/Cas9 基因剪刀。研究人員可以非常精準地使用它們改變動物、植物和微生物的 DNA(去氧核糖核酸)。這個技術徹底改變了分子生命科學,為植物育種帶來了新機會、有助於創新的癌症療法、並可能使治癒遺傳性疾病的夢想成真。

科學的吸引力之一是它難以預測——你永遠無法預知一個想法或問題會將你引至何處。有時候好奇的心會遇到死胡同,有時則會遇到棘手的迷宮,需要花費多年的時間在其中探索。但是一次又一次地,她意識到自己是第一個凝視著一個未知的可能性從地平線上升起的人。
這個被稱為 CRISPR/Cas9 而具有驚人潛力的基因編輯器,就是這樣的一個意外發現。當夏本提爾和道納開始研究一個鏈球菌屬細菌的免疫系統時,一個想法是她們可能開發出一種新的抗生素。相反的,她們卻發現了一個分子工具,可用於精準的切割基因物質,使她們可以輕易地改變生命的密碼。
一個影響所有人的強大工具
在這個發現後僅僅八年,這些基因剪刀就重塑了生命科學。生物化學家與細胞生物學家現在可以輕易地研究不同基因的功能,以及它們在疾病進展中的可能角色。在植物育種中,研究人員可以賦予植物特定的性質,例如在溫暖的氣候下具有抗旱能力。在醫學上,這個基因編輯器正在為癌症提供新的療法,以及運用在企圖治癒遺傳性疾病的首批研究中。
實在有太多的例子是關於 CRISPR/Cas9 如何的使用,其中還包括不道德的應用方法。與所有強大的技術一樣,這些基因剪刀需要被管控,有關這部分,後文會有更多說明。
在 2011 年波多黎各的一家咖啡館裡,夏本提爾和道納都不知道她們的第一次會面,將是一次改變人生的相遇。我們將首先介紹夏本提爾,她是最初建議雙方合作的人。
夏本提爾著迷於病原菌
有人曾稱讚夏本提爾的積極、專心和慎密,另有些人說她總是在尋找意外的發現。她自己喜歡引用路易.巴斯德(Louis Pasteur)的名言:「機會總是善待那些有準備的心靈」。追求新發現以及對自由和獨立的渴望,支配著她走的道路。包括在巴黎巴斯德研究所攻讀博士學位在內,她曾待過五個不同的國家,七個不同的城市,以及在十個不同的機構工作。
她的研究環境和方法雖發生了變化,但是她的大部分研究都有一個共同分母:病原菌(pathogenic bacteria)。它們的侵略性為什麼那麼高?它們如何發展出抵擋抗生素的能力?是否可以找到能阻止其進展的新療法?
2002 年,夏本提爾在維也納大學成立自己的研究小組時,她專注於對人類造成危害最大的細菌之一:釀膿鏈球菌(Streptococcus pyogenes)。它每年感染數以百萬的人,經常引起易於治療的感染,例如扁桃腺炎(tonsillitis)和膿皰症(impetigo),但是它也可能導致危及生命的敗血症,並破壞身體的軟組織,而得到「食肉者」的稱號。
為了更進一步地了解釀膿鏈球菌,夏本提爾首先徹底研究了這種細菌如何調控其基因,這決定是發現基因剪刀的第一步——但是在我們進一步跟隨她走上這條路之前,我們將先了解更多有關道納的資訊,因為在夏本提爾對釀膿鏈球菌進行詳細研究的當兒,道納第一次知曉了一個縮寫,她認為其發音聽起來就像是英文的 crisper。

科學——如偵探故事一般的探險
即便是一個在夏威夷長大的孩子,道納也強烈渴望了解各種事物。一天,她的父親把詹姆斯.華生(James Watson)寫的書《雙螺旋》放在她的床上。這是個具有偵探風格的故事,描述了華生和弗朗西斯.克里克(Francis Crick)如何解開了 DNA 分子的結構。那是個與她在學校教科書中所讀過完全不同的故事,她被其中的科學過程所擄獲,體會到科學不僅僅是一堆事實而已。
但是當她真正開始解決科學謎團時,她的注意力並非放在 DNA 上,而是它的同胞分子:RNA(核糖核酸)。當我們在 2006 年看著她時,她正在加州大學伯克萊分校領導著一個研究小組,已經擁有了 20 年的 RNA 研究經驗,具有開發突破性研究的靈敏嗅覺,並獲得非常成功的研究聲譽,最近剛進入了一個令人興奮的新領域:RNA 干擾(RNA interference)。
多年來研究人員一直認為他們了解 RNA 的基本功能,但他們突然發現許多小型 RNA(small RNA)參與了細胞中的基因活性調節。道納參與的 RNA 干擾研究,導致她在 2006 年接到一通來自不同部門的一位同事的電話。
攜帶古老免疫系統的細菌
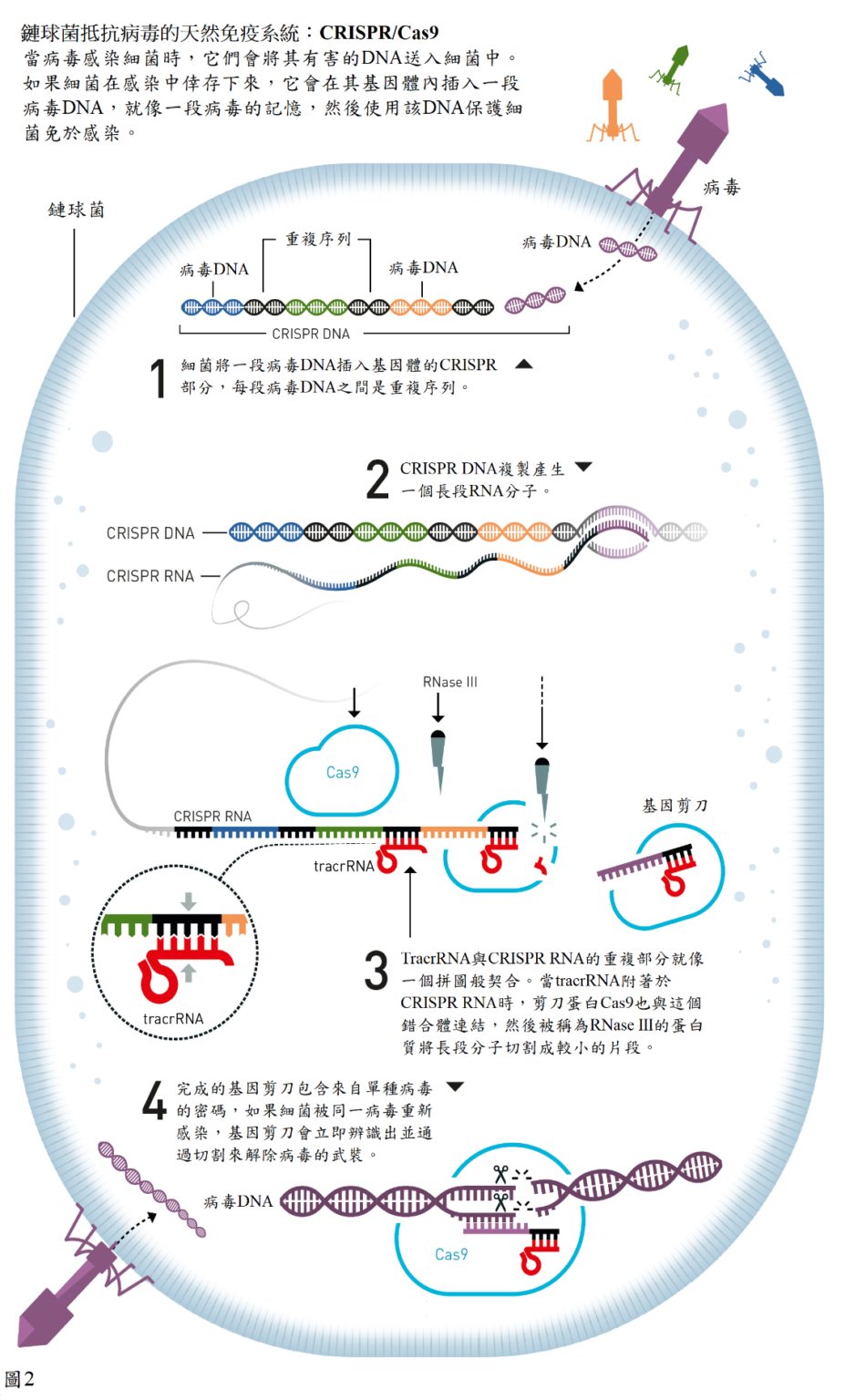
她的同事是微生物學家,告訴了道納一個新發現:研究人員比較各種極為不同的細菌以及古細菌(一種微生物)的基因物質時,出人意料地,他們發現保存完好的 DNA 重複序列,相同的密碼一再重複出現,但是在重複段落之間有著一組獨特的不同序列(圖 2),就像一本書中各個獨特的句子之間,重複著相同的單字。
這些重複序列的陣列稱為「群聚且有規律間隔的短回文重複序列」,縮寫為 CRISPR。有趣的是,CRISPR 中獨特的非重複序列似乎與各種病毒的基因密碼匹配,所以目前的想法為:這是古老的免疫系統的一部分,可以保護細菌和古細菌免受病毒侵害。其假說為如果細菌受到病毒感染而成功地存活,它就會將一部分病毒基因密碼加入其基因體(genome),作為對感染的記憶。
她的同事說,還沒有人知道這一切是如何運作的,但懷疑這種細菌用來中和病毒的機制,類似於道納研究的課題:RNA 干擾。
道納繪出了一個複雜的機器
這個消息極不尋常但更令人振奮,如果細菌確實具有一個古老的免疫系統,那麼這極為重要。道納有著一種栩栩如生的分子計謀感覺,她開始學習有關 CRISPR 系統的所有知識。
研究人員證明除了 CRISPR 序列外,還發現了一些特殊基因,他們將其稱為 CRISPR-關聯者(CRISPR-associated),簡稱為 Cas。有趣的是,道納發現這些基因的編碼,與已知專門用於鬆解和切割 DNA 的蛋白質之基因非常相似。那麼 Cas 蛋白質具有相同的功能嗎?它們會切割病毒 DNA 嗎?
她讓她的研究小組開始工作,幾年後,她們成功地揭示了幾種不同 Cas 蛋白質的功能。同時,少數幾個其它大學的研究小組,也正在研究新發現的 CRISPR/Cas 系統。他們所繪出的圖像顯示細菌的免疫系統可以採取非常不同的形式,道納所研究的 CRISPR/Cas 系統屬於第 1 類;那是一個複雜的機器,需要許多不同的 Cas 蛋白質來清除病毒。第 2 類系統相當簡單,因為它們需要較少的蛋白質。在世界的另一端,夏本提爾剛剛遇到了這樣的系統,現在就讓我們的故事回到她身邊。
CRISPR 系統中一片新而未知的拼圖塊
當我們的故事離開夏本提爾時,她正住在維也納,但在 2009 年,她獲得了很好的研究機會而搬到了在瑞典北部的於默奧大學(Umeå University)。有人警告她要搬到世界上如此偏遠的地區不是個好決定,但是漫長而黑暗的冬天使她工作時充滿了平和與寧靜。
這正是她需要的。她正好也對調控基因的小型 RNA 感興趣,並與在柏林的研究人員合作,詳細研究了釀膿鏈球菌中發現的一些小型 RNA。研究的結果讓她花了許多時間思考,因為該細菌中一種大量存在的小型 RNA 是一個新的變種,該 RNA 的基因密碼與該細菌基因體中奇特的 CRISPR 序列非常類似。
兩者之間的相似性讓夏本提爾懷疑它們是有關聯的,仔細分析它們的基因密碼還顯示,未知的小型 RNA 的一部分與重複的 CRISPR 相互匹配,就像找到兩塊完全密合的拼圖塊一樣(圖 2)。
夏本提爾從未研究過 CRISPR,但她的研究小組為了釐清釀膿鏈球菌中的 CRISPR 系統,啟動了一些徹底的微生物學偵探工作。這個系統屬於已知的第 2 類,僅需一個 Cas 蛋白質:Cas9,即可裂解病毒 DNA。夏本提爾發現,被稱為謄本活化 crispr RNA(tracrRNA)的新 RNA 分子,也具有決定性功能;基因體中的 CRISPR 序列所製造出來的長段 RNA,需要 tracrRNA 讓它成熟為活性形式(圖 2)。
經過深入而有目標性的實驗,夏本提爾於 2011 年 3 月發表了 tracrRNA 的發現,她知道自己正尾隨著某個精采的東西。她有多年的微生物學經驗,但為了持續研究 CRISPR/Cas9 的系統,她希望能與生物化學家合作,道納則是當然的選擇。因此在當年春天,夏本提爾受邀參加在波多黎各舉行的會議報告她的發現時,她企圖結識這位非常有經驗的伯克萊研究人員。
波多黎各咖啡館中改變人生的會面
碰巧的是,她們在會議的第二天在一家咖啡館見了面,道納的同事介紹了她們認識。第二天,夏本提爾提議她們應該一起探索這個首都的舊城區。當她們沿著鵝卵石鋪就的街道漫步時,開始談到彼此的研究,夏本提爾想知道道納是否對合作感興趣?她有意參與釀膿鏈球菌簡單的第 2 類系統中,Cas9 功能的研究嗎?
道納很感興趣,她們和同事們通過線上會議擬定了該研究的計劃。她們懷疑 CRISPR RNA 是辨識病毒 DNA 所必需的,而 Cas9 是切斷 DNA 分子的剪刀。但是當她們在生物體外進行測試時,什麼都沒有發生,DNA 分子仍保持完整。為什麼?實驗條件有問題嗎?還是說 Cas9 具有完全不同的功能?
經過大量的腦力激盪和無數失敗的實驗之後,她們的研究人員終於添加了 tracrRNA 進行測試,原先他們認為僅在 CRISPR RNA 被切割成活性形式後,才需要 tracrRNA(圖 2),但是一旦 Cas9 可以使用 tracrRNA,大家一直期待的事情真的發生了:DNA 分子被切割成兩部分。
大自然透過進化解決問題的方法經常使研究人員感到驚訝,但這次卻是非同尋常的,鏈球菌所發展出的抵禦病毒武器,既簡單又有效,甚至可謂傑出。基因剪刀的歷史可能就此結束:夏本提爾和道納曾經在一種對人類造成巨大苦難的細菌中,發現了一種細菌的基本機制。光是這發現就已令人驚奇,但機會總是善待那些有準備的心靈。
劃時代的實驗
研究小組人員決定嘗試簡化基因剪刀,利用對 tracrRNA 和 CRISPR RNA 的新知識,他們設計出方法將兩者融合成一個分子,命名為「嚮導 RNA」(guide RNA)。利用這種簡化的基因剪刀變體,他們接著開始進行劃時代的實驗:研究是否可以控制這種基因工具,從而於研究人員指定的位置切割 DNA。
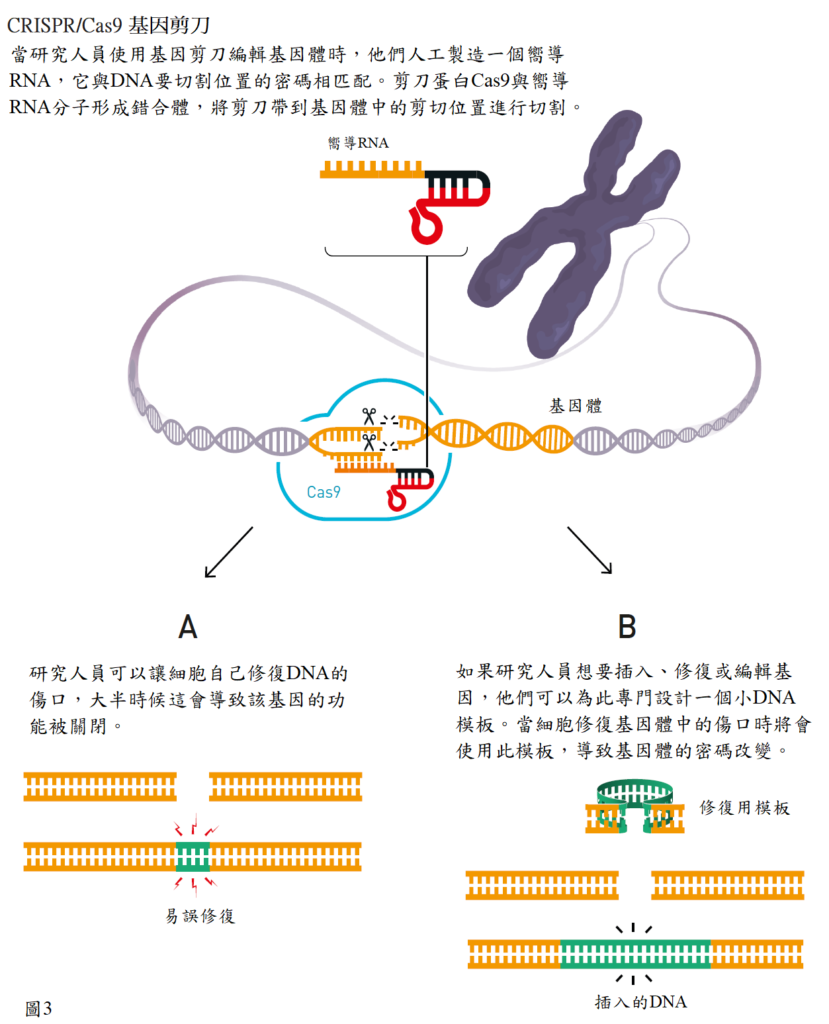
此時研究人員知道已經接近了重大突破,他們使用一個已經在道納實驗室的冰櫃中存放的基因,並選擇了五個不同的基因切割位置,然後更改剪刀的 CRISPR 部分,使其密碼與進行切割位置的密碼匹配(圖 3),結果是勢不可擋的將 DNA 分子切割在正確的位置。
基因剪刀改變了生命科學
夏本提爾和道納在 2012 年發表 CRISPR/Cas9 基因剪刀的發現後不久,這個工具被多個研究小組展示可用於修飾小鼠和人類細胞中的基因體,導致爆炸性的發展。先前,改變細胞、植物或生物體中的基因非常耗時,有時甚至是不可能的。使用這種基因剪刀,研究人員原則上可以在他們想用的任何基因體中進行切割。接著可以很容易利用細胞的天然 DNA 修復系統,從而改寫生命密碼(圖 3)。
由於這種基因工具非常易於使用,現在廣泛的應用於基礎研究中。它可用於更改細胞和實驗動物的 DNA,以了解不同基因的功能和相互的作用,例如在疾病過程中的角色。
基因剪刀也已成為植物育種的標準工具,以前研究人員修改植物基因體使用的方法,通常需要添加抗生素耐藥性基因,但種植這種農作物時,其抗生素耐藥性可能會擴散給周圍微生物。多虧了基因剪刀,研究人員不再需要使用這些較舊的方法,因為他們現在可以對基因體進行非常精確的更改。許多其它應用中,他們還編輯了使水稻吸收土壤中重金屬的基因,使得改良的水稻品種具有較低的鎘和砷的含量。研究人員還開發了在溫暖的氣候中更能抵抗乾旱的農作物,並且可以抵抗昆蟲和害蟲,否則將不得不使用農藥。
遺傳疾病治癒的希望
在醫學上,基因剪刀為癌症的新免疫療法做出了貢獻,實驗正在企圖讓夢想實現——治癒遺傳疾病。研究人員已經在進行臨床試驗以研究是否可以使用 CRISPR/Cas9 來治療一些血液疾病,例如鐮形血球貧血症和 beta-地中海型貧血症,以及遺傳性眼疾。
他們也在開發修復大型器官中基因的方法,例如大腦和肌肉。動物實驗顯示,經過特殊設計的病毒可以將基因剪刀導入需要的細胞,作為治療毀滅性遺傳疾病的模型,例如肌肉失養症,脊髓肌肉萎縮和杭丁頓舞蹈症。但是該技術仍需要進一步改善,使之能在人體上進行測試。
基因剪刀的能力需要監控
與其所有優點並存的,基因剪刀也可能被濫用。例如,可以使用此工具創造基因修飾過的胚胎。但是,多年來有法律及法規控制基因工程的應用,其中包括禁止會讓變化遺傳給後代的人類基因體修改方式。另外,涉及人類和動物的實驗,必須經過道德委員會的審查和批准才得執行。
可以肯定的是:這些基因剪刀影響著我們所有人。我們將面臨新的倫理問題,但是此一新的工具很可能有助於解決當今人類面臨的許多挑戰。通過她們的發現,夏本提爾和道納開發了一種化學工具,將生命科學帶入了一個新時代。她們使我們注視著無法想像的廣闊前景,並且,在我們探索這片新領域的過程中,一定會創造出新的和意想不到的發現。



































《運動基因》立體封面72dpi.jpg)




