病毒的一生中,擁有一些特殊、特有的蛋白質。那些就是研發藥物攻擊的目標
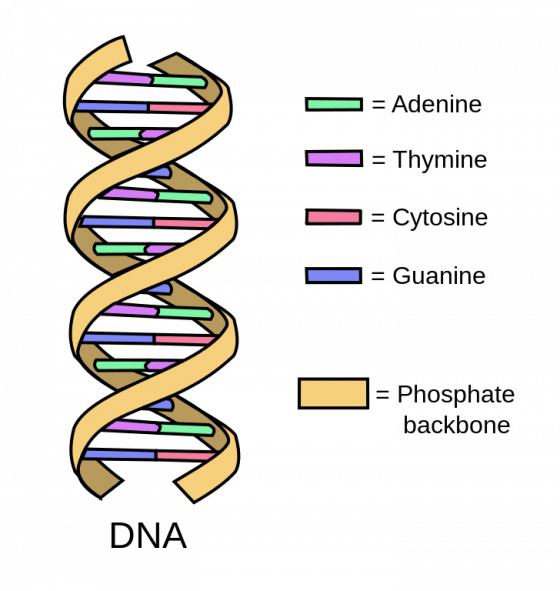
只要是生物都要複製基因,才能誕生下一代。基因由 DNA 或 RNA 組成,小單元即為為核苷酸。因此,結構類似核苷酸、但能阻礙複製的仿核苷酸藥物,就成了醫療上常見的抗病毒用藥。
瑞德西韋未能擊敗伊波拉,與之後的華麗轉身
2014年,西非爆發大規模伊波拉出血熱(Ebola Hemorrhagic Fever)。伊波拉出血熱的病原體是伊波拉病毒(Ebola virus),屬RNA絲狀病毒,所引起的疾病致死率最高達 90%。伊波拉大流行引起科學界高度警戒,也讓新藥研發光速起飛。瑞德西韋也在此時,投入競賽,正式進入臨床試驗、一見真章。
在陸續通過細胞、動物實驗的考驗後,瑞德西韋於 2018 年投入西非戰場1。可惜的是,隔年的臨床試驗初步結果揭示,另兩款的抗體藥物 REGN-EB3、mAb114 的患者,存活率比施打瑞德西韋的患者高。2019 年 8 月,宣布終止使用瑞德西韋、塵封於抽屜。
2020 年,新型冠狀病毒(SARS-CoV-2)全球大爆發。因過往的實驗裡,瑞德西韋曾表現出抑制 2003 年 SARS 病毒的能力,便匆匆地被拉出倉庫、重新登板先發。
- 01/31,新英格蘭期刊報告美國第一例新型冠狀病毒疾病(COVID-19)患者被瑞德西韋治癒2。
- 05/01,基於大型臨床試驗的中期報告,美國食品藥物管理署 (FDA, U.S. Food and Drug Administration) 受予緊急治療。瑞德西韋華麗轉身,成為眾所矚目的新救命藥。
三種仿核苷酸藥物對抗病毒的原理
仿核苷酸藥物干擾遺傳物質複製的原理有三種,分別是3:
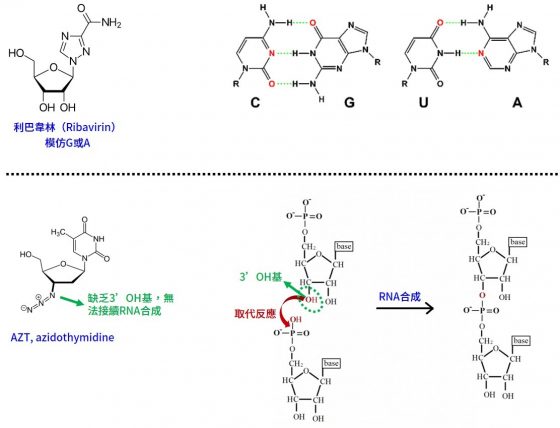
- 誘發突變,如:利巴韋林(Ribavirin)
- 立即終止複製,如:AZT(azidothymidine)
- 延遲終止複製,如:瑞德西韋(remdesivir)
病毒誤用利巴韋林後,將引起錯誤複製、致命突變。研究發現,利巴韋林提高小兒麻痺病毒 9.7 倍的突變、導致產出大量無效的子代病毒,進而降低 99.3% 的病毒活性3。
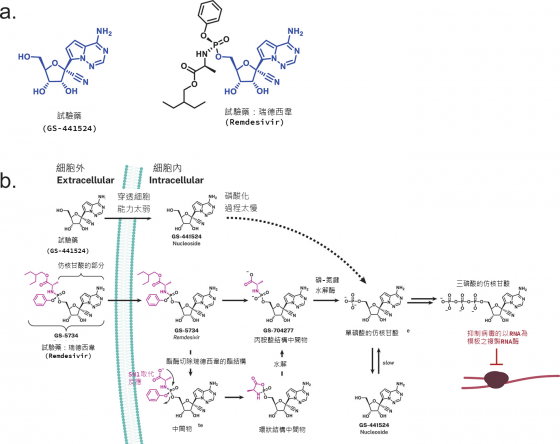
而第二種原理,是直接強行終止複製。因為 RNA 或 DNA 複製的過程中,需透過醣基的 3’-OH 基,進行取代作用連接下一個鹼基(如下圖);而 AZT 因為沒有醣基的 3’-OH 基,故無法接續下一個鹼基。因此若病毒誤用了 AZT,在缺乏醣基 3’-OH 基情況下,複製只能被強行終止。
而瑞德西韋等化合物,屬於第三種原理。是利用藥物的立體障礙,意即化合物擁有的特殊結構、官能基等,讓酵素在複製過程中,內部出現空間阻礙,進而停止酵素作用3,4。
卡住酵素的齒輪:瑞德西韋抑制病毒活性的原理
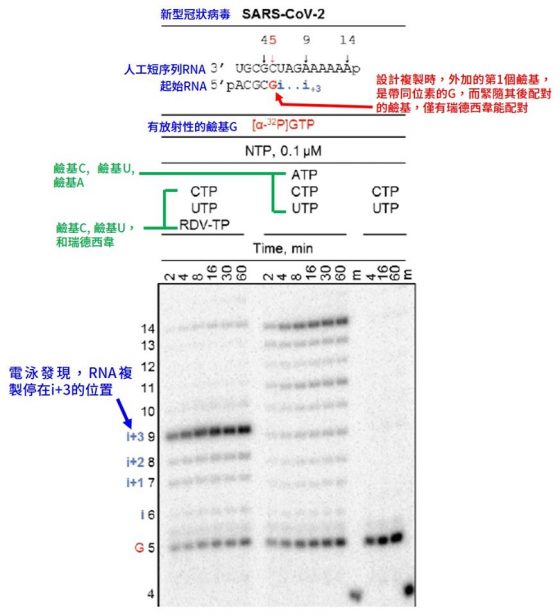
為了理解瑞德西韋殺死病毒的原理,科學家人工編織了短序列的 RNA 鏈和起始片段,並加入了 RNA 依賴性 RNA 聚合酶(RNA-dependent RNA polymerase, RdRp)、正常 RNA 鹼基,以及瑞德西韋5。結果發現,複製的 RNA 鏈,停留在 i+3 的位置 (如下圖)5。換言之,當瑞德西韋被聚合酶誤用後,RNA 鏈會在瑞德西韋之後算起,第 3 個鹼基時停止複製(伊波拉病毒的RdRp,停在 i+5 的位置6)。
依據電腦建模運算,認為瑞德西韋醣基上碳1的 CN 鍵,和 RNA 依賴性 RNA 聚合酶產生了空間衝突,阻礙了酵素的正常功能,導致 RNA 的複製在i+3的位置停止3,7,8。
多方合擊:對抗新型冠狀病毒的藥物們
為什麼瑞德西韋可以抑制多種 RNA 病毒呢?新型冠狀病毒的生活週期裡,有著許多病毒特有的酵素、蛋白質參與。例如 RNA依賴性RNA聚合酶(RdRp),是病毒獨有的酵素,人類細胞通常缺乏此酵素,因此可作為藥物的重點攻擊目標。
RNA 依賴性 RNA 聚合酶利用病毒的 RNA 為模版,複製成千上萬的子代病毒 RNA。而幾乎所有 RNA 病毒,都必須使用RNA 依賴性 RNA 聚合酶(RdRp)來複製子代基因。瑞德西韋即是讓此酵素失效,殺死多種 RNA 病毒、成為廣譜型的抗病毒藥物。
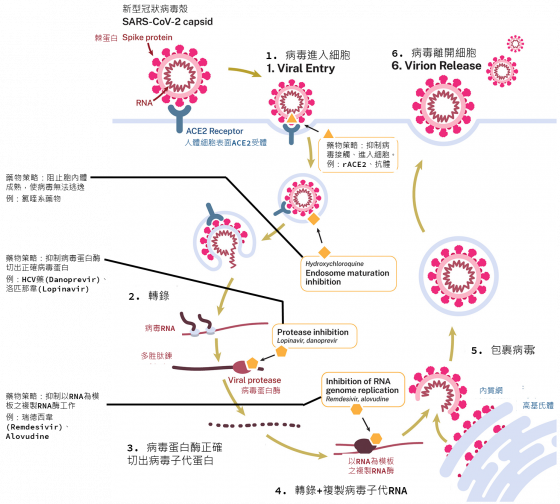
除了瑞德西韋外,多種藥物也嘗試打擊新型冠狀病毒。如:改變包內體(endosome)酸鹼條件,使病毒無法逃出胞器的羥氯喹(hydroxychloroquine)。辨認病毒表面蛋白質,使病毒難以結合細胞受器的、阻止侵入細胞的抗體藥物。
回頭看瑞德西韋的研發、失敗而塵封,如今卻躍然成為人類的希望,筆者認為要感謝二十多年前科學家的遠見,和繼任者的堅持,我們現在才有瑞德西韋,能在這場大瘟疫裡掙得更多的生機。
保持冷靜,繼續前進。Keep Calm and Carry On.
參考文獻
- 伊波拉不再是不治之症?兩種抗體藥物取得一線曙光。2019/08/19。泛科學。蔣維倫
- 伊波拉的藥物Remdesivir,可以用以對抗新型冠狀病毒肺炎(COVID-19)?由美國第一例治療報告談起。2020/02/14。泛科學。蔣維倫
- Richard T. Eastman, Richard T. Eastman, Jacob S. Roth, Kyle R. Brimacombe, Anton Simeonov, Min Shen, Samarjit Patnaik, Matthew D. Hall (2020) Remdesivir: A Review of Its Discovery and Development Leading to Emergency Use Authorization for Treatment of COVID-19. ACS Central Science. https://doi.org/10.1021/acscentsci.0c00489
- Ashleigh Shannon, Nhung Thi Tuyet Le, Barbara Selisko, Cecilia Eydoux, Karine Alvarez, Jean-Claude Guillemot, Etienne Decroly, Olve Peersen, Francois Ferron, and Bruno Canard (2020) Remdesivir and SARS-CoV-2: structural requirements at both nsp12 RdRp and nsp14 Exonuclease active-sites.. Antiviral Research. DOI: 10.1016/j.antiviral.2020.104793
- Calvin J Gordon, Egor P Tchesnokov, Emma Woolner, Jason K Perry, Joy Y. Feng, Danielle P Porter and Matthias Gotte (2020) Remdesivir is a direct-acting antiviral that inhibits RNA-dependent RNA polymerase from severe acute respiratory syndrome coronavirus 2 with high potency. Journal of Biological Chemistry. DOI: 10.1074/jbc.RA120.013679
- Calvin J. Gordon, Egor P. Tchesnokov, Joy Y. Feng, Danielle P. Porter, Matthias Götte (2020) The antiviral compound remdesivir potently inhibits RNA-dependent RNA polymerase from Middle East respiratory syndrome coronavirus. Journal of Biological Chemistry. DOI: 10.1074/jbc.AC120.013056
- Dustin Siegel, Hon C. Hui, Edward Doerffler, Michael O. Clarke, Kwon Chun, Lijun Zhang, Sean Neville, Ernest Carra, Willard Lew, Bruce Ross, Queenie Wang, Lydia Wolfe, Robert Jordan, Veronica Soloveva, John Knox, Jason Perry, Michel Perron, Kirsten M. Stray, Ona Barauskas, Joy Y. Feng, Yili Xu, Gary Lee, Arnold L. Rheingold, Adrian S. Ray, Roy Bannister, Robert Strickley, Swami Swaminathan, William A. Lee, Sina Bavari, Tomas Cihlar, Michael K. Lo, Travis K. Warren, Richard L. Mackman (2017) Discovery and Synthesis of a Phosphoramidate Prodrug of a Pyrrolo[2,1-f][triazin-4-amino] Adenine C-Nucleoside (GS-5734) for the Treatment of Ebola and Emerging Viruses. Journal of Medicinal Chemistry. https://doi.org/10.1021/acs.jmedchem.6b01594
- Wanchao Yin, Chunyou Mao, Xiaodong Luan, Dan-Dan Shen, Qingya Shen, Haixia Su, Xiaoxi Wang, Fulai Zhou, Wenfeng Zhao, Minqi Gao, Shenghai Chang, Yuan-Chao Xie, Guanghui Tian, He-Wei Jiang, Sheng-Ce Tao, Jingshan Shen, Yi Jiang, Hualiang Jiang, Yechun Xu, Shuyang Zhang, Yan Zhang, H. Eric Xu (2020) Structural basis for inhibition of the RNA-dependent RNA polymerase from SARS-CoV-2 by remdesivir. Science. DOI: 10.1126/science.abc1560