2020/05/01,美國授權瑞德西韋(Remdesivir)緊急治療新型冠狀病毒疾病(COVID-19)重症患者,吉利德科學(Gilead Sciences, Inc.)股價也應聲大漲。然而,瑞德西韋並非一帆風順,它也歷經失敗、塵封於抽屜,因緣際會才重新站回投手丘。本篇將講述瑞德西韋的崛起、失敗,與華麗轉身。
科學家的妄想:對抗RNA病毒的萬能藥
數十年來,RNA 病毒對人類的威脅越來越大,如:2009 年的 H1N1 流感病毒、2012 年的中東呼吸症候群冠狀病毒(Middle East respiratory syndrome coronavirus, MERS)。
著眼於此,上個世紀末期,美國疾病與控制中心(Centers for Disease Control and Prevention , CDC)、美國陸軍傳染病醫學研究所(United States Army Medical Research Institute of Infectious Diseases, USAMRIID)、吉利德科學這些單位透過三方合作,試圖找到一種能廣泛抑制多種 RNA 病毒的藥物。
換言之,科學家希望有種萬能藥,能對抗現在和未來所有的 RNA 病毒1,2。數十年的研究,累積了約一千種仿核苷酸藥物的各種生化資料。
瑞德西韋的研發可追溯到天然的仿核苷酸藥物 Tubercidin(抗結核菌素)。它是來自放射線菌(細菌,該門產生多樣化的抗生素)分泌的天然毒物3,結構類似 RNA 或 DNA 的腺嘌呤(Adenine,代號A),能讓其他微生物在複製 DNA 或 RNA 時,不小心誤用 Tubercidin,導致死亡。
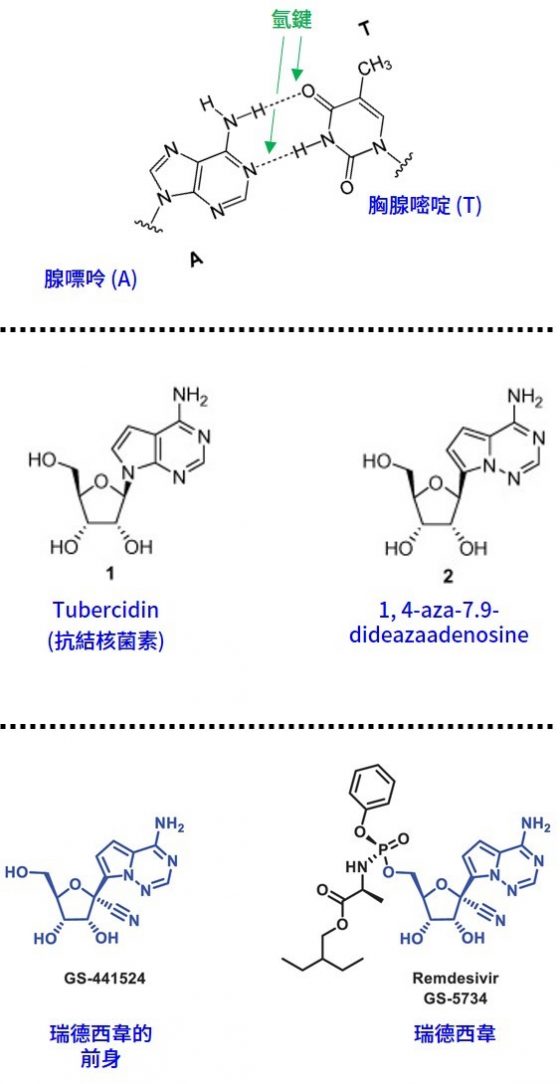
科學家模仿 Tubercidin,創造了 1, 4-aza-7.9-dideazaadenosine,發現也有類似的毒殺功能。而吉利德的科學家以大自然為師,合成了一系列的化合物,並開始測試這些化合物的潛力。
嚴苛的篩選:誰是最好的抗病毒萬能藥?
科學家修飾 1, 4-aza-7.9-dideazaadenosine 醣基上的碳1,讓該位置有四種不同的官能基,其後再測試此四類化合物對病毒的抑制效果3。
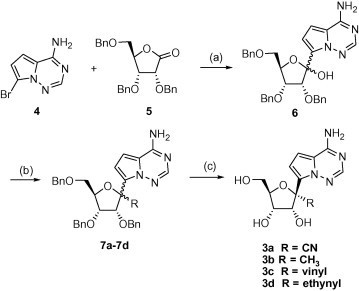
如下表,在抑制多種病毒裡,上圖的 3a 化合物有最廣泛的抗病毒能力,除了西尼羅河病毒、克沙奇A型病毒外,針對其他病毒都有一定的抑制效果(遠低於半數細胞毒性的濃度時,就能抑制半數病毒)。3b化合物也有廣譜抑制效果,但不如3a。3c化合物僅能抑制2003年的冠狀病毒、3d化合物沒有觀察到抗病毒效果3。
仿核苷酸化合物 1, 4-aza-7.9-dideazaadenosine 的各種版本及對病毒的有效濃度
| EC50/CC50 (μM) | ||||
| 3a | 3b | 3c | 3d | |
| C型肝炎病毒 | 4.1/>89 | 39/>45 | >89/>89 | >89/>89 |
| 黃熱病毒 | 11/>30 | ND | ND | ND |
| 登革熱2型病毒 | 9.46/>30 | >30/>30 | >30/>30 | >30/>30 |
| 西尼羅河病毒 | >30/>30 | >30/>30 | >30/>30 | >30/>30 |
| A型流感病毒 | 27.9/>30 | >30/>30 | >30/>30 | >30/>30 |
| 副流感病毒 | 1.71/>30 | 5.23/>30 | >30/>30 | >30/>30 |
| SARS-CoV-1 | 2.24/>30 | >30/>30 | 14.0/>30 | >30/>30 |
| 克沙奇A型病毒/腸病毒 | >30/>30 | >30/>30 | >30/>30 | >30/>30 |
- EC50:半數病毒抑制濃度;CC50:半數細胞毒性濃度
因為 3a-3d 化合物的單磷酸官能基上,帶有高度電荷性,因此難以穿透疏水性的細胞膜。因此科學家將兩個支鏈修飾於單磷酸上,形成疏水性較高的9a-9d化合物,再檢測此系列的毒性、抗病毒性、細胞膜內的累積能力。
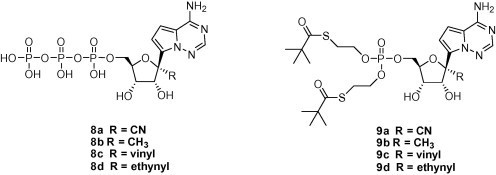
如下表,以抗病毒能力而言,可發現 9a、9b 化合物的效果最好、有療效的濃度最低。但以安全性而言,9b 化合物則比 9a危險,殺死半數細胞的濃度(CC50),還不到半數抑制病毒濃度(EC50)的十倍,在臨床應用上困難。藥物的安全濃度太窄,可能在殺死病毒的過程中,也將細胞殺死。以細胞內可累積濃度而言,也以 9a 化合物為最佳,此結構的細胞滲透度最高 3。
| EC50/CC50( μM ) | 細胞內累積濃度 ( pmol/million ) | |
| 9a | 0.085/3.2 | 4,220 |
| 9b | 0.078/0.73 | ND |
| 9c | 3.43/12 | 440 |
| 9d | 6.01/26 | 150 |
吉利德的科學家於 2012 年發表了這些成果。然而,誰也沒想到兩年後,突如其來的瘟疫,瑞德西韋就此拉上投手丘,接受真實世界的考驗了。
後續請見 瑞德西韋發展與原理(下):模仿「核苷酸」阻止遺傳物質的複製!
參考文獻
- Richard T. Eastman, Richard T. Eastman, Jacob S. Roth, Kyle R. Brimacombe, Anton Simeonov, Min Shen, Samarjit Patnaik, Matthew D. Hall (2020) Remdesivir: A Review of Its Discovery and Development Leading to Emergency Use Authorization for Treatment of COVID-19ACS Central Science. https://doi.org/10.1021/acscentsci.0c00489
- Dustin Siegel, Hon C. Hui, Edward Doerffler, Michael O. Clarke, Kwon Chun, Lijun Zhang, Sean Neville, Ernest Carra, Willard Lew, Bruce Ross, Queenie Wang, Lydia Wolfe, Robert Jordan, Veronica Soloveva, John Knox, Jason Perry, Michel Perron, Kirsten M. Stray, Ona Barauskas, Joy Y. Feng, Yili Xu, Gary Lee, Arnold L. Rheingold, Adrian S. Ray, Roy Bannister, Robert Strickley, Swami Swaminathan, William A. Lee, Sina Bavari, Tomas Cihlar, Michael K. Lo, Travis K. Warren, Richard L. Mackman (2017)Discovery and Synthesis of a Phosphoramidate Prodrug of a Pyrrolo[2,1-f][triazin-4-amino] Adenine C-Nucleoside (GS-5734) for the Treatment of Ebola and Emerging Viruses Journal of Medicinal Chemistry. https://doi.org/10.1021/acs.jmedchem.6b01594
- Aesop Cho, Oliver L. Saunders, Thomas Butler, Lijun Zhang, Jie Xu, Jennifer E. Vela, Joy Y. Feng, Adrian S. Ray, Choung U. Kim (2012) Synthesis and antiviral activity of a series of 1′-substituted 4-aza-7,9-dideazaadenosine C-nucleosides. Bioorganic & Medicinal Chemistry Letters. https://doi.org/10.1016/j.bmcl.2012.02.105