- 作者/白映俞醫師
- 本文轉載自 Care Online 照護線上《值得注意的癌症症狀(懶人包)》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔!

魔鬼藏在細節中,癌症預兆也藏在小症狀中
每次到醫院就診時,醫師是否都會問一句:「你覺得哪裡不舒服嗎?」不管是自己主觀感覺到無力、疼痛,或身旁的人說自己看起來很喘,該去看診檢查一下,這些「症狀和徵象」對醫師來說都是很有參考價值的。
如果只有一個症狀,或許難以馬上找到病因,或讓人了解疾病的全貌;但隨著患者提到的症狀愈多,醫師就能像掌握愈多線索的柯南一般,找出疾病兇手。
現代人壽命愈來愈長,但罹癌人數也不斷攀升,因此不少人會想知道:「我有沒有辦法早一點知道自己是否罹患癌症呢?」對於一些常見的癌症,像是乳癌,我們就會建議要定期做篩檢。
定期篩檢的意思就是你即使沒有症狀,符合一定年齡或一定的條件就建議要定期做檢查。但多數癌症發生率沒那麼高,目前沒有推薦的定期篩檢方式,那我們該怎麼注意自己的健康狀況呢?
要注意自己的身體發出來的訊號!
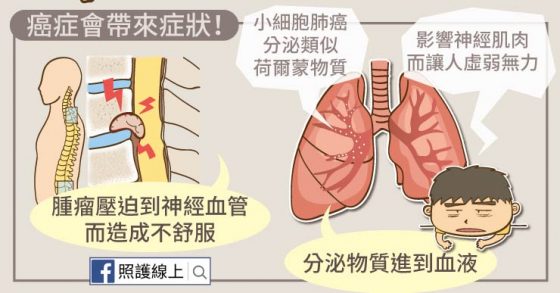
生長中的癌症會壓迫到周遭的器官、血管、神經,也可以分泌物質進到血流中,這些都會帶來一些身體的警訊。像是長在腦內的腫瘤,即使腫瘤很小只有一公分上下,也可能因為長的位置很重要而帶來症狀,例如長在腦下垂體的腫瘤可能會壓迫到視神經交叉而導致視野改變。這時,「視野改變」就是身體發出的警訊。
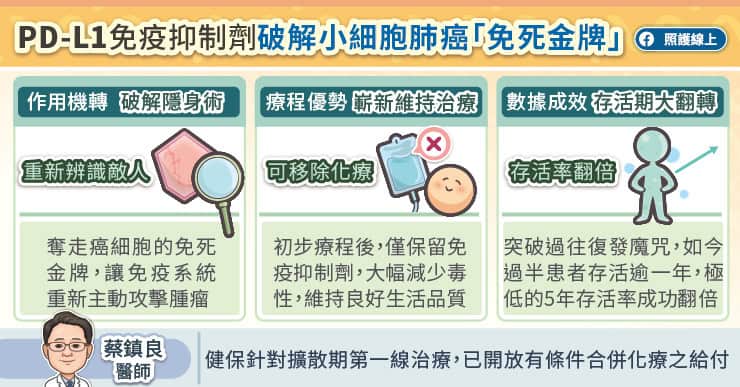
肺癌中容易快速侵襲的「小細胞癌」則會分泌類似荷爾蒙的物質,進入血流,升高血液中的鈣離子濃度,影響神經、肌肉的運作,讓患者覺得虛弱無力。這時,「虛弱無力」就是身體發出的警訊。
假如我們忽略了這些徵兆症狀,就會讓癌症威脅潛伏更久,身體逐步被黑暗勢力控制。但如果能藉由認識症狀、徵兆而及早找出問題,就像是身體的黎明升起,能提高治癒癌症的希望。
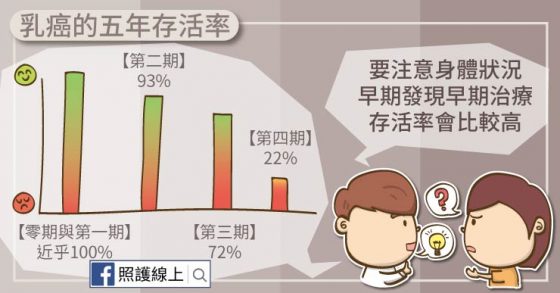
談到癌症的存活率,我們常會講「一年存活率」、「五年存活率」、「十年存活率」來說。例如講五年存活率的時候,就是指被診斷為某種癌症之後,能存活超過五年以上的患者比率。
而罹患同一樣癌症的患者們,在不同分期的狀況下,結果就不太一樣。
拿女性最好發的癌症—乳癌來說的話,乳癌零期與乳癌第一期患者的五年存活率近乎是 100%,也就是如果患者是在乳癌零期、乳癌第一期時就知道自己罹患乳癌,並接受治療,幾乎所有的患者都能存活五年以上。但是,如果是乳癌第四期的患者,五年的存活率就降到了 22%,也就是大約四個乳癌四期的患者中,從診斷後僅有一位能存活到五年。
看到這裡,大家應該就愈能夠清楚知道,欲了解自己身體表現出的徵兆症狀,早一點就醫檢查治療,愈能夠早一點知道自己是否罹患癌症,並接受治療。
不過,癌症引起的症狀可以是很常見的問題,像是發燒、疼痛,大家偶爾都會發燒、或這裡痛那裡痛,難道都要擔心自己是癌症嗎?不,我們不是希望大家變成驚弓之鳥,所以請要了解,以下我們提到的症狀,都不是只有癌症會引發這些症狀,所以一有症狀的時候,先不要緊張,但只要症狀持續時間很久,或症狀愈來愈嚴重,就要記得就醫檢查。
接下來,我們就來看看一些值得注意的癌症症狀吧!
癌症症狀報你知!有這些狀況可要注意啦!
 無法解釋的體重下降
無法解釋的體重下降
如果常看照護線上的朋友們應該會知道,我們在講「預防疾病」的時候,常常會提到要注意體重,肥胖是真的會提高罹患多種癌症的機率的。所以平時少吃一點,多作點運動,讓身體精實,絕對是聰明健康的好方式。
然而,當你沒有特別改變吃東西的質與量,也沒有特別多運動,突然間莫名其妙地就瘦了五公斤以上,可不要以為這是天上掉下來的禮物。
無法解釋的體重下降可以是癌症的第一個徵兆,而且可能是胰臟、胃、食道、肺臟等處的癌症的徵兆。
發燒
發燒常常是身體對抗細菌、病毒等感染入侵時的反應,所以我們常把感冒發燒放在一起講。但發燒不一定就只有感冒才會引起。當癌症影響到我們的免疫系統調控,就有可能會引起發燒。
若有白血病(血癌)和淋巴癌,可能在疾病早期會出現發燒症狀。而其他的癌症如果到轉移他處時,也可能造成發燒。所以如果每天發燒不知道原因且超過一星期,就算燒的不高也要記得就醫。
疲憊不堪
看到這句,可能很多人會苦笑說:「我每天都覺得很累!」但癌症造成的疲憊會讓人真的好累好累,即使休息一整天也難以改善。
有些人是白血病的初期,血球功能和數量變化而讓人很累。另外有些人則是因為罹患大腸癌或胃癌,腫瘤處持續出血而不自知。
 排便習慣改變
排便習慣改變
不管是大便或小便的習慣改變都要注意喔。例如長時間便祕、拉肚子、大便的形狀改變,都是大腸癌的徵兆。如果尿尿時會痛,看到血尿,變得頻尿或沒尿,尿尿要愈來愈出力,或尿流變得很細、沒力,就有可能是膀胱癌或攝護腺癌。雖然年紀大的時候,這些尿尿的症狀很有可能是攝護腺肥大引起的,但年紀到了的話,還是要抽血檢查PSA,或由醫師安排肛門指診、經直腸超音波確定是否有癌症。
無法癒合的潰瘍
傷口不算少見,但傷口如果一直不會好,那就不對!皮膚癌可以長得像個潰瘍,剛開始大家也都是當傷口治療,但差別就在於它一直不會好!這就要很小心。
嘴巴裡面如果一直有不會好的潰瘍,且是有抽菸、喝酒、嚼檳榔的人,就要小心口腔癌。若發現陰莖、陰道的潰瘍,也最好讓醫師檢查,不要因為害羞就自行擦藥,雖然這些私密處的潰瘍常常是感染引起的,但有些則是癌症早期的徵兆。
身體各處不正常的出血或分泌物
若看到糞便中有血,可能很多人第一個想法是痔瘡流血,沒錯,但不管是帶鮮血的糞便,黑黑的像瀝青的糞便,還是要注意是否有腸胃道的癌症。另外,陰道異常出血,像是不在經期該在的時間出現的陰道流血,性行為後出血,分泌物帶血,尤其是已經停經後的陰道出血,都最好就醫檢查,排除子宮內膜癌或子宮頸癌的可能。尿中帶血,您可以看看「血尿原因很多種」這篇介紹,但提醒您,腎臟癌及膀胱癌都可能導致血尿。還有,如果擠壓乳頭時發現有帶血的分泌物,也要趕快就醫檢查。
各種皮膚變化
如果皮膚顏色變黃、眼白變黃,這是黃疸,要趕快找出黃疸的原因。另外還要注意痣的變化。像是皮膚上出現新的斑點,或原本的痣改變了形狀、顏色、大小,都可能是皮膚癌的徵兆,請看「你的痣帶財?還是帶癌?」這篇。
- 本文轉載自 Care Online 照護線上《值得注意的癌症症狀(懶人包)》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔!
- 加入照護線上LINE官方帳號,健康資訊不漏接!
https://line.me/R/ti/p/%40careonline

 無法解釋的體重下降
無法解釋的體重下降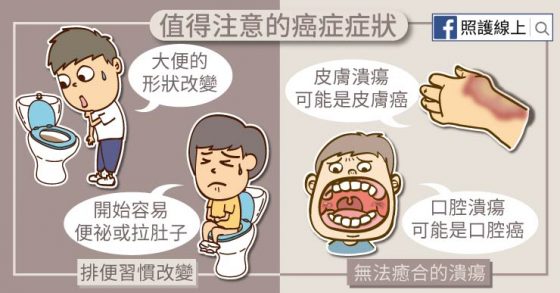 排便習慣改變
排便習慣改變