
賓州州立大學醫學院的研究者發現新的抗癌方法,他們利用奈米技術將C6-ceramide(神經醯胺, 又稱Cerasomes)-一種在細胞質膜中控制細胞老化跟死亡的不溶性脂質分子-變成可溶性。奈米處理過後的Cerasomes可以有效毒死肝癌細胞,使癌細胞組織無法增生血管、獲得養份,但對一般正常細胞沒有影響,也不會有一般抗癌藥物帶給病人的嚴重副作用。
肝癌是世界上第五普遍的癌症,肝癌患者活過5年的機率低於百分之五,通常的療法是化療跟外科手術,包括器官移植。
資料來源:ScienceDaily

賓州州立大學醫學院的研究者發現新的抗癌方法,他們利用奈米技術將C6-ceramide(神經醯胺, 又稱Cerasomes)-一種在細胞質膜中控制細胞老化跟死亡的不溶性脂質分子-變成可溶性。奈米處理過後的Cerasomes可以有效毒死肝癌細胞,使癌細胞組織無法增生血管、獲得養份,但對一般正常細胞沒有影響,也不會有一般抗癌藥物帶給病人的嚴重副作用。
肝癌是世界上第五普遍的癌症,肝癌患者活過5年的機率低於百分之五,通常的療法是化療跟外科手術,包括器官移植。
資料來源:ScienceDaily
本文與 益福生醫 合作,泛科學企劃執行
昨晚,你又在床上翻來覆去、無法入眠了嗎?這或許是現代社會最普遍的深夜共鳴。儘管換了昂貴的乳膠枕、拉上百分之百遮光的窗簾,甚至在腦海中數了幾百隻羊,大腦的那個「睡眠開關」卻彷彿生鏽般卡住。這種渴望休息卻睡不著的過程,讓失眠成了一場耗損身心的極限馬拉松 。
要理解失眠,我們得先認識身體的一套精密防衛系統:下視丘-垂體-腎上腺軸(HPA axis) 。這套系統原本是演化給我們的禮物,讓我們在面對劍齒虎或突如其來的危險時,能迅速進入「戰鬥或快逃」的備戰狀態。當這套系統啟動,腎上腺就會分泌皮質醇 (壓力荷爾蒙),這種荷爾蒙能調動能量、提高警覺性,讓我們在危機中保持清醒 。
然而,現代人的「劍齒虎」不再是野獸,而是無止盡的專案進度、電子郵件與職場競爭。對於長期處於高壓或高強度工作環境的人們來說,身體的警報系統可能處於一種「切換不掉」的狀態。
在理想的狀態下,人類的生理時鐘像是一場精確的接力賽。入夜後,身體會進入「修復模式」,此時壓力荷爾蒙「皮質醇」的濃度應該降至最低點,讓「睡眠荷爾蒙」褪黑激素(Melatonin)接棒主導。褪黑激素不僅負責傳遞「天黑了」的訊號,它還能抑制腦中負責維持清醒的食慾素(Orexin)神經元,幫助大腦順利關閉覺醒開關。

然而,當壓力介入時,這場接力賽就會變成跑不完的馬拉松賽。研究指出,長期的高壓環境會導致 HPA 軸過度活化,使得夜間皮質醇異常分泌。這不僅會抑制褪黑激素的分泌,更會讓食慾素在深夜裡持續活化,強迫大腦維持在「高覺醒狀態(Hyperarousal)」。 這種令人崩潰的狀態就是,明明你已經累到不行,但大腦卻像停不下來的發電機!
長期的睡眠不足會導致體內促發炎細胞激素上升,而發炎反應又會進一步活化 HPA 軸,分泌更多皮質醇來試圖消炎,高濃度的皮質醇會進一步干擾深層睡眠與快速動眼期(REM),導致睡眠品質變得低弱又破碎,最終形成「壓力-發炎-失眠」的惡行循環。也就是說,你不是在跟睡眠上的意志力作對,而是在跟失控的生理長期鬥爭。
面對這種煞車失靈的失眠困局,科學家們將目光投向了人體內另一個繁榮的生態系:腸道。腸道與大腦之間存在著一條雙向通訊的高速公路,這就是「菌-腸-腦軸 (Microbiome-Gut-Brain Axis, MGBA)」,而某些特殊菌株不僅能幫助消化、排便,更能透過神經與內分泌途徑與大腦對話,直接參與調節我們的壓力調節與睡眠節律。這種菌株被科學家稱為「精神益生菌」(Psychobiotics)。

在眾多研究菌株中,發酵乳桿菌 Limosilactobacillus fermentum PS150 的表現格外引人注目。PS150菌株源於亞洲益生菌權威「蔡英傑教授」團隊的專業研發,累積多年功能性菌株研發經驗的科學成果。針對臨床常見的「初夜效應」(First Night Effect, FNE),也就是現代人因出差、換床或環境改變導致的入睡困難,俗稱認床。科學家在進行實驗時發現,補充 PS150 菌株能顯著恢復非快速動眼期(NREM)的睡眠長度,且入睡更快,起床後也更容易清醒。更重要的是,不同於常見的藥物助眠手段(如抗組織胺藥物 DIPH)容易造成快速動眼期(REM)剝奪或導致睡眠破碎化,PS150 菌株展現出一種更為「溫和且自然」的調節力,它能有效縮短入睡所需的時間,並恢復睡眠中代表深層修復的「Delta 波」能量。
科學家發現,即便將 PS150 菌株經過特殊的熱處理(Heat-treated),轉化為不具活性但保有關鍵成分的「後生元」(Postbiotics),其生物活性依然能與活菌媲美 。HT-PS150 技術解決了益生菌在儲存與攝取過程中容易失去活性的痛點,讓這些腸道通訊員能更穩定地發揮作用 。
在臨床實驗中,科學家觀察到一個耐人尋味的現象:當詢問受試者的主觀感受時,往往會遇到強大的「安慰劑效應」,無論是服用 HT-PS150 還是安慰劑的人,主觀上大多表示睡眠變好了。這種「體感上的進步」有時會掩蓋真相,讓人分不清是心理作用還是真實效益。
然而,客觀的生理數據(Biomarkers)卻揭開了關鍵的差異。在排除主觀偏誤後,實驗數據顯示 HT-PS150 組有更高比例的人(84.6%)出現了夜間褪黑激素分泌增加,且壓力荷爾蒙(皮質醇)顯著下降,這證明了菌株確實啟動了體內的睡眠調控系統,而不僅僅是心理安慰。
最值得關注的是,對於那些失眠指數較高(ISI ≧ 8)的族群,這種「生理修復」與「主觀體感」終於達成了一致。這群人在補充 HT-PS150 後,不僅生理標記改善,連原本嚴重困擾的主觀睡眠效率、持續時間,以及焦慮感也出現了顯著的進步。
了解更多PS150助眠益生菌:https://lihi3.me/KQ4zi
睡眠從來就不只是單純的休息,而是一場生理功能的全面重整。想要重獲高品質的睡眠,關鍵在於為自己建立一個全方位的修復生態系。
這套系統的基石,始於良好的生活習慣。從減少睡前數位螢幕的干擾、優化室內環境,到作息調整。當我們透過規律作息來穩定神經系統,並輔以現代科學對於 PS150 菌株的調節力發現,身體便能更順暢地啟動睡眠開關,回歸自然的運作節律。
與其將失眠視為意志力的抗爭,不如將其看作是生理機能與腸道微生態的深度溝通。透過生活作息的調整與科學實證的支持,每個人都能擁有掌控睡眠的主動權。現在就從優化生活型態開始,為自己按下那個久違的、如嬰兒般香甜的關機鍵吧。

討論功能關閉中。
本文由 肺纖維化(菜瓜布肺)社團衛教 合作,泛科學撰文
在現代醫學的警示清單裡,乳癌、大腸癌這些疾病大家都不陌生;但有一個「隱蔽且致命」的威脅卻常被忽視,那就是「肺纖維化」。其中最常見的類型「特發性肺纖維化」(IPF),其預後往往不太樂觀,確診後的五年存活率甚至比許多常見的癌症還低。
首先,我們得先破解一個迷思:肺纖維化並不是單一疾病,而是許多種間質性肺病的共同表現。當我們聽到「肺纖維化」,腦中常浮現「菜瓜布肺」的形象,患者的肺部外觀充滿一個個空洞與疤痕,像極了乾燥的絲瓜。這精準描繪了肺部組織逐漸硬化、失去彈性的過程。
更重要的是,IPF 這類肺纖維化的威脅在於「不可逆」的特性,一旦形成就很難逆轉。這跟部分 COVID-19 康復者身上、仍有機會復原的肺纖維化,是兩種完全不同的概念。

為什麼好端端的肺會變成菜瓜布?這其實是一場身體修復機制失控的結果。
「纖維化」的組織,就是肺部間質組織(interstitium)的疤痕化。間質是圍繞在肺泡周圍,包含血管與支持肺部結構的結締組織。在正常情況下,肺部損傷後會啟動修復機制,並再生健康組織。但在肺纖維化的患者體內,這套修復機制卻「當機」了。
身體會不斷地發出訊號,導致負責修復工作的「纖維母細胞」(fibroblasts)被過度活化,進而失控地沉積膠原蛋白疤痕組織,最終在肺部形成永久性的纖維化。
科學家發現,這個過程之所以棘手,在於它是一個「惡性循環」,肺部同時存在著「發炎反應」與「纖維化」這兩條路徑 ,它們相互加乘,演變成難以阻斷的強大破壞力。
雖然特發性肺纖維化 (IPF) 的具體成因不明 ,但已知某些特定族群的風險更高。例如抽菸,特定年齡與性別(50歲以上男性)、長期暴露於粉塵環境的工作者(農業、畜牧業、採礦業…)、胃食道逆流者。此外,患有自體免疫疾病(如類風濕性關節炎、乾燥症、硬皮症、皮肌炎/多發性肌炎,)的患者,他們併發肺纖維化的機率遠高於一般人,必須特別警覺。

面對這個不可逆的疾病,醫學界長年束手無策,直到 2014 年才迎來一道曙光。美國 FDA 批准了兩種機制不同的新藥:Nintedanib 和 Pirfenidone。這兩種藥物的出現是治療史上的分水嶺,首度被證實能夠「延緩」IPF 患者肺功能的惡化速度。
然而,這場戰役尚未結束。現有的治療雖然帶來了希望,卻也凸顯了「未被滿足的醫療需求」。從機制上來看,這些藥物主要抑制的是「纖維化路徑」。
這讓科學界開始思考這個未被滿足的棘手問題:既然疾病的本質是「發炎」與「纖維化」的雙重打擊,那麼,我們是否能找到「同時抑制」這兩條路徑的全新策略,從而更有效地打斷這個惡性循環?
為了解決難題,科學家將目光鎖定在一個細胞內的酵素:磷酸二酯酶 4B(PDE4B)。
為什麼鎖定它?讓我們看看它的「雙重作用」機制:
簡單來說,鎖定並抑制 PDE4B,就像是同時抑制了免疫風暴與纖維化的工程,有望從雙從抑制打擊這個惡性循環。
近十年來,全球在肺纖維化領域投入了大量的臨床試驗,我們相信,在科學家逐步破解肺纖維化惡性循環的複雜難題後,期盼未來能為無數患者爭取到更安全、健康的生活與未來。
最後,我們必須再次提醒,特發性肺纖維化(IPF)與漸進性肺纖維化(PPF)是極具破壞性、且不可逆的疾病。面對這個比癌症更致命的對手,雖然現有的治療手段能延緩惡化,但無法逆轉已經形成的肺部疤痕組織,因此「早期診斷、早期治療」仍是對抗肺纖維化最重要的黃金時刻。

討論功能關閉中。

小細胞肺癌惡性高且復發快。如今「PD-L1免疫合併化療」打破治療瓶頸,有效阻斷腫瘤逃逸,讓患者五年存活率翻倍!健保已將其納入一線給付,助病友延長壽命並兼顧生活品質。
「過往小細胞肺癌患者往往在第一線化療結束後,兩、三個月就面臨猛烈復發,高達三分之二的病人活不過一年,身為醫師不禁常感覺束手無策之憾。」三軍總醫院內科部胸腔內科主任蔡鎮良醫師表示,「如今,在PD-L1免疫抑制劑問世後,越來越多小細胞肺癌病友能跨過『存活一年』的門檻,且在進入維持治療後,得以卸下化療的沉重負擔,單用PD-L1免疫抑制劑也有機會穩定控制疾病,重拾美好的日常生活。」
肺癌主要分為小細胞與非小細胞兩大類,其中與抽菸高度相關的小細胞肺癌雖罹病比例逐年下降,僅佔約7-8%,但因其細胞分裂增殖與擴散極快,即使進行低劑量電腦斷層(LDCT)也不一定能早期揪出疾病。小細胞肺癌患者多數確診時已無法進行手術,過往近六成存活期少於一年,能活超過五年者僅約6%,被視為惡性度極高的癌症。
蔡鎮良醫師指出,小細胞肺癌預後極差的關鍵點在於「復發快速」。雖然初期對化學治療反應率高,但極易產生抗藥性;一旦復發,僅剩少數患者對化療仍有反應,也沒有其他有效藥物選擇,導致治療陷入難以突破的瓶頸。
所幸,醫學迎來了近二十年來極為重要的進展–PD-L1免疫抑制劑。蔡鎮良醫師說,醫學界發現小細胞肺癌腫瘤會利用PD-1與PD-L1的結合機制,躲避免疫系統的追殺,就宛如拿著「免死金牌」般。PD-L1免疫抑制劑能精準阻斷這項結合,破解腫瘤的免疫逃逸機制,讓免疫系統重新主動攻擊癌細胞。
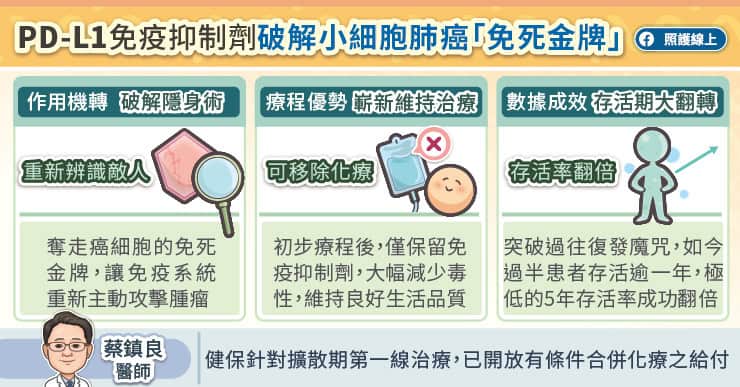
研究證實,PD-L1免疫抑制劑合併化學治療可顯著改善無惡化存活期,降低死亡風險。蔡鎮良醫師分享診間觀察,過往能存活過一年的患者很少,如今可說過半數都有機會可存活超過一年;最新的延續性追蹤更顯示,試驗組的五年存活率從過往的6%成功翻倍達12%,為患者帶來了長達五年的長期生存效益。目前PD-L1免疫抑制劑合併化療,已被國際權威癌症治療指引NCCN列入擴散期小細胞肺癌的第一線治療首選。
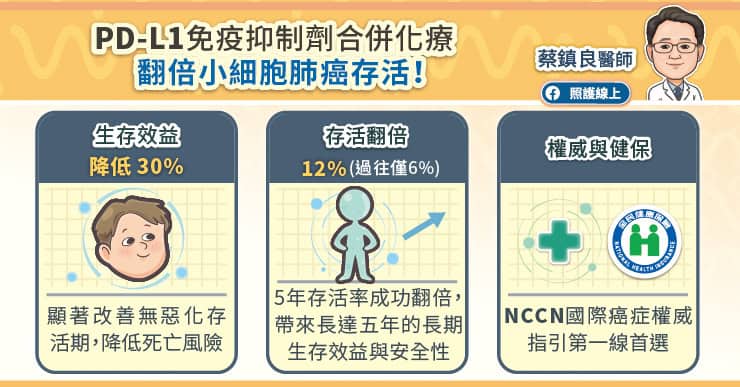
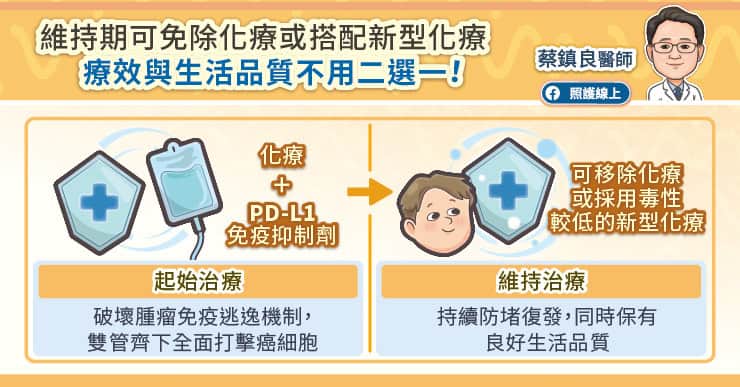
小細胞肺癌免疫合併化療可分為前、後兩治療階段:
在整體治療期間,病友務必落實健康生活,並且「絕對要戒菸」,同時維持充足營養,確保有足夠體力應付療程。PD-L1免疫抑制劑的安全性較高,但仍需配合常規監測甲狀腺、血糖等數值,若出現症狀如皮疹、腹瀉等,請及時向醫師反應。
蔡鎮良醫師說,目前台灣健保針對擴散期小細胞肺癌患者,將PD-L1免疫抑制劑合併標準化療納入第一線給付,至今已滿兩年;給付條件雖限定於「無腦部轉移」,但若經濟許可或有私人保險時,仍建議腦轉移病友自費使用,因為從臨床實際療效來看,PD-L1免疫抑制劑合併化療對腦轉移病患也有效果,長遠也呼籲健保可積極考慮放寬限制,以盡可能嘉惠更多有需要的病友。
討論功能關閉中。