美國科學家利用 CRISPR-Cas9 技術,首度成功修復人類胚胎的遺傳性疾病基因,成功率大幅提高至 72.4%,這項研究成果於今年八月二日發表在《自然》期刊,可說是基因編輯技術進展的里程碑,不過要將這項技術應用於臨床治療,還需要更多的實驗測試才能確定不會有罕見的錯誤發生。
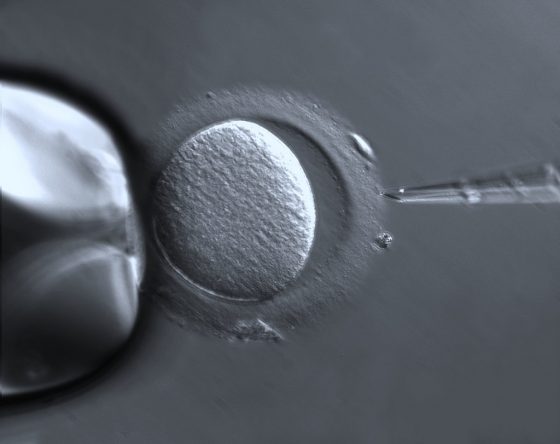
利用 CRISPR-Cas9 修正胚胎中的遺傳性疾病基因
帶領研究團隊的通訓作者,也是《自然》雜誌評選的 2013 年度十大科學家──美國奧勒岡健康與科學大學的米塔利波夫(Shoukhrat Mitalipov)教授,再一次為世界帶來劃時代的研究。他曾以開發出極受爭議的粒線體置換療法(也就是常聽到的三親嬰兒)和利用人類皮膚細胞培養出幹細胞而聞名於世,這次他的團隊的驚世之作,則是將目前超夯的基因編輯技術── CRISPR-Cas9 ──直接注射入胚胎,成功修正遺傳性疾病基因。
研究團隊選擇用來測試的,是常見的遺傳性心臟病──肥厚心肌症(Hypertrophic cardiomyopathy, HCM)的基因,這個疾病平均每500人就有一人患病,而且通常不會在年幼時發病,因此帶有這個遺傳性疾病的基因並沒有因為天擇而消失,好發於中年人以及年輕運動員。
影片/本文所提研究之實驗操作過程
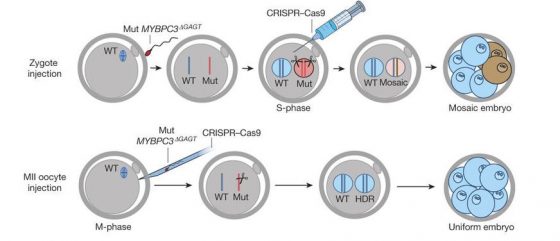
(S-phase injection:受精後18小時注射,M-phase injection:受精前注射)
研究人員為了測試這個方法是否能夠將遺傳性疾病基因修正,他們將 CRISPR-Cas9 注射到帶有一套正常基因和一套疾病基因的受精卵中,看看最後胚胎是否能成功被修正成不帶疾病基因。
實驗室將正常基因的卵子,以及帶有疾病基因的精子,進行體外人工授精,並且在不同的時間注射 CRISPR-Cas9 (「受精前(和精子一起注射)」和「受精後18小時」)。當 CRISPR-Cas9 注射之後,它會辨認出疾病基因,並將該段疾病基因剪切成DNA雙股斷裂,再交由細胞本身的DNA修補機制將DNA修復完成。
他們發現在「受精後」才將 CRISPR-Cas9 注射的話,因為受精卵已經開始進行細胞分裂,所以無法有效的修復胚胎內所有的細胞,使得部分胚胎內含有不同基因組的細胞(如下圖上排最右邊,藍色是正常細胞,褐色是仍含有疾病基因的細胞),而形成鑲嵌式胚胎(Mosaic embryo),或者是完全沒有被修復,胚胎內仍然具有基因缺陷。成功被修復的比例約 66.7%(36/54)。
如果在「受精前」將精子、CRISPR-Cas9 和正常基因片段一起注射,就能在 DNA 開始複製前進行修復,獲得較佳的修復結果。研究人員分析發現,所有的胚胎都進行了基因修復的步驟,72.4%的胚胎修復成功(42/58),剩下其他的胚胎則是正確辨認疾病基因的位置,但修復失敗了。
研究團隊還發現,在使用這個基因修正的方法時,胚胎會使用本身的 DNA 進行修復,而非研究人員額外加入的 DNA 片段,意思是在胚胎發育初期,只會根據原本就存在於細胞中的基因進行修正,而不會使用外來的基因片段。這和他們一開始預期的不同,顯示胚胎在發育的早期修復 DNA 的機制可能和後期所使用的不太一樣。
同時為了要檢驗 CRISPR-Cas9 在運作時,是否錯誤的處理到其他基因,造成了不必要的突變(這種突變稱為「脫靶突變 off-targeting mutation」),他們也做了胚胎的全基因組定序。他們發現在所有正常基因的細胞裡面,完全沒有這樣的現象發生,這也顯示了這個基因修正方法的可行性與穩定性大大的提高。
技術突破使成功率大增,但仍需要更多實驗確認安全性
這項研究是由米塔利波夫的團隊聯合南韓與中國的團隊共同進行。雖然在他們發表之前,還有另外三個中國團隊也發表過使用 CRISPR-Cas9 來修正胚胎基因的研究,但他們這項研究的重要性,在於首次有這麼高的成功率,能直接對人類胚胎進行基因工程修正遺傳性疾病基因,並且大大減少了鑲嵌式胚胎的數量,以及 CRISPR-Cas9 常被質疑的問題:脫靶突變的現象,也沒有被偵測到。
雖然成功率目前只有 72%,不過米塔利波夫對此有信心可以藉由調整實驗條件來達到成功率 90%以上。儘管如此,仍然要謹慎面對這項技術,這樣的技術算是生殖細胞工程(Germline engineering),會使得修正後的基因能夠傳到後代子孫,如果失敗的話,將導致突變或疾病基因代代相傳,研究中的實驗數據量也只有五十幾,還需要更多的實驗才能確定不會有罕見的錯誤發生。
設計出你的理想寶寶?還有很長一段路要走
有人說:這個胚胎基因編輯技術成功後,「設計嬰兒」就指日可待了。《自然》期刊的評論員 Heidi Ledford 在 Nature Podcast 的訪問中表示,這樣的想法是個「滑坡謬誤」。這個利用 CRISPR-Cas9 修正胚胎基因的方法,只能將有問題的部分修改成原本就已經存在的基因序列(例如實驗中父方的疾病基因被修正為母方的正常基因),無法說我選擇要這樣的眼睛、這樣的鼻子、或者超高 IQ,然後提供一段基因片段,就把你的「完美寶寶」製造出來,這個方法做不到,而且技術上還有很多困難要克服,還有很長的一段路要走。而這大概也是通訊作者米塔利波夫堅持使用「基因修正(correction)」來描述他們的方法,而非使用「基因編輯(editing)」的原因。
麻省理工學院的一位癌症研究學者 Richard Hynes 認為,一旦胚胎基因修正技術的困難被克服,那我們就需要開始思考與討論這項技術對社會的影響,以及該如何立法規範這種技術的使用。而這篇堪稱里程碑的研究,就是告訴我們,是時候該開始討論了。
參考資料:
- Correction of a pathogenic gene mutation in human embryos, Nature (2017), Hong Ma et al., doi:10.1038/nature23305
- Biotechnology: At the heart of gene edits in human embryos, Nature | News & Views (2017), Nerges Winblad & Fredrik Lanner, doi:10.1038/nature23533
- CRISPR fixes disease gene in viable human embryos, Nature | News (2017), Heidi Ledford, doi:10.1038/nature.2017.22382
- In Breakthrough, Scientists Edit a Dangerous Mutation From Genes in Human Embryos, New York Times
- Deadly gene mutations removed from human embryos in landmark study, The Guardian
- First Human Embryos Edited in U.S. – MIT Technology Review, July 26, 2017
延伸閱讀:
- 打造完美寶寶,工業技術與資訊月刊285期2015年07月號
- 「DNA編輯大師」張鋒與CRISPR / Cas9 / Cas9基因編輯技術 – PanSci泛科學
- 《自然》雜誌2013年度十大人物 – PanSci泛科學
- CRISPR發展之英雄榜 – 科學Online