- 作者/照護線上編輯部
- 本文轉載自 Care Online 照護線上《成人急性淋巴性白血病(ALL)進展快、易復發,微量殘留病灶檢測(MRD)助調整治療策略,專科醫師圖文解說》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接

「有位六十多歲的女士因為頭暈、虛弱、疲勞而就醫,結果發現血球數量嚴重異常,紅血球與血小板數量偏低,且有大量不成熟的淋巴球,進一步檢查才發現竟是急性淋巴性白血病(Acute Lymphoblastic Leukemia,簡稱 ALL)引起。」臺北榮民總醫院內科部輸血醫學科簡聖軒醫師指出,「由於急性淋巴性白血病的病程進展快速,所以個案在確診後,就有即刻治療的必要。」
然而,患者因為身體機能相對較差,難以接受完整的化學治療,治療成效有待加強,遲遲未達殘留病灶檢測(MRD)陰性。所幸,後來透過免疫治療大幅殲滅癌細胞,並接續使用異體幹細胞移植,穩定控制疾病至今。
急性淋巴性白血病發作,貧血、瘀青、發燒、淋巴結腫大是警訊
急性淋巴性白血病源自淋巴球的惡性病變,正常的淋巴性芽細胞原本會分化成淋巴球,但是在癌化之後,產生了大量不成熟的細胞,這些多而無用的淋巴球會壓迫到正常血球的生成,進而衝擊患者的健康、甚至危及性命。
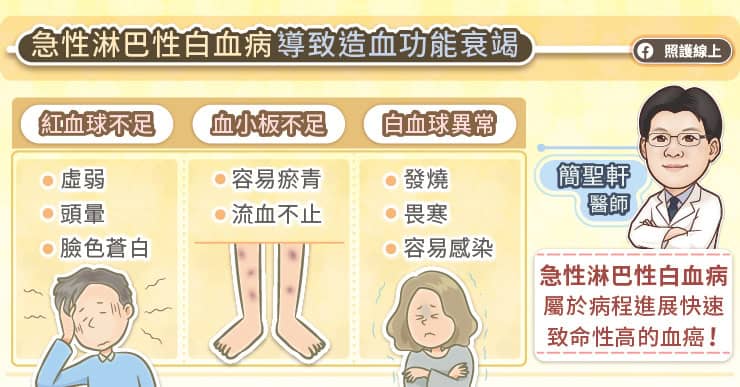
急性淋巴性白血病的症狀與造血功能衰竭有關,簡聖軒醫師指出,紅血球數量偏低會讓患者出現臉色蒼白、頭暈、虛弱等貧血的狀況,血小板數量偏低會讓患者容易出現瘀青、流血不止的狀況,白血球數量異常會讓患者容易遭到感染而發燒、畏寒。另外還可能出現淋巴結腫大、脾臟腫大、骨頭疼痛、夜間盜汗、體重減輕等症狀。
簡聖軒醫師說,急性淋巴性白血病剛發病時,患者可能覺得身體有些不舒服,不過也許經過一、兩個禮拜的時間,症狀就會變得很嚴重,甚至危及性命。
大人、小孩都可能發生急性淋巴性白血病,在台灣每年大約有三百個新病例。簡聖軒醫師說,突然罹患急性淋巴性白血病,對患者是很大的衝擊,諸如就學、工作、婚姻、生育等計畫,都可能被迫中斷,往往需要一段時間才有辦法調適、接受。
微量殘留病灶檢測(MRD)幫助調整治療策略
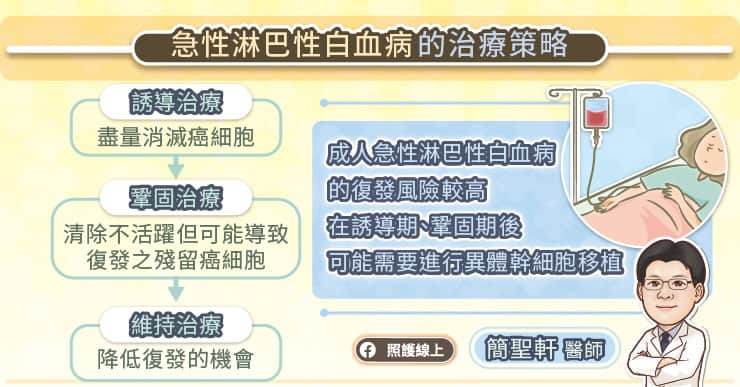
由於急性淋巴性白血病的進展相當快,所以在確定診斷後,便要盡快接受治療。簡聖軒醫師說,第一階段為誘導治療,以高劑量化學治療為主,並視基因突變的狀況加入標靶藥物,盡量消滅癌細胞;第二階段為鞏固治療,希望清除那些不活躍但可能再生長並導致復發之殘留白血病細胞,此階段可以依患者狀況,適時的加入免疫治療強化癌細胞的清除成效;第三階段為維持治療,希望藉由低劑量藥物降低復發的機會。
為了評估治療成效,現在可使用「微量殘留病灶檢測(Measurable Residual Disease,簡稱MRD)」。簡聖軒醫師說,微量殘留病灶檢測(MRD)運用流式細胞儀或基因檢測,靈敏度高,可偵測到殘留在體內微量的癌細胞,讓醫師能根據檢測結果,判斷治療成效以及即時調整治療策略。
值得一提的是,成人急性淋巴性白血病的復發風險較高,可能需要進行異體幹細胞移植。簡聖軒醫師說,在做異體幹細胞移植之前,會希望盡可能把癌細胞清乾淨,因此,是否可以達成殘留病灶檢測(MRD)陰性是一大關鍵。但若在誘導治療時,仍未達成微量殘留病灶(MRD)陰性,則可視情況加入免疫治療,提升微量殘留病灶(MRD)陰性的機率。
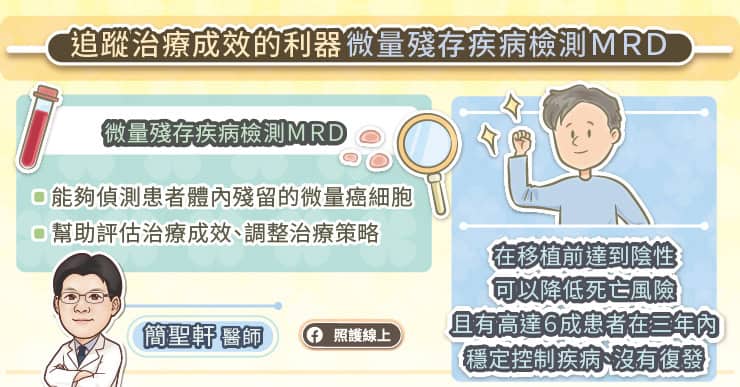
在急性淋巴性白血病的治療與追蹤過程中,微量殘留病灶檢測(MRD)是重要指標,能夠幫助醫師決定要不要繼續做治療,要不要考慮異體幹細胞移植。微量殘留病灶檢測(MRD)陰性達標後再進行異體幹細胞移植,患者的死亡與復發風險較低,也有高達 6 成的患者在三年內穩定控制疾病、沒有發生復發1。
微量殘留病灶檢測(MRD)與包含免疫治療在內的精準治療已納入健保給付,幫助急性淋巴性白血病患者提升治療成效,減輕經濟負擔。
急性淋巴性白血病的治療持續進步,患者務必與醫師密切配合,才能達到較佳的預後。
筆記重點整理
- 急性淋巴性白血病 ALL 病程進展快速,屬於高致命性、低存活率的血癌。剛發病時,患者可能覺得身體有些不舒服,不過也許經過一、兩個禮拜的時間,症狀就會變得很嚴重,甚至危及性命。
- 急性淋巴性白血病的症狀與造血功能衰竭有關,紅血球數量偏低會讓患者出現臉色蒼白、頭暈、虛弱等貧血的狀況,血小板數量偏低會讓患者容易出現瘀青、流血不止的狀況,白血球數量異常會讓患者容易遭到感染而發燒、畏寒。另外還可能出現淋巴結腫大、脾臟腫大、骨頭疼痛、夜間盜汗、體重減輕等症狀。
- 急性淋巴性白血病的治療,第一階段為誘導治療,以高劑量化學治療為主,並視基因突變的狀況加入標靶藥物,盡量消滅癌細胞;第二階段為鞏固治療,希望清除那些不活躍但可能再生長並導致復發之殘留白血病細胞;第三階段為維持治療,希望藉由低劑量藥物降低復發的機會。成人急性淋巴性白血病的復發風險較高,可能需要進行異體幹細胞移植。
- 在治療與追蹤過程中可使用微量殘留病灶檢測(MRD)評估治療成效。微量殘留病灶檢測(MRD)陰性達標後再進行異體幹細胞移植,患者的死亡與復發風險較低,也有高達6成的患者在三年內穩定控制疾病、沒有發生復發1。
參考資料:
- Bar M, et al. Leuk Res Treatment. 2014;2014:421723.
- 本文轉載自 Care Online 照護線上《成人急性淋巴性白血病(ALL)進展快、易復發,微量殘留病灶檢測(MRD)助調整治療策略,專科醫師圖文解說》,歡迎喜歡這篇文章的朋友訂閱支持 Care Online 喔
- 加入照護線上 LINE 官方帳號,健康資訊不漏接